Таблица по биологии (амебы и прочие твари) реферат по биологии
Тип Простейшие. Класс Саркодовые.Амеба. Бактерия Вакуоль пищеварительная вакуоль сократительная вакуоль Выделять- что? куда? Выделить-с помощью чего? Выделение Двигаться -как? c помощью чего? Движение Диссимиляция Дышать-как? чем? Он , она дышит, они дышат Дыхание Жидкий продукт Захватывать-что ? с помощью чего? Инцистироваться /рисовать/ Класс Неблагоприятные условия Образовать- вокруг чего? что? Переваривать Перевариваться-где? Питаться -как? чем? /читать/ Питание +р. п. Пища Поверхность Представитель . Пресная вода Простейшее животное Псевдоподия Размножаться -как? -чем? Размножение +р.п. Cаркодовые животные Тип Условия плохие условия Циста Тип Простейшие. Класс Жгутиковые.Эвглена Глазок Глотка Жгутик Зеленый /ая, ое, ые/ Зеленая эвглена Клеточный рот Поглощать что? /читать/ Попадать куда? во что? Продольное деление Резервуар Свет на свету Содержаться где? он, она, содержится, они содержаться Способ способ питания Стигма/глазок/ Фотосинтез Волосок /чувствительный/ Выполнять что? функцию нападения функцию защиты Гермафродит Гидройдные животные Диффузный /ая,ое,ые/ Зигота Капсула Кишечнополостные животные Клетка железистая клетка интерстициальная клетка нервная клетка половая клетка стрекательная клетка эпителиальномускульная клетка Кусок Кусочек пищи Мезоглея Оплодотворение перекрестное оплодотворение Отделятся- от чего? Отросток /вырост/ Передавать-что? Подошва Полость Почка Почкование Расти /идти/ Слой Соединение Сперматозоид Способ питания внутриклеточный способ питания внутриполостный способ питания Способ размножения половой способ размножения бесполый способ размноже- ния Ферменты Щупальца Эктодерма Энтодерма Яйцеклетка Тип Кольчатые черви. Класс Малощетинковые черви.Дождевой червь. Анус Бок левый бок правый бок Брюшко Воронка Вперед/назад Всасывать -что? Всасываться -где? Ганглий /узел/ Дождевой червь Желудок Замкнутый/ая,ое.ые/ Зоб Кишка задняя кишка средняя кишка Кольцо окологлоточное кольцо Кольцевой сосуд Кольчатый червь Комиссуры Конец головной конец хвостовой конец Малощетинковые черви Мышцы кольцевые мышцы продольные мышцы Отверстие -где? Открываться-где? Пищевод Сердце Система выделительная система кровеносная система пищеварительная система Сокращаться Сосуд
Класс Малощетинковые черви.Дождевой червь. Анус Бок левый бок правый бок Брюшко Воронка Вперед/назад Всасывать -что? Всасываться -где? Ганглий /узел/ Дождевой червь Желудок Замкнутый/ая,ое.ые/ Зоб Кишка задняя кишка средняя кишка Кольцо окологлоточное кольцо Кольцевой сосуд Кольчатый червь Комиссуры Конец головной конец хвостовой конец Малощетинковые черви Мышцы кольцевые мышцы продольные мышцы Отверстие -где? Открываться-где? Пищевод Сердце Система выделительная система кровеносная система пищеварительная система Сокращаться Сосуд
Оборудование: Таблица «Тип Простейшие» Фрагмент видеофильма «Амеба» Фрагмент видеофильма «История открытия одноклеточных организмов» Ход урока
ответом
Описание контрольных измерительных материалов для проведения промежуточной аттестации 5 класс 1.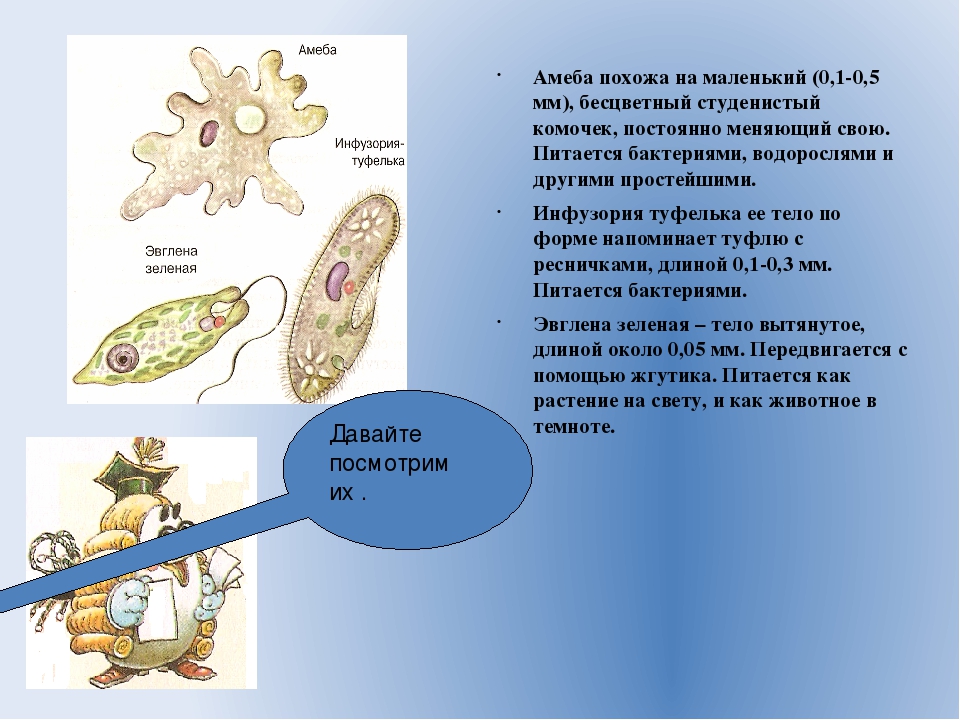 Документы, определяющие содержание проверочной работы Содержание и структура проверочной работы определяются
Документы, определяющие содержание проверочной работы Содержание и структура проверочной работы определяются
Открытый урок в 7 классе
Открытый урок в 7 классе Тема: «Многообразие одноклеточных животных и их значение». Форма проведения: аукцион знаний. Цели: — обобщить и закрепить знания о типе Простейшие, об отдельных его представителях
Урок 5. Общая характеристика бактерий
Глава 2. МНОГООБРАЗИЕ ЖИВЫХ ОРГАНИЗМОВ ЦАРСТВО БАКТЕРИЙ Урок 5. Общая характеристика бактерий Что вам известно о бактериях? Знакомство с многообразием живых организмов мы начнем с самых многочисленных
Подробнее1. Пояснительная записка
1. Пояснительная записка Данная программа составлена с учетом следующих нормативнометодических документов: Федеральный закон от 29. 12.2012г. 273-ФЗ «Об образовании в Российской Федерации». Федеральный
12.2012г. 273-ФЗ «Об образовании в Российской Федерации». Федеральный
учебный год
Государственное бюджетное общеобразовательное учреждение средняя общеобразовательная школа 242 с углубленным изучением физики и математики Красносельского района Санкт-Петербурга Принята Педагогическим
Подробнее1. Пояснительная записка:
1. Пояснительная записка: Рабочая программа по биологии разработана в соответствии: С Федеральным государственным образовательным стандартом основного общего образования, утвержденный приказом Министерства
ПодробнееБИОЛОГИЯ Живые организмы
2.2.2.10. БИОЛОГИЯ Живые организмы Биология как наука. Роль биологии в практической деятельности людей. Разнообразие организмов. Отличительные признаки представителей разных царств живой природы. Методы
Методы
БИОЛОГИЯ. 5 класс МОСКВА «ВАКО»
БИОЛОГИЯ 5 класс МОСКВА «ВАКО» УДК 372.857 ББК 74.262.8 К64 Издание допущено к использованию в образовательном процессе на основании приказа Министерства образования и науки РФ от 14.12.2009 729 (в ред.
Подробнее6 КЛАСС (68 ч) Введение
БИОЛОГИЯ. «ЖИВОЙ ОРГАНИЗМ». 6 КЛАСС (68 ч) Введение Биология наука о живых организмах. Из истории развития биологии. Современная биология. Важность биологических знаний для развития медицины, сельского
ПодробнееКТП на учебный год по биологии 9 класс
КТП на 2015-2016 учебный год по биологии 9 класс п/п Тема урока Дата КЭС 1. Введение. Биология наука о жизни 1. Многообразие живого мира. 2. Основные свойства живых 3. Развитие биологии в додарвинский
ПодробнееУДК :57 ББК 28.
 0я72 С62
0я72 С62УДК 373.167.1:57 ББК 28.0я72 С62 С62 Сонин, Н. И. Тематические тесты к учебнику А. А. Плешакова, Н. И. Сонина «Биология. Введение в биологию. 5 класс» / Н. И. Сонин. 3-е изд., стереотип. М. : Дрофа, 2017.
ПодробнееЖивые клетки. Вариант 1
Тест 1 Живые клетки. Вариант 1 1. Живая клетка представляет собой: 1) простое вещество 3) часть живого организма 2) сложное вещество 4) часть неживой природы 2. Полужидкое вещество, которое заполняет клетку,
ПодробнееВодоросли низшие растения
Водоросли Водоросли низшие растения Водоросли обширная и неоднородная группа низших растений. Водоросли самые многочисленные и одни из самых важных для планеты фотосинтезирующих организмов. Они встречаются
Подробнее Проект по биологии на тему: «Клетка»
Муниципальное общеобразовательное учреждение средняя общеобразовательная школа 1 Проект по биологии на тему: «Клетка» Выполнила: Кизка Е. А. Проверили: Дронова А. О. Калуцкая Н.Н. Хабаровск 2008 История
А. Проверили: Дронова А. О. Калуцкая Н.Н. Хабаровск 2008 История
ЛАБОРАТОРНАЯ РАБОТА 5
ЛАБОРАТОРНАЯ РАБОТА 5 Тема: «Сравнение клеток растений, животных, грибов и бактерий» Цель: Закрепить умение готовить микропрепараты и рассматривать их под микроскопом, находить особенности строения клеток
ПодробнееСИСтЕМа ОРГаНИчЕСКОГО МИРа
СИСтЕМа ОРГаНИчЕСКОГО МИРа Все существующие на Земле организмы разделены на четыре царства: Дробянки, Грибы, Растения, Животные. Дробянки относятся к прокариотам (доядерным организмам), грибы, растения,
ПодробнееПОЯСНИТЕЛЬНАЯ ЗАПИСКА
ПОЯСНИТЕЛЬНАЯ ЗАПИСКА Сведения о программе Рабочая программа составлена на основе авторской программы В.В. Пасечника «Биология. Бактерии, грибы, растения. 5 класс» (Рабочие программы. Биология. 5 9 классы:
Биология. 5 9 классы:
Изучение темы: «Простейшие» в 7-м классе
Урок 1 Тема Среда обитания, строение и дыхание простейших.
Задачи:
1. Способствовать изучению
особенностей строения одноклеточных животных
(простейших)
2. Подвести учащихся к пониманию единства
органического мира.
3. Закрепить умение работать с микроскопом.
4. Использовать активные формы и приемы работы с
целью проявления личного уровня зунов.
Понятия: Одноклеточное животное, дыхание, питание, хищник,
Оборудование:
1. На каждую парту микроскоп.
2. Таблицы “Простейшие” “Хламидомонада”.
3. Микропрепараты “Амеба”, “Эвглена”,
“Туфелька”.
Ход урока.
1. Вступительное слово учителя:
Простейшие — это первая группа животных, которую мы изучаем. Как вы думаете, что мы о них должны узнать?
1) строение,
2) среда обитания,
3) как дышат; как размножаются; как передвигаются?
На эти вопросы мы с вами и будем отвечать.
1) История открытия – сообщение
учащегося.“300 лет назад жил в г. Дельфте, что в
Голландии шлифовальщик стекол Антон Левенгук.
Через свои стекла он рассматривал окружающий
его мир. Взяв застоявшуюся воду из бочки, он
увидел в ней движущиеся организмы. Левенгук
очень удивился и назвал их ничтожнейшими
зверушками. Позднее ученые дали им название
простейшие. Заслуга Левенгука перед наукой
велика: во-первых, он открыл не видимых
невооружённым глазом животных. И, во-вторых, он
сделал микроскоп орудием изучением природы”.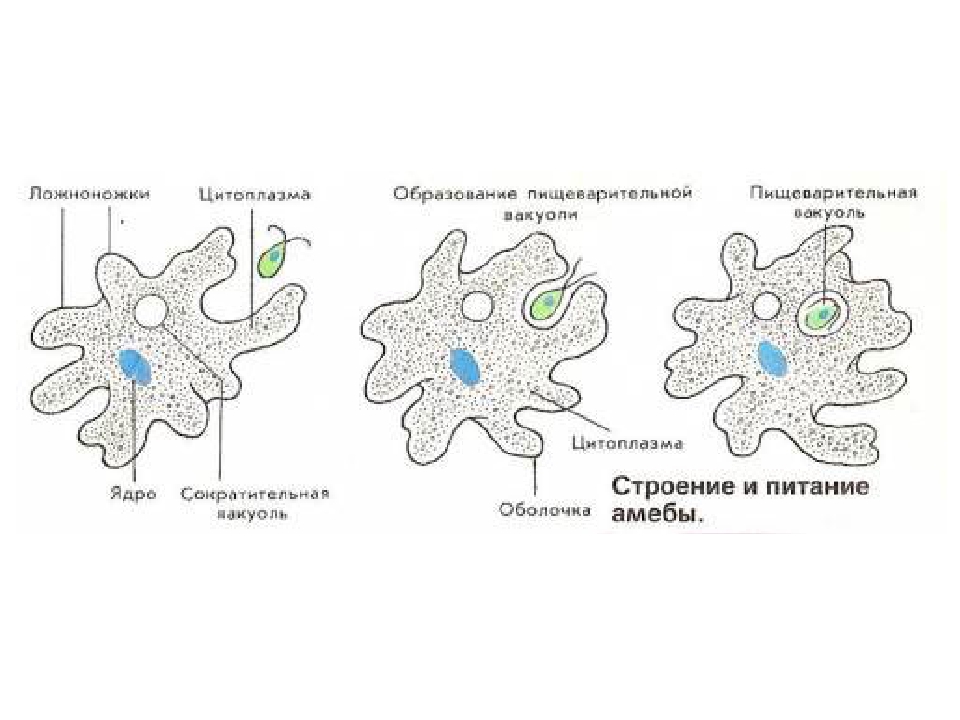
2) Изучение строения простейших.
– Приготовьте таблицу (1) как на доске. Надписи сделайте точно также.
царство |
животные |
||
Вид |
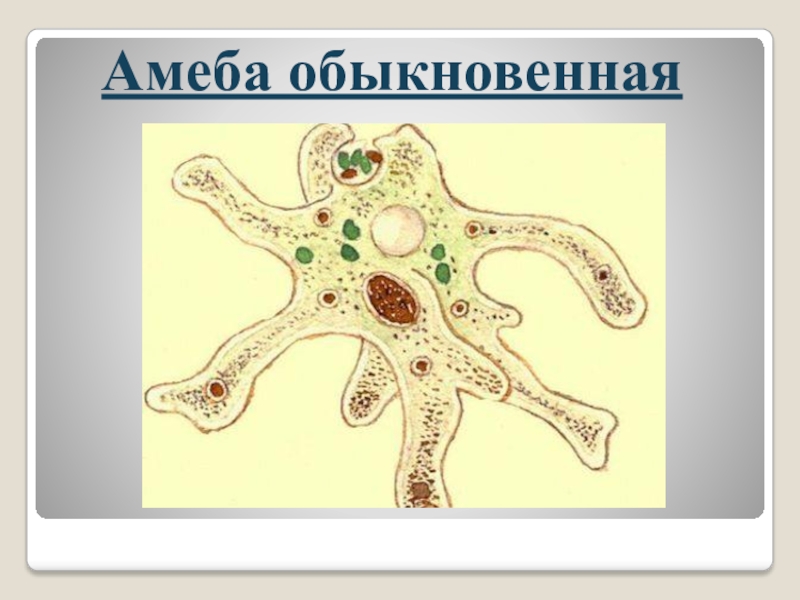
Амеба обыкновенная |
Эвглена зеленая |
Туфелька обыкновенная |
Строение |
Ложноножка Оболочка Цитоплазма Сократительная вакуоль Ядро Пищеварительная вакуоль
|
Жгутик Стигма Сократительная вакуоль Оболочка ХлоропластЦитоплазма Ядро Запасные питательные вещества |
Реснички Сократительная вакуоль Пищеварительная вакуоль Ядро М. Рот Порошица Цитоплазма Оболочка |
Среда |
Загрязненная |
С гнилыми листьями |
Загрязненная |
Движение |
Ложноножки |
Жгутики |
Реснички |
Питание |
Гетеротрофное, хищник |
Гетеротрофное, автотрофное |
Гетеротрофное, хищник |
Дыхание |
Кислород поступает через поверхность |
Кислород поступает через поверхность | Кислород поступает через поверхность |
Размножение |
Деление клетки |
Деление клетки |
Деление клетки, конъюгация |
– Какие особенности строения можем
отметить у каждого организма, рассматривая
микропрепарат, читая текст, стр. 11, 14, 16 и
рассматривая рисунки (1, 4, 7). Обсуждаем в парах, (на
каждой парте какой-то препарат) и зарисовываем на
доске и в тетрадях.
11, 14, 16 и
рассматривая рисунки (1, 4, 7). Обсуждаем в парах, (на
каждой парте какой-то препарат) и зарисовываем на
доске и в тетрадях.
4. Внимательно рассмотрите рисунок в тетради. Чем отличаются эвглена от амебы и туфельки.
– Наличием хлоропластов.
5. Сравним ее с хламидомонадой (Таблица на доске).
– Наблюдается большое сходство, что указывает на родство между растительным и животным миром.
6. Как вы думаете, в какой среде могут жить эти животные и почему?
– В воде, потому что имеют очень тонкую оболочку, которая не может защитить их от потери воды.
7. Уточним сведенья о среде по учебнику, обсудим в парах, выскажемся, занесем таблицу.
8. Питание простейших.
Вспоминаем, на какие группы делятся по способу
питания. Работаем в группах. Озвучиваем.
Читаем статьи в учебнике стр. 11–1 ряд; стр. 14–2 ряд; стр. 16–3 ряд. Рассказываем у настенной таблицы. Заносим в таблицу пункт “Питание”.
9. Дыхание простейших. Подумайте и скажите, как могут дышать эти животные? Объяснить.
– Через всю поверхность тела О2 поступает внутрь тела.
3. Закрепление. Обратим внимание на наши цели, что мы хотели узнать:
1) Какая среда обитания?
2) Строение:
а) Из каких частей состоит клетка?
б) Что находится под оболочкой?
в) Что кроме цитоплазмы и ядра находится в клетке простейших?
3) Чем является клетка простейших?
4) Почему мы говорим о связи растительного и животного мира?
5) Каковы заслуги Левенгука перед наукой.
4. Домашнее задание: статьи на
страницах 11,14,16.
Домашнее задание: статьи на
страницах 11,14,16.
5. Заключение. Спасибо всем за урок. Оценки! На следующий урок продолжим изучение.
Урок 2. Тема: Процессы жизнедеятельности простейших.
Задачи:
1. Изучить процессы жизнедеятельности у одноклеточных организмов.
2. Закрепить понятие о систематике животных.
3. Развивать умение делать выводы и обобщения.
Понятия: Вид, класс, царство, обмен веществ.
Оборудование:
1. Микроскопы.
2. Культура инфузорий.
3. Лабораторное оборудование.
4. Таблицы “ Простейшие”, “Хламидомонада”.
5. Лабораторное оборудование.
6. Соль.
7. Аппликации “ Размножение”.
Ход урока.
I. Актуализация знаний (вопросы учителя)
1. Вспомним, какие цели вы выдвинули на прошлом уроке?
2. Какие из этих целей мы достигли?
3. Какова среда?
Какова среда?
4. Почему именно вода?
5. Как дышат? Какой газ используют?
6. Что общего в строении у всех простейших – (их тело состоит из одной клетки).
II. Изучение нового материала.
1. Передвижение туфельки. Рассматриваем под микроскопом, читаем в учебнике стр. 11,14,16, обсуждаем в парах. Рассказываем о движении туфельки, амёбы, эвглены. Заносим данные в таблицу.
2. Деление простейших на классы.
Как связано наличие того или иного органа передвижения с принадлежностью к классу?
(Работаем в парах, используем настенную таблицу и таблицу в тетради). Делаем вывод, данные заносим в таблицу. Обращаем внимание на название вида.
Процессы обмена веществ.
Подумайте, обсудите в парах и скажите, какие вещества поступают в тело, а какие выделяются и как.
Деление клетки. Коньюгация. Заносим пунктом 4 в таблицу.
4. Размножение – вспомните, как размножается
хламидомонада. Учитель рассказывает о
размножении простейших, используя аппликации.
Заносим в таблицу пункт .
Учитель рассказывает о
размножении простейших, используя аппликации.
Заносим в таблицу пункт .
5. Раздражимость – посмотрите, что произойдёт, если вы в свой микроскоп положите хрусталик соли. (Вносим хрусталик к краю кожи).
6. Что наблюдаете?
Вывод: Животное обладает способностью реагировать на раздражители – это свойство раздражимости. Им обладают все. Амёбы плывут к бактериям. Эвглена плывёт на свет. Заносим в таблицу пунктом .
III. Заключение к уроку.
Мы с вами закончили изучение группы животных под названием простейшие.
1. Почему их так называют?
2. На какие классы делят и почему?
3. Какие свойства организма присущи простейшим?
IV. Домашнее задание.
Параграф 3,4,5. Сообщения “Раковинные корненожки”, “Паразитические простейшие”.
Урок 3. Урок – путешествие “ По морям, по волнам”
Тема: Общая характеристика простейших”
Задачи:
1. Обобщить знания о простейших как
одноклеточных животных.
Обобщить знания о простейших как
одноклеточных животных.
2. Совершенствовать умения выделять главное.
Оборудование:
1. “ Чемоданчик с карточками”
2. Магнитная доска
3. Иллюстрация “ 9 вал ”
4. Карточки счетчики (на каждого)
5. Аппликация “ Деление простейших “
6. Доска с карманчиком
7. Пакет с карточками “ Таксономические единицы”
8. Силуэты животных (у каждого)
Содержание урока. Звучит музыка “ По морям, по волнам “
Условия игры: Урок проводится в форме путешествия. Учащиеся перевоплощаются в матросов. Разбиваются на 3 команд , каждому выдается карточка – счетчик .
- Проверка снаряжения
- Метеосводка. На доске прикреплены 3 иллюстрации картины Айвазовского “9 вал ”, на обратной стороне которых есть вопрос и задание. Под каждым рисунком подпись “Шторм”, если ученик правильного ответил на вопрос, меняется на “Штиль” – отплытие разрешается.
“Что возьмем в дорогу”. В “ чемоданчике “
матроса находятся карточки с терминами, которым
учащиеся должны уметь дать четкую формулировку :
ложноножка, жгутик, реснички, пищеварительная
вакуоль, сократительная вакуоль, циста, ротовое
отверстие, глотка, раздражительность, обмен
веществ.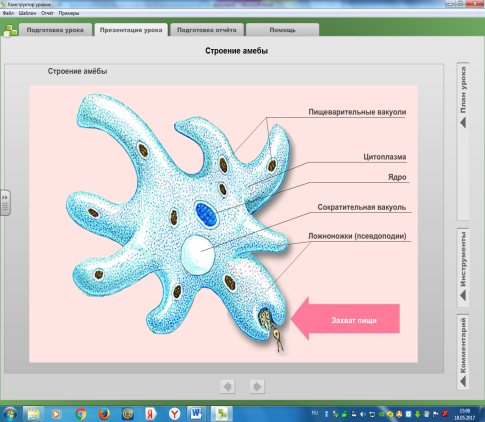 Эти карточки помещаем на магнитную
доску.
Эти карточки помещаем на магнитную
доску.
Вопросы и задание для эрудитов (4б)
- На обратной стороне нарисована туфелька.
Какое животное здесь изображено? Какое значение имеет для него способность к передвижению?
2. Нарисована эвглена зеленая . Какое животное здесь нарисовано? Как оно питается?
3. Нарисована амеба . Как происходит у нее процесс размножения (по аппликации)?
III. Тренажер:
1. Восстанови порядок (4б) ,работа в паре, от каждой команды 2 человека
– На пару выдается конверт с карточками и доска с карточками. Разложить правильно.
Карточки класс (1шт) ,царство (1шт), животные (1), корненожки (1), эвглена(1), амеба (1), туфелька(1), зеленая (1) , обыкновенная (2).
Результат демонстрируется классу и обсуждается.
2. “Смотри, не забывай “– за каждый правильный ответ 0,5 балла, сигналят силуэтом животного
а) какое животное передвигается с помощью ложноножек?
б) у какого животного есть светочувствительный глазок?
в) у какого 2 ядра?
г) у какого животного есть жгутик?
д) у какого животного тело покрыто очень тонкой оболочкой?
ё) у какого животного есть реснички?
ж) какое может питаться как растение?
з) какое животное имеет две сократительные вакуоли?
к) какое животное захватывает пищу ложноножками?
л) у какого животного есть рот?
м) у какого животного есть 1 ядро?
н) какое животное является хищником?
о) образуются запасные питательные вещества?
п) имеет порошицу?
3. “Угадай, кто спрятался (5б) на каждого карточка со схемами. Узнать, какое животное под какой буквой (из таблицы пункт 4). Оцениваем по образцу (высший балл 5). Устно озвучиваем ответ .
4. “Отгадай задуманное животное (2б). На доске силуэты простейших . Учитель берет рисунок любого ( дети не видят, и отвечают только “да “ или “нет”). Вопросов каждая команда может задать не более 4. Например:
– У него есть хлоропласты?
– По способу питания это хищник?
– Имеет не определённую форму тела? – ответ “Амеба”
5. Кто лишний (3 балла). Работает группа из трех человек. Выдаются пакеты с изображениями: амебы, туфельки, эвглены, гидры, обозначенные буквами ( А,Б,С,Д)
– Назвать лишнее и объяснить почему.
6. Конкурс художников(2б). На классной доске изображены фрагменты тел простейших.
– Узнать, объяснить по какому признаку узнали .
IV. Подведение итогов – Мы преодолели уже много преград. Подсчитали свои достижения ( по командам) одной команде так держать, другой молодцы, третьей не сдаваться без боя, главные преграды впереди. Встречаемся на следующем уроке. Звучит музыка.
Урок 4. Урок – путешествие “По морям, по волнам”.
Тема: Многообразие простейших, их роль в природе и жизни человека.
Задачи:
1. Расширить знания учащихся о простейших животных.
2. Выяснить роль простейших в природе и жизни человека.
3. Совершенствовать умения учащихся оценивать свой труд.
Оборудование:
1. Таблицы настенные
2. Карточки – задания
3. Иллюстрации к сообщениям.
Содержание урока.
I. Учитель – наше путешествие продолжается. Нам осталось преодолеть несколько опасных мест – и мы у цели. Не забывайте отмечать свои достижения.
Звучит музыка “По морям, по волнам”.
Препятствие “Бриз”.
II. На каждую парту 2 конверта. До черты – это обязательный уровень; После черты – повышенной трудности. Высший – более 10.
1. Эвглена, амёба, туфелька живут…
2. Их тело – это одна…
3. Клетка имеет 3 основные части…,…,…
4. При дыхании они поглощают…
5. Все они размножаются способом…
6. Кислород в тело простейших
7. Амёба и туфелька по способу питания…
8. Движение эвглены на свет и туфельки в сторону бактерий – это…
9. У эвглены есть…, поэтому она питается как…
10. При наступлении неблагоприятных условий у простейших образуется…
Первая остановка: Интересная история (Сообщение о раковинных корненожках)
III. Препятствие “Шторм”. 14 баллов.
На каждую группу. Шуточный рассказ с ошибками.
“Дорогие мама и папа! Служба у меня идёт хорошо. При увольнении на берег я в парке увидел амёбу. Она росла на клумбе и была красивого изумрудного цвета. Возвращаясь на корабль, я решил отдохнуть на чистых трудах; Вода в них хрустально чистая. Вижу, плавают в ней маленькие прозрачные эвглены, все покрытые курчавыми ресничками. А вслед за ними, туфельки. И машут им своими жгутиками. Удивился я на такие чудеса, да и пошёл к себе на корабль.
Любящий вас сын Ваня.
Вторая остановка “Сообщение о паразитических простейших”.
IV. Цунами. 16 баллов.
Учащиеся берут любую карточку, на карточке выставлено высшее количество баллов.
Нарисована туфелька – подписать рисунок.
Ответить па вопросы.
1. Основная роль простейших в природе заключается в том, что они являются:
а) Основным кормом для рыб.
б) Входят в цепи питания.
в) Образуют и выделяют кислород.
2. Туфелька передвигается, потому что у неё есть:
а) Реснички.
б) Жгутики.
в) Ложноножки.
3. Пища у туфельки переваривается в:
а) сократительной вакуоли,
б) пищеварительной вакуоли,
в) ротовом отверстии.
4. Для удаления непереваренных остатков у туфельки есть:
а) ядро,
б) порошица,
в) реснички.
5. При неблагоприятных условиях у туфельки образуется:
а) циста,
б) спора,
в) стигма.
V. Рисунок эвглены – подписать.
VI. Заполнить таблицу.
| Органоиды | Амёба | Эвглена | Туфелька |
| 1. Оболочка 2. Ядро 3. Цитоплазма 4. Ложноножка 5. Жгутик 6. Реснички 7. Пищеварительная вакуоль 8. Сократительная вакуоль 9. Ротовое отверстие 10. Глотка 11. Порошица 12. Хлоропласт |
|
|
|
VII. Рисунок амёбы – подписать.
VIII. Дайте определения следующим понятиям.
1. Сократительная вакуоль.
2. Пищеварительная вакуоль.
3. Светочувствительный глазок.
Учитель: Дорогие путешественники, вы храбро преодолевали все препятствия. Если вы набрали более 50 баллов, то вы благополучно прибыли домой с оценкой “5”; Если набрали более 40 баллов – хорошо; если более 30 баллов – удовлетворительно. Но если меньше, то, увы, вы остались в море. Но не огорчайтесь, пройдя подготовку, вы сможете доплыть до берега.
В заключении – игра в светофор.
Зелёный цвет – Урок понравился.
Жёлтый цвет – Урок понравился, но…
Красный цвет – Урок не понравился, потому что…
Технологическая карта урока по биологии для 5-го класса на тему «Животные. Простейшие»
Цели урока:
- образовательные: создать условия для знакомства с особенностями строения, многообразием Простейших, их значением в природе и жизни человека; сравнивать, характеризовать их сходство и различия; делать выводы.
- развивающие: умение выделять и находить сходства в строении одноклеточных животных и растений; выдвигать предположения об их функциях.
- воспитательные: воспитывать бережное отношение к животному миру, формируя экологическую грамотность.
Место урока в разделе: Урок №1 в разделе «Животные».
Тип урока: Урок формирования новых знаний, комбинированный.
Основные термины и понятия: Простейшие, одноклеточные, амеба обыкновенная, инфузория- туфелька, малярийный плазмодий.
Межпредметные связи: Гигиена, физкультура, медицина,история.
Наглядность: таблица «Тип простейшие», презентация к уроку «Одноклеточные животные. Простейшие».
Формы работы на уроке: фронтальная работа со всем классом, работа в малых группах, индивидуальная работа.
Методы: проблемный, исследовательский через различные формы организации учебной деятельности (групповые, индивидуальные) на различных этапах урока, где ведущей является самостоятельная познавательная деятельность обучающихся, беседа, рассказ, работа с информационным источником, решение биологических задач.
Оборудование: пластилин зеленого, бурого, белого цветов; мультимедийное оборудование, дидактический раздаточный материал
Технологическая карта урока
ПриложениеМаршрутный лист №1Выясните общие признаки царства Растения. По мере выполнения заданий, делайте записи в тетради.
Определите преобладающий цвет простейшего. Выясните, почему некоторые простейшие являются автотрофами. Используйте текст учебника на стр. 53-54, 2 абзац и таблицу «Простейшие».
Маршрутный лист №2(1 группа)
1. Прочитайте текст об амёбе обыкновенной.
Амёба – свободноживущее микроскопическое животное. Ее можно обнаружить в небольших мелких прудах с илистым дном. Тело амёбы достигает в размерах 0,1–0,5 мм. Внутри клетки находится ядро и цитоплазма.
Форма тела амёбы постоянно меняется из-за образующихся в разных его участках лопастеобразных выпячиваний цитоплазмы, называемых псевдоподиями (ложноножками). Эти временные структуры служат для передвижения и захвата пищи.
Несмотря на примитивное строение, амёба вполне самостоятельный организм.
Амёба – всеядное животное. Ее пищу составляют водоросли, жгутиковые, инфузории. Как только амёба оказывается рядом с потенциальной добычей, ее цитоплазма образует несколько ложноножек, которые окружают жертву. Из цитоплазмы, окружающей добычу, выделяется пищеварительный сок.
Образуется пищеварительная вакуоль. После усвоения растворенной пищи, непереваренные остатки выбрасываются наружу.
2. Вылепите животное из пластилина заполните таблицу отметьте знаком «+» и «–» признаки простейшего.
Маршрутный лист №2(2 группа)
1. Прочитайте текст об эвглене зеленой.
Зеленая эвглена – необычное существо. Эвглена живет в пресноводных водоемах, богатых растворенными органическими соединениями. Тело эвглены вытянутое, длиной около 0,05 мм. Его передний конец притуплен, задний заострен. У эвглены нет клеточной стенки. Наружный слой цитоплазмы плотный, он образует вокруг тела эвглены оболочку. На переднем конце тела эвглены находится жгутик, при помощи которого она передвигается. В ее цитоплазме расположен светочувствительный глазок.
Питание эвглены. В цитоплазме эвглены содержится около 20 хлоропластов, придающих ей зеленый цвет. В хлоропластах находится хлорофилл. На свету эвглена питается, как растение, – при помощи процесса фотосинтеза. В темноте она усваивает готовые органические вещества, образующиеся при разложении различных отмерших организмов.
2. Вылепите животное из пластилина заполните таблицу отметьте знаком «+» и «–» признаки простейшего.
Маршрутный лист №2(3 группа)
1. Прочитайте текст об инфузории туфельки.
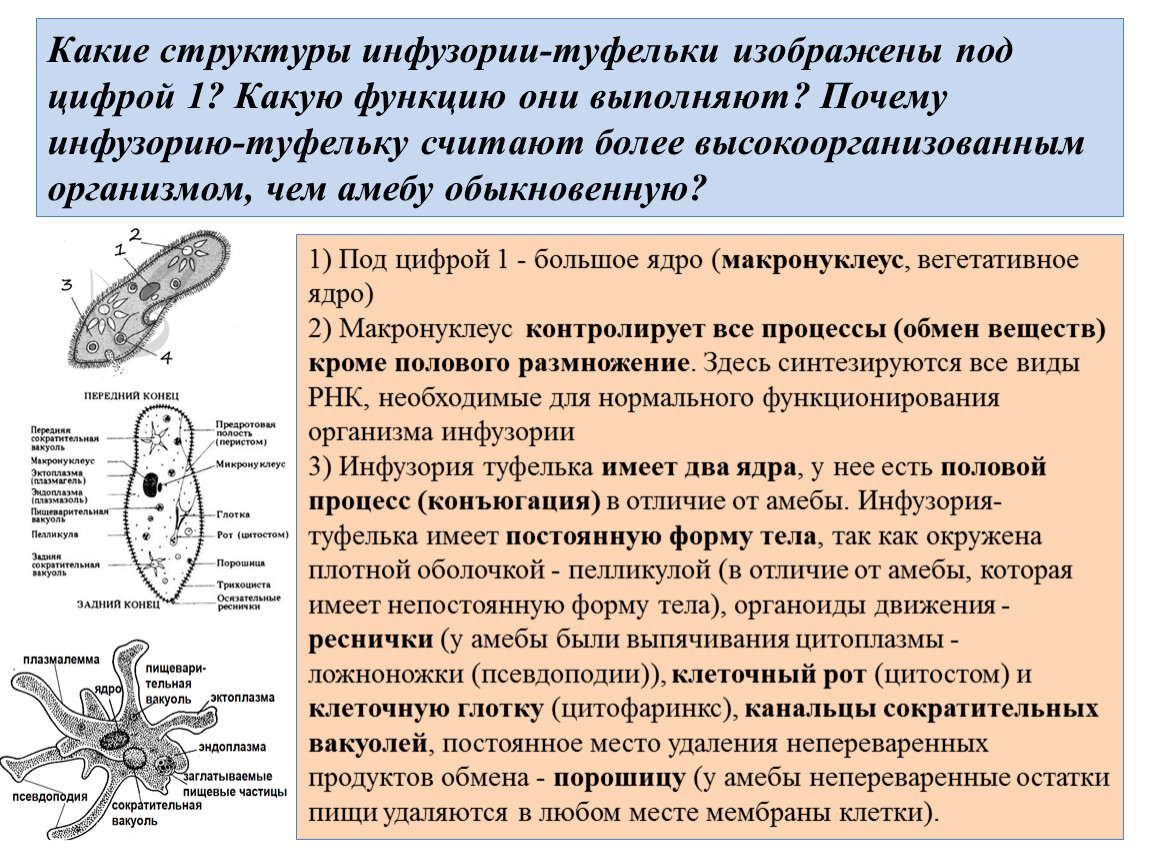
Инфузория туфелька – обитатель стоячих водоемов с большим количеством разлагающегося органического материала. Она имеет удлиненное тело длиной 0,1–0,3 мм, форма которого постоянна. Все тело инфузории покрыто продольными рядами многочисленных коротких ресничек, при помощи которых туфелька плавает тупым концом вперед.
Инфузория туфелька отличается от других простейших сложностью внутриклеточной организации. Ее цитоплазма содержит два ядра ( большое и маленькое).
Питание. Ближе к переднему концу тела инфузории находится постоянное углубление – ротовая воронка, которое ведет в глотку. Реснички желобка постоянно работают, создавая ток воды. Вода подхватывает и подносит ко рту основную пищу туфельки – бактерий. Через глотку бактерии попадают внутрь тела инфузории. В цитоплазме вокруг них образуется пищеварительная вакуоль. Переваривание пищи и усвоение питательных веществ у туфельки происходит так же, как и у амёбы. Непереваренные остатки выбрасываются наружу через отверстие – порошицу.
2. Вылепите животное из пластилина заполните таблицу отметьте знаком «+» и «–» признаки простейшего.
Таблица «Сходство и различие простейших» (у каждого на парте).
№ п/п | Органоиды | Простейшие | ||
Амеба обыкновенная | Эвглена зеленая | Инфузория туфелька | ||
1 | Оболочка | + | + | + |
2 | Цитоплазма | + | + | + |
3 | Ядро | + | + | + |
4 | Ложноножка | + | — | — |
5 | Жгутик | — | + | — |
6 | Ресничка | — | — | + |
7 | Пищеварительная вакуоль | + | — | + |
8 | Сократительная вакуоль | + | + | + |
9 | Ротовое отверстие | — | — | + |
10 | Порошица | — | — | + |
11 | Хлоропласты | — | + | — |
12 | Светочувствительный глазок | — | + | — |
Урок 9. Внутреннее строение и жизнедеятельность простейших | Поурочные планы по биологии 6-7 класс
Урок 9. Внутреннее строение и жизнедеятельность простейших
05.01.2015 4011 834Цели урока: закрепление знаний о жизненных свойствах организмов, выявление характерных черт строения и процессов жизнедеятельности простейших; формирование умений работать с учебными таблицами.
Оборудование: таблица «Тип Простейшие».
Ход урока
I. Организационный момент
II. Актуализация опорных знаний
1. Оказывается, не все простейшие способны активно двигаться, есть и те, которые ведут прикрепленный образ жизни. Кто они? Как тогда они добывают себе пищу, как защищаются? Слушаем сообщение «Инфузории-сувойки», Обращаем внимание на сидячий образ жизни, способы добычи пищи и защиты от врагов.
Инфузории-сувойки питаются бактериями, попадающими к ним в организм вместе с потоком воды. А как питаются другие представители одноклеточных животных и многое другое из их жизни мы узнаем сегодня на уроке.
2. Опрос по цепочке.
Прием «логическая цепочка» (отвечает 1 ученик) или «опрос по цепочке» (в построении развернутого, логически связного ответа участвует группа учащихся, — при этом рассказ одного ученика прерывается в любом месте и передается другому ученику жестом учителя).
О Составьте развернутый, логически связный ответ с использованием терминов прошлого урока: одноклеточные, простейшие, вода, жгутик, реснички, ложноножки, раздражитель, раздражимость.
Таким образом учащиеся проговаривают главные мысли прошлого урока. Подводятся итоги.
3. Индивидуальная работа по карточкам
Объясните термины: ‘
одноклеточные животные, простейшие, ложноножка, жгутик, реснички, раздражитель, раздражимость.
В каких средах жизни можно встретить простейших?
III. Изучение новой темы
Простейшими называют организмы, тело которых состоит из одной- единственной клетки с формированным ядром (эукариотической). Размеры — обычные для эукариотических клеток, — примерно 0,02-0,2 мм, но «в их лице» мы встречаемся с самой сложной организацией, известной для биологических клеток вообще. Ведь каждый одноклеточный организм — самостоятельный, и в его клетке-теле происходят такие процессы, которые у многоклеточных осуществляются лишь на уровне тканей и органов.
Функции любой клетки, органа, организма зависят от особенности их строения. Поэтому наша первая задача: по рисункам, таблице и тексту учебника рассмотреть особенности строения одноклеточных организмов. Для оформления результатов деятельности используем таблицу (Организуется самостоятельная работа по изучению нового материала по § 9).
Записываем тему урока и оформляем таблицу в тетради.
О Заполните таблицу, проставив знаки «плюс» (наличие) или «минус» (отсутствие) в каждой из трех колонок. Сделайте выводы по результатам вашей работы.
Структура | Амеба | Эвглена зеленая | Инфузория-туфелька |
Оболочка | + | + | + |
Цитоплазма | + | + | + |
Ядро | + | + | + (2) |
Ложноножки | + | _ |
|
Жгутик | _ | + | _ |
Реснички | _ | _ | + |
Пищеварительная вакуоль | + | _ | + |
Сократительная вакуоль | + | + | + |
Ротовое отверстие | _ | _ | + |
Порошица | _ |
| + |
Хлоропласты | _ | + | _ |
Светочувтвительный глазок | — | + | — |
После заполнения таблицы заслушиваются выводы, сформулированные учащимися.
Важно отметить следующее:
jsS Амеба, эвглена зеленая и инфузория-туфелька — одноклеточные организмы. Клетки имеют общий план строения: оболочка, цитоплазма, ядро.
jsS Для процессов питания и выделения продуктов жизнедеятельности используются временные органеллы — пищеварительные и сократительные вакуоли, а инфузорией еще и порошица.
& Органоиды движения — ложноножки, жгутики, реснички способствуют перемещению животных в их среде обитания.
& Различия в составах клеток тесно связаны с особенностями их процессов жизнедеятельности.
О Составьте рассказы о строении амебы, эвглены и инфузории-туфельки с использованием таблицы «Тип Простейшие», отмечая участие структур клетки в жизненных процессах. (Работу проводим в группах. Обязательное условие: использование таблицы во время рассказа).
Полный текст материала смотрите в скачиваемом файле.
На странице приведен только фрагмент материала.
Бактерия |
|
Вакуоль |
|
пищеварительная вакуоль [KL1] |
|
сократительная вакуоль |
|
Выделять- что? куда? |
|
Выделить-с помощью чего? |
|
Выделение |
|
Двигаться -как? c помощью чего? |
|
Движение |
|
Диссимиляция |
|
Дышать-как? чем? |
|
Он , она дышит, они дышат |
|
Дыхание |
|
Жидкий продукт |
|
Захватывать-что ? с помощью чего? |
|
Инцистироваться |
|
/рисовать/ |
|
Класс |
|
Неблагоприятные условия |
|
Образовать- вокруг чего? что? |
|
Переваривать |
|
Перевариваться-где? |
|
Питаться -как? чем? |
|
/читать/ |
|
Питание +р. п. |
|
Пища |
|
Поверхность |
|
Представитель |
. |
Пресная вода |
|
Простейшее животное |
|
Псевдоподия |
|
Размножаться -как? -чем? |
|
Размножение +р.п. |
|
Cаркодовые животные |
|
Тип |
|
Условия |
|
плохие условия |
|
Циста |
|
Тип Простейшие. Класс Жгутиковые.Эвглена |
|
Глазок |
|
Глотка |
|
Жгутик |
|
Зеленый /ая, ое, ые/ |
|
Зеленая эвглена |
|
Клеточный рот |
|
Поглощать что? /читать/ |
|
Попадать куда? во что? |
|
Продольное деление |
|
Резервуар |
|
Свет |
|
на свету |
|
Содержаться где? |
|
он, она, содержится, |
|
они содержаться |
|
Способ |
|
способ питания |
|
Стигма/глазок/ |
|
Фотосинтез |
|
Хлорофилл |
|
Тип Простейшие. Класс Ресничные.Парамеция. |
|
Вверх |
|
Вниз |
|
Глотка |
|
Дно |
|
на дне |
|
Инфузория |
|
Макронуклеус |
|
Микронуклеус |
|
Поперечный /ая, ое,ые/ |
|
Ресничные животные |
|
Рот |
|
Твердый/ая, ое, ые/ |
|
твердые продукты |
|
Функция |
|
Паразитические представители простейших |
|
Антилопа |
|
Болеть-чем? |
|
он, она болеет, они болеют |
|
Возбудитель- чего? |
|
Грызун |
|
Дизентерия |
|
Еж |
|
Использовать -кого? |
|
/читать/ |
|
Кишечник |
|
Класс Споровики |
|
Кожа |
|
Кольцевая форма |
|
Кровь /ж. р./ |
|
Лейшманиоз |
|
Личинка |
|
Малярийный комар |
|
Могут вызывать |
|
Муха це-це |
|
Относится к чему? |
|
/говорить/ |
|
Паразит |
|
Переносить -что? |
|
Песчанка |
|
Плазмодий |
|
Разрушать -что? |
|
Селезенка |
|
Соблюдать правила личной гигиены |
|
Сонная болезнь |
|
Спинномозговая жидкость |
|
Среда обитания |
|
Стенка |
|
стенка толстой кишки |
|
Суслик |
|
Трипаносома |
|
Уничтожать что? |
|
/читать/ |
|
Чувствовать себя как? |
|
Тип Кишечнополостные.Класс Гидройдные.Гидра. |
|
Водоем |
|
Волосок /чувствительный/ |
|
Выполнять что? |
|
функцию нападения |
|
функцию защиты |
|
Гермафродит |
|
Гидройдные животные |
|
Диффузный /ая,ое,ые/ |
|
Зигота |
|
Капсула |
|
Кишечнополостные животные |
|
Клетка |
|
железистая клетка |
|
интерстициальная клетка |
|
нервная клетка |
|
половая клетка |
|
стрекательная клетка |
|
эпителиальномускульная клетка |
|
Кусок |
|
Кусочек пищи |
|
Мезоглея |
|
Оплодотворение |
|
перекрестное оплодотворение |
|
Отделятся- от чего? |
|
Отросток /вырост/ |
|
Передавать-что? |
|
Подошва |
|
Полость |
|
Почка |
|
Почкование |
|
Расти /идти/ |
|
Слой |
|
Соединение |
|
Сперматозоид |
|
Способ питания |
|
внутриклеточный способ питания |
|
внутриполостный способ питания |
|
Способ размножения |
|
половой способ размножения |
|
бесполый способ размноже- ния |
|
Ферменты |
|
Щупальца |
|
Эктодерма |
|
Энтодерма |
|
Яйцеклетка |
|
Тип Кольчатые черви.Класс Малощетинковые черви.Дождевой червь. |
|
Анус |
|
Бок |
|
левый бок |
|
правый бок |
|
Брюшко |
|
Воронка |
|
Вперед/назад |
|
Всасывать -что? |
|
Всасываться -где? |
|
Ганглий /узел/ |
|
Дождевой червь |
|
Желудок |
|
Замкнутый/ая,ое.ые/ |
|
Зоб |
|
Кишка |
|
задняя кишка |
|
средняя кишка |
|
Кольцо |
|
окологлоточное кольцо |
|
Кольцевой сосуд |
|
Кольчатый червь |
|
Комиссуры |
|
Конец |
|
головной конец |
|
хвостовой конец |
|
Малощетинковые черви |
|
Мышцы |
|
кольцевые мышцы |
|
продольные мышцы |
|
Отверстие -где? |
|
Открываться-где? |
|
Пищевод |
|
Сердце |
|
Система |
|
выделительная система |
|
кровеносная система |
|
пищеварительная система |
|
Сокращаться |
|
Сосуд |
|
брющной сосуд |
|
спинной сосуд |
|
Спина |
|
Срез |
|
поперечный срез |
|
продольный срез |
|
Течь |
|
он,она течет |
|
они текут |
|
Трубочка |
|
Узел /ганглий/ |
|
надглоточный узел |
|
подглоточный узел |
|
Участвовать- в чем? |
|
Цепочка |
|
Щетинка |
|
Эпителий |
|
Тип Членистоногие. Класс Насекомые. |
|
Аорта |
|
Бабочка |
|
Включать-что? |
|
Внешний |
|
Внутренний |
|
Глаз |
|
Голова |
|
Грудь/ж.р./ |
|
Двусторонняя симметрия |
|
Дыхальце |
|
Жабры |
|
Жевательный желудок |
|
Измельчаться |
|
/читать/ |
|
Имаго |
|
Камера |
|
Крупный/ большой/ |
|
Кузнечик |
|
Куколка |
|
Легкое |
|
Личинка |
|
Линять |
|
Мальпигиевы сосуды |
|
Метаморфоз |
|
Многоножки |
|
Незамкнутая/ая,ое,ые/ |
|
незамкнутая кровеносная система |
|
Обитать-где? |
|
Пара |
|
Паукообразные |
|
Покрывать -что? чем? |
|
/читать/ |
|
Покрыт /а,о/ -чем? |
|
Полость /ж. р./ |
|
Похож/а,е,и/ |
|
Проходить |
|
Развиваться-из чего? |
|
Раздельнополые животные |
|
Ракообразные животные |
|
Самец |
|
Самка |
|
Стадия |
|
Усик |
|
Хитин |
|
Хитиновый /ая,ое,ые/ |
|
Челюсть нижняя |
|
Челюсть верхняя |
|
Членистоногие животные |
|
Яйцо |
|
Яичник |
|
План-конспект урока амеба обыкновенная (тема урока)
ПЛАН-КОНСПЕКТ УРОКА
_________
Амеба обыкновенная____________
(Тема урока)
ФИО (полностью) | Герасимова Нина Кузьмовна | |
Место работы | Муниципальное бюджетное общеобразовательное учреждение «Средняя общеобразовательная школа №10» г. Чайковский Пермского края | |
Должность | Учитель | |
Предмет | Биология | |
Класс | 7 | |
Тема и номер урока в теме | 7 | |
Базовый учебник | Константинов В. М., Бабенко В.Г., Кучменко В.С. Биология: Животные: Учебник для 7 класса общеобразовательных учреждений/ Под ред. В.М.Константинова, И.Н.Пономаревой. – М.: Вентана – Граф, 2004. |
8. Цель урока: формирование знаний учащихся об особенностях строения и жизнедеятельности амебы обыкновенной как целостного одноклеточного организма, ведущего самостоятельный образ жизни.
Задачи
— обучающие: ознакомить учащихся с особенностями строения, жизнедеятельности одноклеточных, как целостных одноклеточных организмов, ведущих самостоятельный образ жизни на примере амебы обыкновенной;
-развивающие: развивать у учащихся умение работать с текстом и рисунками,
умения учащихся работать с ЭОР, находить ответы на вопросы; развивать
интеллектуальные качества: внимание, память, наблюдательность; формировать
навыки самостоятельной
работы.
-воспитательные: воспитывать познавательный
интерес к животному миру.
Тип урока: введение нового материала с использованием ЭОР и самостоятельной деятельности учащихся.
Формы работы учащихся: фронтальная, парная, индивидуальная работа на ПК
Необходимое техническое оборудование:
— компьютер, экран, проектор, раздаточный материал (задания для работы в парах), учебник, таблицы по зоологии, фрагменты модулей из единой коллекции ЭОР, ПК
Структура и ход урока
Таблица 1.
СТРУКТУРА И ХОД УРОКА
№ | Этап урока | Название используемых ЭОР (с указанием порядкового номера из Таблицы 2) | Деятельность учителя (с указанием действий с ЭОР, например, демонстрация) | Деятельность ученика | Время (в мин.) |
1 | 2 | 3 | 5 | 6 | 7 |
1 | Организационный момент | Приветствие учащихся, проверка предварительной организации класса, психологический настрой учащихся на совместную деятельность. | Приветствие. Готовность к деятельности на уроке | 0,5 мин | |
2 | Введение нового материала. А. История открытия одноклеточных организмов. | Организация учащихся на активное слушание. (Приложение 1) Сценка — сообщение об открытии и изучении простейших животных совместно с учеником. | Воспринимают информацию, сообщаемую учителем и учеником. | 3 мин | |
Б. Классификация простейших | Рассказ учителя с записью схемы на доске. (Приложение 2) | Зарисовка схемы классификации одноклеточных животных в тетради | 3 мин | ||
В. Среда обитания, передвижение и внешний вид амебы | №1. Просмотр видеофрагмента «Амеба» | Задает вопросы учащимся: — Где обитает амеба обыкновенная? — Какова форма ее тела? — Как передвигается амеба? — Что такое ложноножки? — Почему амебу обыкновенную называют амебой протеем? | Работа учащихся с текстом учебника, ответы на вопросы учителя. | 3 мин | |
Г. Строение амебы. | Формулировка учителем заданий для выполнения самостоятельной работы. Фронтальная работа по демонстрационной таблице. — На какой органоид указывает указка? | Самостоятельная работа учащихся с рисунком учебника «Внешнее строение амебы». Ответы на вопросы учителя. | 3 мин | ||
Д. Питание амебы. | №2. Просмотр видеофрагмента «Питание амебы и пищеварительной вакуоли» | Задает вопрос учащимся: Как вы думаете, чем и как питаются амебы? Формулировка учителем заданий для выполнения самостоятельной работы. | Самостоятельное выполнение задания по карточке. Установить правильную последовательность питания амебы. (Приложение 3) | 4 мин | |
Е. Выделение у амебы | №3. Просмотр видеофрагмента «Выделение избытков жидкости». | Формулировка учителем заданий для выполнения самостоятельной работы. | Самостоятельное выполнение задания по карточке. Выбери правильные утверждения. (Приложение 4) | 4 мин | |
Ж. Дыхание амебы | Задает вопросы учащимся: — Что поглощают организмы в процессе дыхания? — Где амеба берет кислород? – А какой газ выделяется в процессе дыхания? — Как кислород и углекислый газ проникают в тело амебы? | Самостоятельная работа учащихся с текстом учебника. Отвечают на вопросы учителя. | 3 мин | ||
И. Размножение амебы. | №4. Просмотр демонстрации «Бесполое размножение амебы». | Формулировка учителем заданий для выполнения самостоятельной работы. | Самостоятельное выполнение задания по карточке. Вставь пропущенное слово в предложение. (Приложение 5) . | 3 мин | |
3 | Формулировка учителем заданий для выполнения учащимися | Определение практического модуля ЭОР, комментарии по выполнению. | Знакомятся с заданиями, задают вопросы по их условиям. | 2 мин | |
4 | Выполнение учащимися практического задания | №5. Практический модуль «Амеба – представитель пресноводных саркодовых». | Учитель проверяет результаты выполнения практических заданий, анализирует ответы, оценивает деятельность учащихся. | Выполняют задание. Самостоятельная работа с ЭОР. | 15 мин |
5 | Формулирование выводов урока | Формулирует выводы, организует процесс рефлексии. | Фиксируют выводы, рефлексируют. | 2 мин | |
6 | V. Домашнее задание. параграф №9 Подготовить сообщения о представителях «Класса Саркодовые», желательно с компьютерной презентацией. | Организует запись домашнего задания в дневниках, предлагает сделать выбор сообщений на следующий урок. | Записывают домашнее задание, выбирают сообщения. | 0.5 мин |
Приложения к плану-конспекту урока
________Обыкновенная амеба.______
(Тема урока)
Таблица 2.
ПЕРЕЧЕНЬ ИСПОЛЬЗУЕМЫХ НА ДАННОМ УРОКЕ ЭОР
№ | Название ресурса | Тип, вид ресурса | Форма предъявления информации (иллюстрация, презентация, видеофрагменты, тест, модель и т.д.) | Гиперссылка на ресурс, обеспечивающий доступ к ЭОР |
1 | Амеба | информационный | видеофрагмент | /catalog/res/7b16e564-0a01-022a-01de-437651012d02/?from=79f17baa-95ce-4223-85b1-1673e0f21e25&interface=pupil&class=49&subject=29 |
2 | Питание амебы образование пищеварительной вакуоли | информационный | анимация | /catalog/res/f2b6ff8d-09a3-4273-9025-53d3f5b7a727/?from=79f17baa-95ce-4223-85b1-1673e0f21e25&interface=pupil&class=49 |
3 | Выделение избытков жидкости. | информационный | анимация | /catalog/res/000003ae-1000-4ddd-551d-190046bb2fe0/?from=000001a1-a000-4ddd-7bd7-0a0046b1da3f&interface=pupil&class=49&subject=29 |
4 | Бесполое размножение амебы | информационный | демонстрация | http://school—collection.edu.ru/catalog/rubr/79f17baa-95ce-4223-85b1-1673e0f21e25/79010/?interface=pupil&class=49& |
5 | Амеба – представитель пресноводных саркодовых | практический | Практические задания. | /card/9857/ameba-predstavitel-presnovodnyh-sarkodovyh.html |
Приложение 1
Сценка.
Учитель: Открытие и изучение простейших животных
было тесно связано с изобретением и
усовершенствованием микроскопа.
Существование этих организмов было
установлено в 70-е годы 17 века голландцем
Антони Ван Левенгуком.
В семье
голландского ремесленника в 1632 году
родился мальчик, который получил имя
Антони. В юношеские годы Левенгука
привлекал мир прозрачных стеклянных
шариков, в которых предметы получали
странные формы. Все свободные минуты
Левенгук посвящал шлифовке линз. Со
временем он достиг в этой области
необыкновенного совершенства. Через
ошлифованные линзы он рассматривал
капельки речной воды, бродящего вина,
мелких насекомых, растения.
Ученик: Я изготовил больше 200 линз,
приспособленных для разных целей,
добился увеличения в 270 раз. Так начался
мой путь к научной славе.
Учитель: По сути дела, Левенгук не был ученым, не
имел образования, не знал латыни – свою
работу он основывал только на личном
опыте. Левенгук отличался богатой
фантазией и усидчивостью, что помогало
ему в изучении явлений. Кроме того, он
был необыкновенно изобретательным и
ловким, что позволило ему совершить
великие открытия.
Ученик: Вас интересует, что я увидел в микроскопе?
Удивительная картина открылась передо
мной. В капельке воды, взятой из бочки,
плавало бесчисленное множество живых
существ всевозможных форм. Что это за
существа и как назвать их, я не знал. Они
были невероятно малы, и поэтому я дал
им название «анималькули», что значит
«маленькие животные», «зверюшки».
Учитель: Через полгода, желая узнать, от чего
зависит жгучий вкус перца, Левенгук
попытался отделить мельчайшую частицу.
Когда ему это не удалось, он решил
предварительно размочить перец и залил
его водой.
Ученик: Несколько дней спустя, посмотрев через
линзу на каплю перечного настоя, я увидел
там невероятное количество «маленьких
животных». Одни имели вид удивительных
маленьких звездочек, другие –
треугольников, полумесяцев, третьи
напоминали колокольчики, сидящие на
длинных ножках, четвертые постоянно
меняли свою форму, как крошечные капли
масла, переливающиеся то в ту, то в другую
сторону. Да разве опишешь все то, что я
увидел в одной только капле перечного
настоя! Важно другое, ведь теперь я
открыл способ разводить «маленьких
животных».
Учитель: Оказалось, что их можно разводить не
только в настое из перца, но и в настоях
из травы, сена и различных семян. Теперь-то
Левенгук уже знал, какое «ученое» имя
можно присвоить этим животным.
Ученик: Они разводятся в настоях трав, и я назвал
их «инфузории», то есть «настойные»,
«наливочные» — от латинского слова
«инфузум», что значит «настой», «наливка».
Учитель: Тогда он называл этим названием все
организмы, обитающие в настое.
Приложение 2.
Простейшие
Царство животные | |||
Подтип Одноклеточные или Простейшие | |||
Тип Сарокожгутиконосцы | Тип Инфузории | Тип Споровики | |
Класс Саркодовые | Класс Жгутиконосцы | ||
Амеба протей | Эвглена зеленая | Инфузория — туфелька | Малярийный плазмодий |
Приложение 3
Установить правильную последовательность питания амебы.
А. Образование пищеварительной вакуоли.
Б. Непереваренное содержимое пищеварительной вакуоли выбрасывается наружу.
В. Захват добычи ложноножками
Г. Переваривание пищи.
Д. Пищеварительная вакуоль подходит к поверхности тела амебы.
Ответы: В А Г Д Б
Приложение 4
Выбери правильные утверждения.
А. Избыток воды из тела амебы выводится с помощью сократительной вакуоли.
Б. Сократительная вакуоль необходима амебе для удаления непереваренной пищи.
В. Вода из окружающей среды постоянно поступает внутрь тела амебы.
Г. Сократительные вакуоли отсутствуют у паразитических и морских простейших.
Д. В цитоплазме амебы имеются несколько сократительных вакуолей.
Ответы: А В Г
Приложение 5
Вставь пропущенное слово в предложение.
1.За сутки деление амебы происходит … раз.
2.В неблагоприятных условиях амеба образует …
3. В состоянии цисты амеба может переживать…
4. Циста служит для перенесения неблагоприятных условий и для … амебы.
5. Амеба размножается … путем.
Ответы: 1 – один, 2 – цисту, 3 – неблагоприятные условия, 4 – дизентерийной,
5 – бесполым.
(PDF) Amoebas Lobose
два рода принадлежат к этому семейству. Дифференцированные уроидные структуры
обычно отсутствуют, но у некоторых видов могут присутствовать луковичные, складчатые или морщинистые
уроиды. Обычно единичное ядро
везикулярно у большинства видов, но у некоторых
ядрышковый материал диспергирован на несколько периферических фрагментов
или имеет более сложную структуру, в то время как ядра
Pseudothecamoeba и Thecochaos близки к
. зернистый тип.Амебы рода Thecochaos мульти-
ядросодержащие, но этот род известен только по окрашенным препаратам
E. Penard. Амебы рода Sappinia
имеют пару близко расположенных ядер, напоминающих карион дипло-
. Для Sappinia diploidea описано бинарное слияние клеток во время инцистирования
, но детали этого процесса как
, а также наличие мейоза никогда не документировались. Тем не менее, широко распространено мнение, что это единственная половая амеба
.Клеточная оболочка различается между родами; он может быть
аморфным (Thecamoeba, Parvamoeba и Stenamoeba),
или иметь сверхструктурированный слой (Sappinia), толстую «кутикулу»
(Dermamoeba) или очень толстый слой плотно упакованного гели-
кал. glycostyles (Paradermamoeba), а может быть нитчатым
(Pseudothecamoeba). Последний род также уникален в
с сильно вакуолизированной цитоплазмой, удивительно напоминающей структурные вакуоли Pelomyxa palustris.Группа
включает пресноводные, почвенные и морские организмы,
, некоторые из которых образуют цисты.
Семейство Vannellidae: это амебы с веерообразным морфотипом
, иногда полукруглым, серповидным
или лопатообразным, при передвижении (5 родов, 41 действительный
вида; Рисунок 7 (l) -7 (n) )). У большинства видов имеется одно везикулярное ядро
и несколько с ядрышками, которые расположены на периферии
. Никаких дифференцированных структур уоида не известно.
Гликокаликс состоит из аморфного слоя, за которым следует слой
либо плотно упакованных гексагональных призматических структур
, либо пятиугольных гликостилей. До недавнего времени считалось, что род Vanella
отличается наличием пентагональных гликостилей
, а род Platyamoeba
— наличием призматических структур в клеточной оболочке. Как бы то ни было, молекулярная филогения четко указывает на то, что структура оболочки клетки
не может использоваться для различения родов в этом случае
, и все представители рода Platyamoeba были перенесены
недавно в род Vannella.Это пресноводные,
,почвенные и морские организмы, некоторые из которых образуют цисты.
Семейство Paramoebidae: это довольно разнообразное семейство из
амеб с дактилоподиальным или майореллическим морфотипом
(3 рода, 17 допустимых видов; Рисунок 7 (o) –7 (q)). Данные Molecular
снова указывают на то, что таксон является полифилетическим. Амебы
этого семейства образуют субпсевдоподии, которые представляют собой дактилопо-
диам (Paramoeba и Korotnevella) или короткие конические псевдо-
подии, которые иногда сопровождаются дактилоподиями
(Mayorella).Большинство из них не имеет дифференцированных уроидных структур,
, хотя майореллы могут образовывать складчатую или выпуклую
уроид и временные продольные дорсальные складки. Имеется единичное везикулярное ядро
, а клеточная оболочка представляет собой многослойную «кутикулу»
у Mayorella и имеет чешуйки у Korotnevella и
Paramoeba. Амебы последнего рода содержат одну
или несколько парасом, специфическую ДНК-содержащую самовоспроизводящуюся органеллу
, которая, вероятно, является остатком
очень древнего кинетопластидного симбионта.Группа состоит из
пресноводных, почвенных и морских организмов, ни один из которых, как известно, не образует цисты.
Семейство Vexilliferidae: вероятно, это еще одна филетическая коллекция поли-
, разделенная на молекулярные деревья (3 рода,
15 допустимых видов; рис. 7 (r) и 7 (s)). Эти амебы имеют
дактилоподиальных и фламеллиевых морфотипов, а локомо-
тивные амебы образуют (1) длинные дактилоподийоподобные выступы
, направленные вперед (Vexillifera), (2) короткие дактилоподии (
) () Neoparamopodia короткие конические псевдоподии(Pseudoparamoeba).Выпуклый уроид можно найти у видов Neoparamoeba. Имеется одно везикулярное ядро,
, а амебы рода Neoparamoeba могут содержать одно
или несколько парасомов. Оболочка клеток является аморфной или имеет
гликостилоподобных структур (Neoparamoeba) и может состоять из короткопризматических гексагональных структур (Vexillifera)
или гексагональных пузырчатых структур (Pseudoparamoeba).
Это группа пресноводных, почвенных и морских организмов,
, ни один из которых, как известно, не образует цисты.
Семейство Pellitidae: это амебы морфотипа Flamellian
, в которых отсутствуют субпсевдоподии (один род, два действительных вида
; Рисунок 8 (a)). Имеется единичное везикулярное ядро и
без дифференцированных уроидальных структур. Ячеистая оболочка имеет очень
толщину(до 800 нм) и состоит из
гликостилей, похожих на тюльпаны. Для передвижения эти амебы образуют
коротких вентральных гиалиновых выступов, которые проходят через оболочку клетки
; во время фагоцитоза амеба захватывает добычу, высвобождая часть клеточной мембраны, «отталкивая» гликоз-
тайлов.Это может быть адаптацией к наличию очень толстого слоя гликостилей
, который не может опосредовать клеточную адгезию
или внедряться в пищевые вакуоли вместе с пищевым объектом
. В группу входят пресноводные и морские организмы —
измов, цисты неизвестны.
Семейство Acanthamoebidae: это семейство включает в себя число хорошо известных патогенов животных и человека
, а также молекулярный модельный организм Acanthamoeba cas-
tellanii (2 рода, около 24 действительных морфоспецифических видов).Это
амеб с акантоподиальным морфотипом, что означает наличие
коротких, сужающихся, иногда с развилками subpseu-
доподий, называемых акантоподиями. Нет никаких различий —
энтифицированных уроидальных структур, и «центриольные тела»
(центры организации цитоплазматических микротрубочек (ЦТОЦ))
обнаруживаются около единственного везикулярного ядра. Клеточная оболочка
аморфная, все виды цистообразующие; кисты
двустенные с порами (Acanthamoeba) или более простые
с одинарными стенками (Protacanthamoeba).Известны виды
из пресноводных, почвенных и морских местообитаний.
Семейство Flabellulidae: эти амебы имеют морфотип flabellate
или фламеллиан (два рода, восемь допустимых видов;
Рисунок 8 (b)). При быстром движении они могут стать временными, очень редко монотактическими. Обнаружены характерные адгезивные уроиды
ЧАСТЬ II Протисты202
Отношения между древними бактериями и амебами и патогенные бактерии животных
Abstract
Задолго до того, как бактерии заразили людей, они заразили амеб, которые остаются потенциально важным резервуаром болезней человека.Разнообразные почвенные амебы, включая Dictyostelium и Acanthamoeba , могут содержать внутриклеточные бактерии. Хотя внутренняя среда свободноживущих амеб во многом схожа с окружающей средой макрофагов млекопитающих, они различаются по ряду важных аспектов, включая температуру. Новое исследование в PLOS Biology , проведенное Taylor-Mulneix et al. демонстрирует, что Bordetella bronchiseptica имеет два разных набора генов, которые активируются в зависимости от того, находится ли бактерия в горячей среде хозяина млекопитающего или в прохладной среде хозяина амебы.В данном исследовании конкретно показано, что B . bronchiseptica не только населяет амебы, но и может сохраняться и размножаться на социальной стадии хозяина амебы, Dictyostelium discoideum .
Образец цитирования: Strassmann JE, Shu L (2017) Взаимоотношения древних бактерий и амеб и патогенные бактерии животных. PLoS Biol 15 (5): e2002460. https://doi.org/10.1371/journal.pbio.2002460
Опубликовано: 2 мая 2017 г.
Авторские права: © 2017 Strassmann, Shu.Это статья в открытом доступе, распространяемая в соответствии с условиями лицензии Creative Commons Attribution License, которая разрешает неограниченное использование, распространение и воспроизведение на любом носителе при условии указания автора и источника.
Финансирование: Авторы не получали специального финансирования на эту работу.
Конкурирующие интересы: Авторы заявили, что никаких конкурирующих интересов не существует.
Сокращения: LCV, Legionella — вакуоль, содержащая; NCBI, Национальный центр биотехнологической информации; T2SS, система секреции типа II; T4SS, система секреции типа IV
Происхождение: Введен в эксплуатацию; внешняя экспертная оценка.
Экологические амебы появились раньше животных в качестве носителей бактерий.
Больше всего нас беспокоят бактерии, вызывающие болезни, но иногда мы настолько озабочены своей борьбой с ними, что забываем, что они ведут гораздо более длительную войну. Более чем за миллиард (10 9 ) лет до появления первых животных бактерии разрабатывали стратегии, чтобы сначала сопротивляться гибели простейшими хищниками, а затем фактически заразить своих бывших хищников [1]. Эти стратегии, вероятно, заложили основу для более поздней эволюции взаимодействий животных и бактерий, поэтому понимание того, как они функционируют, обеспечивает важный контекст для понимания современных бактериальных патогенов у людей.Это особенно верно для бактерий, которые проникают в животных через макрофаги [2]. Кроме того, экологические амебы все еще широко распространены в современной почве и воде, поэтому они могут выступать в качестве важных резервуаров, из которых могут возникать новые болезни человека [3]. Многие амебы, в том числе Acanthamoeba castellanii , D . Было обнаружено, что discoideum , Hartmannella vermiformis и Naegleria gruberi содержат бактерии [4]. Бактерии, которые могут победить защиту амеб, получают убежище для размножения, где они защищены от враждебных внешних условий своими невольными хозяевами [5–8].
Стоит отметить, что амебы не попадают в монофилетическую группу, а имеют общую жизненную форму и диету, основанную на фагоцитозе. Бактерии, которые могут уклоняться от защиты амебы, называются устойчивыми к амебе [3,4]. В этих амебах устойчивые бактерии могут выживать, размножаться и быть защищенными в неблагоприятных ситуациях, особенно когда амеба-хозяин образует стойкую кисту с бактериями внутри.
Глоссарий
Устойчивые к амебам бактерии : Бактерии, которые эволюционировали, чтобы противостоять гибели свободноживущим амебам.
Бактериальная секреционная система : механизмы, с помощью которых бактериальные патогены эволюционировали, чтобы экспортировать различные факторы вирулентности через фосфолипидную мембрану и клеточную оболочку.
Эжектосома : периферическая клеточная органелла, ответственная за выброс цитозольных бактерий из клетки без лизиса этой клетки.
Плодовое тело : Многоклеточная структура, на которой расположены споровидные структуры.
Свободноживущие амебы : Широко распространенные простейшие, которые способны изменять свою форму и питаются бактериями, водорослями, грибами и мелкими органическими частицами.
Лизосома : мембраносвязанная органелла, содержащая гидролитические ферменты, способные разрушать биомолекулы.
Фагоцитоз : процесс, при котором клетка поглощает твердую частицу с образованием внутреннего компартмента, известного как фагосома.
Фагосома : вакуоль, образованная вокруг частицы, охваченной фагоцитозом.
Симбиоз : Отношения между особями разных видов, живущими вместе.
Двухкомпонентная регуляторная система : один из видов механизма передачи сигнала, который позволяет организмам ощущать изменяющуюся среду и реагировать на нее.
Спора : Единица полового или бесполого размножения, способная распространяться и выживать в неблагоприятных условиях.
Фактор вирулентности : молекулы, продуцируемые патогенами, которые могут повысить свою приспособленность при взаимодействии с хозяином.
Стратегии выживания внутриклеточных бактерий внутри амеб
Попадание бактерий в амебы происходит просто, потому что амебы поедают бактерии.Обычно амебы поглощают пищевые бактерии посредством фагоцитоза и убивают их внутри фагосомы, где проглоченные бактерии сталкиваются с подкислением, окислительным стрессом, недостатком питательных веществ и различными небольшими молекулами антимикробных препаратов [2] [9,10]. Считается, что выпас амебы является одной из основных факторов, определяющих численность и разнообразие бактерий [11]. Однако некоторые бактерии разработали стратегии, позволяющие выжить при фагоцитозе амеб, и могут использовать ресурсы клетки-хозяина. Бактерии, такие как Legionella pneumophila , которые остаются в вакуоли макрофагов у человека, возможно, являются наиболее изученными бактериями, инфицирующими людей и амеб, но они ни в коем случае не единственные (Таблица 1) [12,13].
Таблица 1. Список патогенов человека, обнаруженных у свободноживущих амеб.
Эти бактерии изолированы от разных хозяев амеб и ведут разный образ жизни [8,14–16]. Они разработали сложные способы экспорта различных факторов вирулентности через свою бактериальную внутреннюю и иногда внешнюю мембрану (у грамотрицательных бактерий), а также через плазматическую мембрану хозяина или фагосомную мембрану, используя различные системы секреции [17,18].
https: // doi.org / 10.1371 / journal.pbio.2002460.t001
Самая очевидная стратегия, позволяющая избежать гибели от хозяина амебы, — это вырваться из вакуоли в цитозоль амебы (рис. 1A). Например, M . маринум и M . tuberculosis развили эту способность (рис. 1A, желтый). Для этого процесса необходима система секреции микобактерий VII типа ESX-1 [12]. Кроме того, как M, . маринум и M . tuberculosis может выбрасываться из клетки через структуру F-актина, называемую эжектосомой, а затем распространяться от клетки к клетке [19,20].
Рис. 1. Схема стратегии выживания внутриклеточных бактерий внутри амеб.
На рисунке представлены две общие стратегии, которые внутриклеточные бактерии используют для выживания внутри амеб. Они могут ускользать из фагосомы (Рис. 1A) или оставаться в фагосомной вакуоли, но изменять ее (Рис. 1B). Зеленые внутриядерные бактерии; желтый — бактерии, которые попадают в цитозоль; синий, несет Burkholderia ; фиолетовый, B . bronchiseptica ; красный, L . пневмофила .
https://doi.org/10.1371/journal.pbio.2002460.g001
В целом цитозоль считается благоприятным для роста бактерий, поскольку он обеспечивает питательными веществами и изолирован от иммунной системы хозяина [21]. Следовательно, это идеальное место для размножения бактерий после побега из фагосомы. Некоторые внутриклеточные патогены могут вторгаться в более необычную внутриклеточную нишу: ядро эукариот (рис. 1А, зеленый). Об этом сообщалось у свободноживущих амеб — например, бактерия, называемая штаммом Pn в Chlamydiae, была обнаружена в ядрах N . clarki [22]. Бактерия, предварительно названная « Candidatus Nucleicultrix amoepiphila» и отдаленно родственная Rickettsiales , была обнаружена в ядрах Hartmannella sp. [23]. По-видимому, эти двое независимо друг от друга выработали внутриядерную привычку.
Вторая стратегия, которую используют бактерии, — оставаться в фагосомной вакуоли, но разрушать ее антимикробные механизмы (Рис. 1B). Эти методы подрывной деятельности включают предотвращение слияния фагосом и лизосом, модуляцию pH фагосом, повреждение фагосомных мембран и / или подавление окислительных всплесков [5].Внутриклеточные патогены используют комбинацию этих подходов. Например, L . Пневмофила (Рис. 1B, красный) развила сложную систему, которая позволяет бактериям захватить фагоцитарную вакуоль [24]. Он уклоняется от эндоцитарного пути и последующего слияния фагосома-лизосома, задерживает его закисление и создает безопасную внутриклеточную нишу, называемую Legionella -содержащей вакуоль (LCV), которая делает возможной внутриклеточную репликацию [24,25]. Дальнейшие исследования показывают, что L . pneumophila использует систему секреции Icm / Dot типа IV (T4SS) и систему секреции Lsp типа II (T2SS), чтобы избежать смерти и использовать ресурсы хозяина [24,26]. Другие бактерии используют аналогичные стратегии [12].
Хорошо изученная амеба D . discoideum добавляет еще одну морщину к истории взаимодействия амеб и бактерий. Эта социальная амеба из семейства Amoebozoa и других членов его семейства большую часть времени ведет себя так же, как и другие почвенные амебы, поедая бактерии и делясь путем бинарного деления.Но когда они перестают находить достаточное количество пищевых бактерий, амебы собираются десятками тысяч в многоклеточную слизь, которая движется навстречу теплу и свету [27]. В конечном итоге этот слизень образует плодовое тело, в котором около 20% клеток (ранее независимых амеб) погибают, образуя прочный стебель, а оставшиеся клетки образуют выносливые споры наверху стебля, куда они с большей вероятностью будут переноситься [27,28 ].
Бактерии могут использовать эту амебу [29,30]. Некоторые бактерии также могут оставаться внутри спор в течение социального цикла. Burkhoderia около грибов — одна из таких бактерий (рис. 1B). Фактически, этот и другие штаммы Burkholderia настолько изменяют фагосомный аппарат, что D . discoideum , инфицированные ими, также могут переносить пищевые бактерии, которые в противном случае переваривались бы (рис. 1B, синий) [31–34]. Эти клоны амебы называются фермерами, потому что они могут посевать и собирать урожай в новых условиях [34].
В целом, большинство внутриклеточных возбудителей амеб занимают фагосомные вакуоли, и лишь некоторые из них способны покинуть фагосому [5].Возможно, это связано с тем, что для выхода из фагосомы необходимы специальные механизмы [5,21]. Нет четкой взаимосвязи между типом стратегии выживания и тем, является ли микроб облигатным или факультативным внутриклеточным патогеном [5].
Взаимодействие между
B . bronchiseptica и амебыМы начали эту статью с того, что отметили, что амебы предшествовали животным на планете более чем на миллиард лет. Если бактерии начали свою инфекционную жизнь в почве и воде, то мы ожидаем, что эти линии будут более древними, чем линии от животных.Для B существует подробное и недавнее исследование по этой теме. bronchiseptica , которая является бактерией грамотрицательных бетапротеобактерий [35]. Он вызывает респираторные инфекции у некоторых видов млекопитающих и тесно связан с B . pertussis , который вызывает коклюш у людей, по данным Всемирной организации здравоохранения, в 2008 году на него во всем мире умерло около 89 000 человек.
Soumana et al. построили филогению штаммов Bordetella , собранных из источников окружающей среды и от животных [36].Для этого Soumana et al. провели поиск в базе данных Национального центра биотехнологической информации (NCBI) на предмет соответствия последовательности 16s рибосомной РНК нескольким видам Bordetella и связали то, что они обнаружили, с источниками последовательностей [36]. Древо соединения соседей, основанное на последовательностях 16S рРНК, показало, что изоляты из окружающей среды были базальными, как и предполагалось [36].
Это не единственная интересная особенность Bordetella . В большинстве исследований взаимодействия амеб с бактериями используются преимущества сходства между амебами и макрофагами, которые объясняются тем, что оба они обладают фагоцитарной активностью [12,24].Хотя использование амеб вместо животных в качестве экспериментальных хозяев для бактерий дает серьезные преимущества, амебы в окружающей среде обычно живут при гораздо более низких температурах (~ 21 ° C), чем макрофаги внутри человеческого тела (~ 37 ° C).
Б . bronchiseptica имеет двухкомпонентную систему передачи сигнала, называемую BvgAS, которая регулирует две отдельные фазы: вирулентную фазу Bvg + и авирулентную фазу Bvg- [37]. Эти системы по-разному работают при низких и высоких температурах [35].При более высокой температуре вирулентность у млекопитающего-хозяина регулируется Bvg +, который контролирует экспрессию более 100 генов [35]. При более низких температурах такой же большой набор генов активируется в состоянии Bvg-. Последние гены позволяют расти при более низких концентрациях питательных веществ и включают движение жгутиков [35]. Оказывается, состояние Bvg− — это то, что позволяет B . bronchiseptica для выживания внутри почвенных амеб, в том числе в лабораторных амебах D . discoideum [35].
Б . bronchiseptica оставался живым через час при добавлении к культуре D . discoideum с антибиотиком гентамицином. Напротив, B . bronchiseptica не смог выжить и час в отсутствие D . discoideum с тем же антибиотиком. Стандартная пищевая бактерия, указанная в D . discoideum (а именно, Klebsiella pneumoniae ) не присутствовал через час в любом случае, а B . bronchiseptica бактерий были защищены внутри амеб. Этот результат был подтвержден аналогичным экспериментом, допускающим B . bronchiseptica для вторжения в другой вид амеб, отдаленно родственный D . дискоидум , А . кастеллании .
Когда D . discoideum прошел социальную стадию, B . bronchiseptica появилось сразу же, хотя и вне спор, что сделало его уязвимым на этой стадии для антибиотиков (рис. 1B, фиолетовый).Не только B . bronchiseptica бактерий выживают в плодовых телах, но когда плодовые тела были разбавлены в 10 раз и переселены на новую лужайку с кормом, B . bronchiseptica пролиферировала вправо вместе с D . дискоидеум . Этот успех пролиферации и выживания у амеб обусловлен экспрессией системы Bvg-, что авторы продемонстрировали, показав, на сколько меньше клеток клона, заблокированного на стадии Bvg +, пролиферировало по сравнению с клоном дикого типа или клоном, заблокированным в Bvg. — этап [35].Авторы далее продемонстрировали, что после прохождения через споры D . дискоидум , B . bronchiseptica были способны инфицировать дыхательные пути мышей [35].
Bordetella — это древний род бактерий, который, вероятно, сначала напал на амеб из окружающей среды, но теперь также вызывает респираторные заболевания у млекопитающих; к этому роду относятся B . pertussis , который поражает только людей и не может выжить в окружающей среде [36].
Тем не менее, вопросы остаются. Это B . bronchiseptica обнаружен в диких штаммах D . discoideum или другие виды Dictyostelium ? Есть ли у других бактерий, вторгающихся как в амеб, так и у животных, разные наборы генов для адаптации к обоим? Кроме того, в будущем предстоит провести всесторонний обзор бактерий, обнаруженных в диких амебах. Возможно, наиболее поучительными будут дальнейшие открытия бактериальных последовательностей в секвенированных геномах амеб.
Выводы
Как прекрасно выразились Макфалл-Нгаи и соавторы, животные эволюционировали в мире, который уже содержал миллиарды бактерий, архей и амеб [38]. Таким образом, неудивительно, что некоторые бактериальные патогены человека и других млекопитающих произошли не только от предков, которые нападали на амеб, но и часто сохраняли эту способность в течение эволюционного времени. Эти новые и захватывающие результаты подробно рассказывают о том, как бактерия может использовать социальный цикл амебы и полностью изменить гены вирулентности, которые она развертывает, в зависимости от того, атакует ли она горячее млекопитающее или холодную амебу.Этот пример, вероятно, будет только первым из множества тщательных исследований, которые точно показывают, как бактерии справляются с этими уловками.
Благодарности
Мы благодарим Тайлера Ларсена и Дэвида Квеллера за чрезвычайно полезные комментарии.
Ссылки
- 1. Брюссоу Х (2007) Бактерии между простейшими и фагами: от стратегий борьбы с хищниками до эволюции патогенности. Молекулярная микробиология 65: 583–589. pmid: 17608793
- 2. Хаас А. (2007) Фагосома: отделение с лицензией на убийство.Трафик 8: 311–330. pmid: 17274798
- 3. Scheid P (2014) Актуальность свободноживущих амеб как хозяев для филогенетически разнообразных микроорганизмов. Паразитологические исследования 113: 2407–2414. pmid: 24828345
- 4. Denoncourt AM, Paquet VE, Charette SJ (2014) Потенциальная роль упаковки бактерий простейшими в сохранении и передаче патогенных бактерий. Границы микробиологии 5: 240. pmid: 243
- 5. Casadevall A (2008) Эволюция внутриклеточных патогенов.Анну Рев Микробиол 62: 19–33. pmid: 18785836
- 6. Guimaraes AJ, Gomes KX, Cortines JR, Peralta JM, Peralta RHS (2016) Acanthamoeba spp. как универсальный хозяин для патогенных микроорганизмов: один мост от вирулентности окружающей среды к хозяину. Микробиологические исследования 193: 30–38. pmid: 27825484
- 7. Hilbi H, Weber SS, Ragaz C, Nyfeler Y, Urwyler S (2007) Экологические хищники как модели бактериального патогенеза. Экологическая микробиология 9: 563–575. pmid: 17298357
- 8.Greub G, Raoult D (2004) Микроорганизмы, устойчивые к свободноживущим амебам. Обзоры клинической микробиологии 17: 413–433. pmid: 15084508
- 9. Cosson P, Lima WC (2014) Внутриклеточное уничтожение бактерий: Dictyostelium — это модельный макрофаг или инопланетянин? Клеточная микробиология 16: 816–823. pmid: 24628900
- 10. Герман Н., Дойшер Д., Ренсинг С. (2013) Убийство бактерий в макрофагах и амебах: все ли они используют латунный кинжал? Будущая микробиология 8: 1257–1264.pmid: 24059917
- 11. Matz C, Kjelleberg S (2005) С крючка — как бактерии выживают при выпасе простейших. Тенденции микробиологии 13: 302–307. pmid: 15935676
- 12. Steinert M. Взаимодействие патоген-хозяин у Dictyostelium, Legionella, Mycobacterium и других патогенов; 2011. Elsevier. С. 70–76.
- 13. Tosetti N, Croxatto A, Greub G (2014) Амебы как инструмент для выделения новых видов бактерий, обнаружения новых факторов вирулентности и изучения взаимодействий между хозяином и патогеном.Микробный патогенез 77: 125–130. pmid: 25088032
- 14. Tosetti N, Croxatto A, Greub G (2014) Амебы как инструмент для выделения новых видов бактерий, обнаружения новых факторов вирулентности и изучения взаимодействий между хозяином и патогеном. Микробный патогенез 77: 125–130. pmid: 25088032
- 15. Боззаро С., Эйхингер Л. (2011) Профессиональный фагоцит Dictyostelium discoideum как модельный хозяин для бактериальных патогенов. Current Drug Targets 12: 942–954. pmid: 21366522
- 16.Steinert M (2011) Взаимодействие патоген-хозяин у Dictyostelium, Legionella, Mycobacterium и других патогенов. Семинары по клеточной биологии и биологии развития 22: 70–76.
- 17. Green ER, Mecsas J (2016) Системы бактериальной секреции: обзор. Микробиологический спектр 4.
- 18. Коста TRD, Фелисберто-Родригес С., Меир А., Прево М.С., Редзей А. и др. (2015) Системы секреции у грамотрицательных бактерий: структурные и механистические взгляды. Nature Reviews Microbiology 13: 343–359.pmid: 25978706
- 19. Хагедорн М., Роде К.Х., Рассел Д.Г., Солдати Т. (2009) Инфекция туберкулезными микобактериями распространяется путем нелитического выброса от их хозяев-амеб. Наука 323: 1729–1733. pmid: 19325115
- 20. Герстенмайер Л., Пилла Р., Херрманн Л., Херрманн Х., Прадо М. и др. (2015) Аутофагический механизм обеспечивает нелитическую передачу микобактерий. Труды Национальной академии наук Соединенных Штатов Америки 112: E687 – E692. pmid: 25646440
- 21.Ray K, Marteyn B, Sansonetti PJ, Tang CM (2009) Жизнь внутри: внутриклеточный образ жизни цитозольных бактерий. Nature Reviews Microbiology 7: 333–340. pmid: 19369949
- 22. Шульц Ф., Хорн М. (2015) Внутриядерные бактерии: внутри клеточного центра управления эукариотами. Тенденции в клеточной биологии 25: 339–346. pmid: 25680230
- 23. Schulz F, Lagkouvardos I., Wascher F, Aistleitner K, Kostanjsek R, et al. (2014) Жизнь в необычной внутриклеточной нише: бактериальный симбионт, заражающий ядро амеб.Журнал ISME 8: 1634–1644. pmid: 24500618
- 24. Hoffmann C, Harrison CF, Hilbi H (2014) Естественная альтернатива: простейшие как клеточные модели инфекции Legionella. Клеточная микробиология 16: 15–26. pmid: 24168696
- 25. Escoll P, Rolando M, Gomez-Valero L, Buchrieser C (2013) От амебы до макрофагов: изучение молекулярных механизмов инфекции Legionella pneumophila у обоих хозяев. Curr Top Microbiol Immunol 376: 1–34. pmid: 23949285
- 26.Hubber A, Kubori T, Nagai H (2014) Модуляция механизма убиквитинации с помощью Legionella. Молекулярные механизмы в патогенезе легионелл 376: 227–247.
- 27. Кессин Р.Х. (2001) Dictyostelium: эволюция, клеточная биология и развитие многоклеточности. Кембридж, Великобритания: Издательство Кембриджского университета. 308 с.
- 28. Smith J, Queller DC, Strassmann JE (2014) Плодовые тела социальной амебы Dictyostelium discoideum увеличивают перенос спор дрозофилой.BMC эволюционная биология 14: 105. pmid: 24884856
- 29. Хагеле С., Колер Р., Меркерт Х., Шлейхер М., Хакер Дж. И др. (2000) Dictyostelium discoideum: новая модельная система хозяина для внутриклеточных патогенов рода Legionella. Cell Microbiol 2: 165–171. pmid: 11207573
- 30.
Bozzaro S, Bucci C, Steinert M (2008) Фагоцитоз и взаимодействия между хозяином и патогеном в Dictyostelium с учетом макрофагов. Международный обзор клеточной и молекулярной биологии 271: 253–300.pmid: 1
45 - 31. ДиСальво С., Хаселкорн Т.С., Башир Ю., Хименес Д., Брок Д.А. и др. (2015) Бактерии Burkholderia заразно вызывают симбиоз протоферм Dictyostelium amoebae и пищевых бактерий. Труды Национальной академии наук 112: E5029 – E5037.
- 32. Столлфорт П., Брок Д.А., Кэнтли А.М., Тиан Х, Квеллер Д.К. и др. (2013) Бактериальный симбионт превращается из несъедобного продуцента полезных молекул в пищу с помощью единственной мутации в гене gacA.Труды Национальной академии наук 110: 14528–14533.
- 33. Brock D, Read S, Bozchenko A, Queller DC, Strassmann JE (2013) Социальные фермеры, выращивающие амебы, носят бактериальное оружие, чтобы защитить и приватизировать свои посевы. Nature Communications 4: 2385. pmid: 24029835
- 34. Брок Д.А., Дуглас Т.Э., Квеллер Д.К., Штрассманн Дж.Э. (2011) Примитивное сельское хозяйство в социальной амебе. Природа 469: 393–396. pmid: 21248849
- 35. Тейлор-Мулникс Д.Л., Бендор Л., Линц Б., Ривера И., Райман В.Е., Деван К.К. и др. Bordetella bronchiseptica использует сложный жизненный цикл Dictyostelium discoideum как усиливающий вектор передачи. PLoS Biol. 2017; 15: e2000420. pmid: 28403138
- 36. Soumana IH, Linz B, Harvill ET (2017) Экологическое происхождение рода Bordetella. Границы микробиологии 8.
- 37. Yuk MH, Harvill ET, Miller JF (1998) Система контроля вирулентности BvgAS регулирует секрецию типа III у Bordetella bronchiseptica.Молекулярная микробиология 28: 945–959. pmid: 9663681
- 38. McFall-Ngai M, Hadfield MG, Bosch TC, Carey HV, Domazet-Lošo T. и др. (2013) Животные в бактериальном мире — новый императив для наук о жизни. Труды Национальной академии наук 110: 3229–3236.
Распределенная база данных с открытым исходным кодом Решение Porxy
На основе этого могут быть достигнуты балансировщик нагрузки сервера, разделение на чтение и запись и высокая доступность. По сравнению с официальным прокси MySQL MySQL, автор подчеркивает удобство конфигурации амебы (файлы конфигурации на основе XML, которые легче писать правила с использованием синтаксиса SQLJEP, чем прокси MySQL на основе сценариев lua).
Amoeba эквивалентен маршрутизатору для запросов SQL. Он нацелен на обеспечение механизмов для балансировки нагрузки сервера, разделения чтения / записи и высокой доступности, а не на их полную реализацию. Вам необходимо использовать MySQL Replication и другие механизмы для реализации синхронизации реплик и других функций. Amoeba также использует подключаемый механизм для управления соединениями с базой данных и реализации маршрутизации. Третьи стороны могут разработать более продвинутые политики взамен авторской реализации.Эта программа в целом соответствует принципу KISS.
Что такое амеба?
Проект Amoeba, среда с открытым исходным кодом, запустил программное обеспечение Amoeba для Mysql в 2008 году. Это программное обеспечение предназначено для уровня прокси-сервера распределенной базы данных MySQL. Он действует как функция маршрутизации SQL при доступе к MySQL на уровне приложения и фокусируется на разработке уровня распределенного прокси-сервера базы данных. Он расположен между Клиентом и Сервером (ами) БД и прозрачен для Клиента.Обеспечивает балансировку нагрузки, высокую доступность, фильтрацию SQL, разделение на чтение и запись, маршрутизацию, связанную с целевой базой данных, и одновременные запросы для объединения результатов из нескольких баз данных. С Amoeba вы можете добиться высокой доступности, балансировки нагрузки и разделения данных из нескольких источников данных. В настоящее время амёба используется на производственных линиях многих предприятий. Основное решение:
- Уменьшите сложную структуру с несколькими базами данных, вызванную разделением данных
- Обеспечивает правила сегментирования и снижает влияние правил сегментирования данных на приложения
- Уменьшить количество соединений между базой данных и клиентом
- Разделение чтения / записи
Зачем нужен Амеба ?
С развитием традиционной технологии баз данных, быстрым развитием технологии компьютерных сетей и расширением области применения приложения баз данных получили широкое распространение в компьютерных сетях.В настоящее время централизованная система баз данных демонстрирует свои недостатки: централизованная обработка неизбежно приведет к снижению производительности. Сборка приложения запускается на компьютере. Как только компьютер выйдет из строя, это повлияет на всю систему, низкая надежность; централизованная обработка приводит к негибкому масштабированию и конфигурации системы, а также к плохой масштабируемости системы. В этой ситуации централизованная база данных будет развиваться в сторону распределенных баз данных. Прозрачная, простая конфигурация и многочисленные преимущества делают Amoeba отличным выбором среди прокси-серверов распределенных баз данных.
Принципы прокси распределенной базы данных
В области распределенных баз данных Amoeba стремится решать проблемы сегментирования данных и централизованно обрабатывать распределенные данные на клиентах. Централизация — понятие относительное. Клиенту не нужно знать физическое место хранения определенных данных. Этой логики можно избежать с точки зрения бизнеса, что значительно упростит клиентские операции с распределенными данными.Преимущества системы распределенных баз данных:
- Снижение затрат. Распределенные базы данных могут быть географически распределенными. Структура системы соответствует требованиям такого распределения. Пользователи могут использовать, запрашивать, поддерживать и выполнять локальное управление, чтобы снизить затраты на связь и избежать централизованных аппаратных устройств, требующих более высоких требований. Кроме того, распределенные базы данных содержат небольшой объем данных на одной машине, и их скорость отклика значительно увеличивается.
- Повышение общей доступности системы. Это позволяет избежать всех последствий паралича, вызванного отказом единственной базы данных.
- Простая масштабируемость и масштабируемость системы. Структура распределенной системы баз данных позволяет легко расширить систему. Новый узел добавляется в базу данных распределенных данных, не влияя на нормальную работу существующей системы. Этот метод более гибкий и экономичный, чем расширение централизованной системы. Расширение крупных систем и обновление системы в централизованных системах часто бывает дорогостоящим и невозможным из-за несовместимости оборудования и сложности изменения программного обеспечения.
Амеба Сопутствующие товары и их введение
1. Amoeba для MySQL
Amoeba для MySQL поддерживает уровень прокси-сервера распределенной базы данных MySQL. Он действует как функция маршрутизации запросов при доступе к MySQL на уровне приложения и фокусируется на разработке прокси распределенной базы данных. Он расположен между клиентом и сервером БД (прозрачен для клиента.Он имеет следующие функции: балансировка нагрузки, высокая доступность, фильтрация запросов, разделение на чтение и запись, связанный с маршрутизацией запрос к целевой базе данных и одновременные запросы для объединения результатов из нескольких баз данных. В Amoeba вы можете добиться высокой доступности, балансировки нагрузки и разделения данных для нескольких источников данных. В настоящее время он используется в производственных линиях многих предприятий. Amoeba для mysql — это виртуальный клиент mysql, который предоставляет протокол mysql. Клиент подключается к амебе так же, как к mysql.Вы должны настроить соответствующие атрибуты аутентификации в амебе.
2. Амеба для Аладдина
Подобно Amoeba для MySQL, протокол MySQL должен использоваться для подключения клиента к Aladdin. Протокол MySQL в основном используется для поддержки широкого спектра языков разработки mysql. Серверная часть Aladdin может одновременно подключаться к различным базам данных. Пока эти базы данных предоставляют драйверы jdbc. Появление aladdin может активно помочь предприятиям в интеграции баз данных.Пользователям не нужно знать, какие типы баз данных и физические адреса используются на сервере. aladdin анализирует операторы SQL и получает запрашиваемые таблицы и условия, затем эти правила объединяются с этими условиями для маршрутизации в соответствующую физическую базу данных.
3. Amoeba для MongoDB
С ростом популярности NoSQL mongoDB, как база данных nosql, получила широкое внимание благодаря своей выдающейся производительности.Можно сказать, что mongoDB заполняет пробелы между традиционными реляционными базами данных и традиционными базами данных «ключ-значение» и обладает обеими выдающимися характеристиками. Amoeba для MongoDB предоставляет полностью автономный и управляемый метод разделения, аналогичный Amoeba для MySQL, и пытается реализовать ту же функцию автоматического разделения. Основанный на платформе Amoeba, аналогично предыдущим продуктам, этот продукт предоставляет такие функции, как обнаружение пульса, балансировщик нагрузки на сервер, переключение при отказе и агрегацию запросов, а также сохраняет предыдущие методы настройки, если вы знакомы с настройкой одного из продуктов Amoeba продукты, начать работу очень просто.
Сравните Amoeba и похожие продукты
1. Сравнение Amoeba для Mysql и MySQL Proxy
В MySQL proxy 6.0, если вы хотите читать / писать, разделяя и читая кластеры и часто записывая кластерные машины, использование mysql proxy требует значительного объема работы. В настоящее время прокси-сервер mysql не имеет готового lua-скрипта. Прокси-сервер Mysql вообще не имеет файла конфигурации, и скрипт lua полностью об этом.Конечно, lua довольно удобен. Следовательно, для выполнения сложной конфигурации требуется большое количество скриптов. Amoeba для Mysql нужно только настроить в соответствии с требованиями.
2. Сравнение Amoeba для mongoDB и mongos
Разделение данных в mongodb имеет понятие чанка. Каждый фрагмент представляет собой сегмент данных (диапазон). Когда размер блока достигает указанного размера данных, он автоматически разделяется на две части.Mongos разделяется на основе сегмента данных (чанка), и поле, основанное на разбиении, должно быть ключом. В настоящее время в большинстве приложений IDS (особенно идентификаторы пользователей) являются последовательными, а у некоторых пользователей могут быть номера мобильных телефонов или номера членских карт. Это затрудняет реализацию разделения диапазона прокси. Следовательно, хотя mongodb mongos предоставляет функцию автоматического сегментирования, разделение данных не поддается контролю и часто не может удовлетворить наши потребности. Amoeba для MongoDB предоставляет полностью автономный и управляемый метод разделения.
Амеба Что я не могу сделать?
- В настоящее время транзакции не поддерживаются.
- Хранимые процедуры в настоящее время не поддерживаются (будут поддерживаться в ближайшем будущем)
- Не подходит для экспорта данных из амебы или запроса больших объемов данных (например, когда запрос возвращает более миллиона записей данных)
- В настоящее время сегментирование базы данных / таблицы не поддерживается.В настоящее время амеба поддерживает только экземпляры Database Sharding. Каждый разделенный узел должен поддерживать одну и ту же структуру таблицы базы данных.
Амеба Архитектура
Amoeba — это среда разработки DataBase Proxy. Он предназначен для решения проблемы разделения данных и разделения чтения / записи. Ниже описывается структура Amoeba.
- На основе Java NIO
- Структура NIO использует неблокирующий режим.В отличие от традиционного программирования Socket, оно тратит впустую системные ресурсы и плохо масштабируется в случае большого количества одновременных запросов.
- Многоразовое подключение к серверу
- Amoeba обеспечивает высокую доступность подключения к базе данных. В системе Amoeba все подключения к базе данных совместно используются всеми клиентами, подключенными к Amoeba одновременно.
- Разделение чтения / записи и разделение данных
- Традиционная технология разделения чтения / записи может быть решена только с помощью клиента или соответствующей технологии драйвера базы данных, и конфигурация клиента также сложна.
- Производительность отдельной базы данных всегда ограничена. На основе Amoeba вы можете найти линейно масштабируемую поддержку нескольких данных. Amoeba предоставляет администраторам баз данных удобное правило сегментирования данных, аналогичное синтаксису SQL.
В то же время клиенту не нужно беспокоиться о том, что слишком много серверов базы данных привнесут дополнительные настройки в приложение.
- Поддерживает высокую доступность и баланс.
- Amoeba обеспечивает обнаружение исключений подключения к базе данных и восстановление подключения.
- Пользователи могут сэкономить на использовании других дорогостоящих аппаратных устройств балансировки нагрузки сервера. Amoeba предоставляет несколько политик балансировки нагрузки сервера баз данных (циклический перебор, количество активных подключений).
- Последовательность амеб
Таинственный 80-нм вирус амебы с почти полным «геномом ORFan» бросает вызов классификации ДНК-вирусов
Abstract
Здесь мы сообщаем об открытии Yaravirus, новой линии амебного вируса с загадочным происхождением и филогенезом.Яравирус представляет собой частицы размером 80 нм и геном дцДНК размером 44 924 п.н., кодирующий 74 предсказанных белка. Более 90% (68) предсказанных генов Yaravirus никогда ранее не описывались и представляют собой ORF. Только шесть генов имели отдаленные гомологи в общедоступных базах данных: экзонуклеаза / рекомбиназа, упаковывающая АТФаза, бифункциональная ДНК-примаза / полимераза и три гипотетических белка. Кроме того, нам не удалось получить вирусные геномы, тесно связанные с Yaravirus, в 8 535 общедоступных метагеномах, охватывающих различные среды обитания по всему миру.Геном Yaravirus также содержал шесть типов тРНК, которые не соответствовали обычно используемым кодонам. Протеомика показала, что частицы Yaravirus содержат 26 вирусных белков, один из которых потенциально представляет собой новый капсидный белок, не имеющий значительной гомологии с основными капсидными белками NCLDV, но с предполагаемым доменом двойного желеобразного валика. Yaravirus расширяет наши знания о разнообразии ДНК-вирусов. Филогенетическая дистанция между Yaravirus и всеми другими вирусами подчеркивает нашу все еще предварительную оценку геномного разнообразия эукариотических вирусов, усиливая необходимость выделения новых вирусов простейших.
Заявление о значимости Было замечено, что у большинства известных вирусов амебы есть много общих черт, которые в конечном итоге побудили авторов классифицировать их в общие эволюционные группы. Здесь мы описываем Yaravirus, сущность, которая может представлять либо первый изолированный вирус Acanthamoeba spp. вне группы NCLDV или, в альтернативном эволюционном сценарии, это удаленный и чрезвычайно редуцированный вирус этой группы. В отличие от других изолированных вирусов амебы, Yaravirus не представлен большой / гигантской частицей и сложным геномом, но в то же время несет большое количество ранее не описанных генов, включая один, кодирующий новый главный белок капсида.Метагеномные подходы также свидетельствовали о редкости Yaravirus в окружающей среде.
Введение
Эволюция и классификация вирусов были предметом интенсивных дискуссий, особенно после открытия гигантских вирусов, заражающих простейших (1–4). Эти вирусы преимущественно характеризуются большим размером вирионов и геномов, кодирующих от сотен до тысяч белков, большая часть которых в настоящее время остается без гомологов в общедоступных базах данных последовательностей (5–9).Эти кодирующие последовательности обычно называют ORFans, и из-за отсутствия филогенетической информации их происхождение и функция все еще остаются загадкой (10–13). Поразительно, но растущее число доступных вирусных геномов демонстрирует наличие огромного набора и большого разнообразия генов без гомологов в текущих базах данных, которые требуют дальнейшего изучения (10). Важно отметить, что многие гены ORFan амебного вируса уже доказали свою функциональность, они экспрессируются и кодируют компоненты вирусных частиц (6, 14).Однако большой набор ORFans затрудняет прогнозирование биологии вирусов, обнаруженных с помощью методов, не зависящих от культивирования, таких как метагеномный анализ, что усиливает необходимость дополнительной изоляции и экспериментальной характеристики новых вирусов.
Все известные в настоящее время изолированные вирусы амеб относятся к нуклеоцитоплазматическим вирусам большой ДНК (NCLDV) (15). В эту группу входят семейства эукариотических вирусов ( Poxviridae, Asfarviridae, Iridoviridae, Ascoviridae, Phycodnaviridae, Marseilleviridae и Mimiviridae ), а также другие линии амебальных вирусов, вирусы мимивирусов, вирусы микозавирусов, вирусы микозовирусов, вирусы микозовирусов, вирусы микозовирусов, пустовирусыNCDLV имеют геномы дцДНК и, как было предложено, имеют общее монофилетическое происхождение на основании критериев, которые включают совместное использование набора предковых вертикально наследуемых генов (16, 17). Из этого небольшого набора генов было обнаружено, что ключевой кластер генов присутствует почти во всех членах NCLDV и состоит из пяти отдельных генов, а именно из семейства ДНК-полимеразы B, прайма-геликазы, упаковывающей АТФазы, фактора транскрипции. и главный белок капсида (MCP), для которого двойная складка желе-ролла (DJR) составляет основной архитектурный класс белков (18, 19).Недавно Международный комитет по таксономии вирусов (ICTV) выдвинул предложение о мегатаксономии вирусов. Супермодуль главного капсидного белка DJR (MCP) ДНК-вирусов присутствует в NCLDV и других икосаэдрических вирусах, которые инфицируют прокариот и эукариот. В дополнение к сигнатуре DJR-MCP, большинство этих вирусов также кодируют дополнительные минорные белки капсида (например, белки пентона) и АТФазы, упаковывающие геном, суперсемейства FtsK-HerA. Согласно этому предложению, эволюционная консервация трех генов морфогенетического модуля в супермодуле DJR-MCP, за исключением всех других вирусов, оправдывает создание области под названием Dividnaviria .Хотя некоторые NCLDV, такие как pandoraviruses, по-видимому, утратили ген DJR-MCP, в их геноме присутствует большой набор генов, которые подтверждают их классификацию в NCLDV (и, следовательно, Dividnaviria ).
Здесь мы описываем открытие Yaravirus, вируса амебы с загадочным происхождением и филогенезом. Яравирус не содержит всех трех отличительных генов Dividnaviria , в которых отсутствует идентифицируемая последовательность минорного капсидного белка с одним желеобразным валиком. Кроме того, у Yaravirus есть загадочный геном, почти полный набор генов которого — ORFans.Яравирус может представлять собой первый выделенный вирус из Acanthamoeba spp. вне группы NCLDV. Этот вирус имеет частицы с каноническим размером 80 нм, что выходит за рамки концепции больших и гигантских вирусов. Таким образом, Yaravirus расширяет наши знания о вирусном разнообразии и бросает вызов существующей классификации ДНК-вирусов.
Результаты
Цикл выделения и репликации яравируса
Поисковое исследование было проведено путем сбора образцов мутной воды из ручьев искусственного городского озера под названием Пампулья, расположенного в городе Белу-Оризонти, Бразилия.Здесь, используя протокол прямого посева образцов воды на культуры Acanthamoeba castellanii (штамм Neff, ATCC 30010), нам удалось выделить новый амебный вирус, который мы назвали Yaravirus brasiliensis, как дань уважения важному персонажу ( Яра, мать вод) мифологических историй коренных племен тупи-гуарани (20). Отрицательное окрашивание выявило присутствие мелких икосаэдрических частиц в супернатанте инфицированных амебных клеток диаметром около 80 нм (рис.1а). Изображения очищенных частиц с помощью криоэлектронной микроскопии позволяют предположить, что частицы Yaravirus представляют собой две оболочки капсида, как ранее описано для Faustovirus (21).
Рисунок 1Частица яравируса и начало вирусного цикла. a Отрицательное окрашивание изолированного вириона Yaravirus. Шкала шкалы 100нм. b Просвечивающая электронная микроскопия (ТЕМ), представляющая начало вирусного цикла, в котором одна частица связана с мембраной клетки-хозяина, а вторая уже была включена амебой внутри эндоцитарной везикулы.Шкала шкалы 200нм. c Детальное изображение внедренной частицы яравируса внутри эндоцитарной везикулы. Шкала шкалы 100нм. d Поглощение вируса амебой может происходить индивидуально, но также и группами частиц, как видно на микрофотографии. Шкала шкалы 250 нм. e Вирусная фабрика полностью развивается, занимая ядерную область и рекрутируя митохондрии вокруг нее. Могут быть различимы две разные области: электронно-просветная область, где вирионы собраны в виде пустых оболочек, и вторая область, образованная несколькими электронно-плотными точками, где геном упакован внутри частиц.Шкала шкалы 500 нм.
В начале заражения у A. castellanii частицы яравируса обнаруживаются прикрепленными к внешней части плазматической мембраны амеб, что свидетельствует об участии рецептора хозяина в интернализации вирионов (рис. 1b). Затем цикл репликации сопровождается включением отдельных или сгруппированных частиц Yaravirus внутрь эндоцитарных пузырьков, которые на более поздней стадии инфекции обнаруживаются рядом с областью, занятой ядром (рис.1б-г). Затем происходит вирусная фабрика, которая полностью превращается в свою зрелую форму, заменяя область, ранее занимаемую ядром клетки, и рекрутируя митохондрии вокруг его границ, что, вероятно, оптимизирует доступность энергии для создания вирионов (рис. 1e). Этап, соответствующий вирусному морфогенезу, происходит аналогично тому, как он наблюдается для других вирусов амебы. Во-первых, он начинается с появления небольших полумесяцев в электронно-просветной области фабрики (рис.1д, рис. 2а). Затем шаг за шагом вирионы приобретают икосаэдрическую симметрию путем последовательного добавления более одного слоя белка или мембранных компонентов вокруг своей структуры (рис. 2а). Сконструированные вирионы с пустым капсидом затем начинают мигрировать к периферии вирусной фабрики, где происходит накопление корпускулярного электронно-плотного материала (рис. 1e, рис. 2b-c). Эти энуклеации разбросаны по периферии инфицированной клетки и, по-видимому, представляют различные области или точки морфогенеза, где происходит заключительный этап созревания Yaravirus.В этих областях капсид Yaravirus заполнен электронно-плотным материалом, и вирус, наконец, готов к высвобождению (рис. 2c — красная стрелка). Иногда также можно наблюдать несколько частиц Yaravirus, упакованных внутри везикулоподобных структур, что указывает на возможное высвобождение путем экзоцитоза, как это наблюдается для других вирусов амеб (22, 23) (рис. 2d). Однако большая часть выделения вируса по-прежнему представлена лизисом амебной клетки с последующим высвобождением частиц яравируса, которые позже достигают супернатанта инфицированной культуры или иногда могут прикрепляться к остаткам клеточных мембран (рис. .2д). Мы также оценили репликацию Yaravirus, одновременно исследуя уменьшение количества клеток-хозяев, связанных с увеличением вирусного генома во время инфекции. Интересно, что в течение первых часов заражения культуры A. castellanii , по-видимому, прогрессивно растут до 24 часов в день, демонстрируя строгий характер репликации вируса Yaravirus (рис. 2f). Затем клетки начинают подвергаться лизису, индуцированному вирусом, только после 72 часов в секунду (рис. 2f). На том же уровне с 96 ч.p.i до 7 дней после заражения не наблюдается изменений в уровнях обнаружения генома Yaravirus, и лизис, кажется, прекращается, а оставшиеся трофозоиты превращаются в цисты (данные не показаны).
Рисунок 2 Морфогенез и высвобождениеYaravirus. a Вирионы собираются путем добавления более одного слоя белка или мембранных компонентов вокруг его структуры. Шкала шкалы 70нм. b Затем частицы начинают мигрировать к периферии клетки, где есть несколько электронно-плотных точек, которые функционируют как морфогенетические структуры для упаковки ДНК внутри частиц яравируса (области внутри пунктирных линий).Шкала шкалы 1000нм. c Подробное изображение морфогенетических областей, где ДНК (красная стрелка) встроена в вирион Yaravirus (черная стрелка). Шкала шкалы 150 нм. d Иногда на заключительном этапе репликации вируса частицы упаковываются внутри везикулоподобных структур, что указывает на возможное высвобождение за счет экзоцитоза. Шкала шкалы 500 нм. e Однако большая часть частиц высвобождается в результате клеточного лизиса и имеет высокое сродство к мембранам клеточного мусора.Шкала шкалы 150 нм. f График, сравнивающий одновременное уменьшение количества клеток-хозяев (красные столбцы) с увеличением генома яравируса во время инфекции (черная линия). Репликацию вирусного генома измеряли с помощью qPCR и рассчитывали с помощью дельта-дельта Ct.
Геном
Секвенирование генома Yaravirus показало наличие двухцепочечной молекулы ДНК длиной 44 924 п.н., несущей в общей сложности 74 предсказанных гена (рис. 3a). Несмотря на меньший геном, чем у других вирусов амебы, Yaravirus кодирует шесть генов тРНК: тРНК-Ser (gct), тРНК-Ser (tga), тРНК-Cys (gca), тРНК-Asn (gtt), тРНК-His (gtg ) и тРНК-Ile (aat) (рис.3а и в). Все они расположены в межгенной области между генами 29 и 30 (рис. 3a и c). В отличие от генов тРНК в тупанвирусах, мы не наблюдали корреляции между изоакцепторами тРНК Yaravirus и кодонами, наиболее часто используемыми вирусом или его хозяином A. castellanii . Геном имеет содержание GC 57,9%, что является одним из самых высоких показателей среди всех обнаруженных на сегодняшний день амебных вирусов. При генетическом анализе Yaravirus имеет спектр содержания GC, который варьируется от 46% до 65%.Анализ межгенных участков генома (содержание GC 46%) не выявил никаких мотивов обогащенной последовательности, которые могли бы указывать на консервативный промотор, в отличие от того, что наблюдается у многих других членов NCLDV (24).
Рисунок 3 Особенности геномаYaravirus. a Круговое представление генома Yaravirus с выделением только шести генов (красные стрелки), которые имеют сходство с аминокислотными последовательностями других организмов в текущих базах данных. Гены, для которых нет совпадений в базах данных, показаны зелеными стрелками. b Процент генов ORFan среди полного генома различных вирусов амебы представлен графиком с красными шкалами. График с зеленоватыми шкалами представляет собой абсолютное количество генов с гомологами в базах данных (гены без ORFan) для каждого из тех же амебных вирусов, проанализированных ранее. c Все шесть предсказанных Yaravirus тРНК, а также их соответствующие последовательности изображены с информацией об их антикодоне (в скобках), длине их нуклеотидов,% содержания GC и положении в межгенных областях генов 29 и 30. .
Если рассматривать только части генома, относящиеся к кодирующим областям, Yaravirus также имеет такую же кодирующую способность, что и другие вирусы, когда их геном был впервые аннотирован, примерно 90%.
Удивительно, но аннотация генома Yaravirus показала, что ни один из его генов не соответствует последовательностям известных организмов, когда мы сравнивали их на уровне нуклеотидов. Когда мы искали гомологию на аминокислотных уровнях, мы обнаружили, что только два предсказанных белка имели совпадения в базе данных Pfam-A, а в общей сложности шесть имели отдаленные совпадения в базе данных nr.Дополнительное предсказание трехмерных структур этих белков указывало на потенциальную функцию еще 4 генов (см. Анализ протеомики). Взятые вместе, более 90% (68) предсказанных генов Yaravirus являются ORFans, чего не наблюдалось для амебных вирусов с момента открытия пандоровирусов (даже после использования более мягких критериев, BLASTp, e-value <10 −3 ) (Рис. 3б) (25). Шесть генов, продукт которых имеет некоторую гомологию с известными белковыми последовательностями (рис. 3b) (таблица 1), гомологичны фрагментам белков, которые, как предполагается, имеют разные функции, таким как бактериальный белок экзонуклеаза / рекомбиназа (ген 2; наилучший результат: Timonella senegalensis ), гипотетический белок (ген 3; лучший результат: A.castellanii ), гипотетический белок (ген 28; лучший результат: Acytostelium subglobosum LB1 — диктиостелид), упаковывающая АТФаза (ген 40; лучший результат: эндемический вирус Pleurochrysis), консервативный гипотетический белок (ген 46; лучший результат: Мельбурневирус, штамм марсельлевируса) и бифункциональная ДНК-примаза / полимераза (ген 69; лучший результат: Marinobacter sp — протеобактерии Alpha ) (Таблица 1).
Таблица 1Гены Yaravirus, сходные с текущими базами данных, и их лучшие результаты
Затем был проведен филогенетический анализ этих различных генов (гены 02, 03, 28, 40, 46 и 69) после их сопоставления с последовательностями белков схожей функции принадлежат к разным членам виросферы и организмам трех клеточных сфер жизни.Учитывая отсутствие представителей в уже известных базах данных, помимо их лучших совпадений, последовательности, соответствующие генам 03 и 28 (оба гипотетических белка), не обладали достаточной генетической информацией для включения в филогенетический анализ. Для анализа, соответствующего гену 02 (экзонуклеаза / рекомбиназа), наблюдали три основные группы для построения морфологии дерева. Яравирус был помещен в одну из этих ветвей, сгруппировавшись с некоторыми членами Eukarya, особенно с каменными кораллами и насекомыми (рис.4). Анализ гена 40 (АТФаза, упаковывающая вирион) показал, что Yaravirus сгруппирован в полифилетическую ветвь с членами, принадлежащими к семейству Mimiviridae , бактериями (хотя многие из этих последовательностей, по-видимому, представляют собой неправильно классифицированные NCLDV из геномов, собранных метагеномом) и Pleurochrysis sp. эндемический вирус 1a и 2. Для филогенетических анализов, соответствующих гену 46 (гипотетический белок, законсервированный в Marseillevirus), Yaravirus был объединен со штаммами Marseillevirus. Для последнего дерева, представляющего анализ на ген 69 (бифункциональная ДНК-примаза / полимераза), мы наблюдали, что Yaravirus разделяет кластер с членами эукариот, соответствующих группам Streblomastix и Phytophthora.Однако следует отметить, что в предыдущем исследовании авторы обнаружили последовательности генов мимивирусов в геноме паразитарного штамма Phytophthora INRA-310 (26). После всех этих анализов важно отметить, что, хотя у Yaravirus есть некоторые гены с представителями в геноме других организмов, их гомология с ортологами очень низкая (от 25,24 до 44,12%), что подчеркивает, что содержание генома Yaravirus существенно отличается от других. члены виросферы (таблица 1).
Рисунок 4Филогенетическое дерево гена Yaravirus, соответствующего вероятной экзонуклеазе / рекомбиназе, представлено в наиболее удачном фрагменте Timonella senegalensis .Также представлены похожие гены, включенные в геном бактерий (зеленый), эукарион (розовый) и других вирусов (синий).
Для обнаружения последовательностей, связанных с Yaravirus, мы исследовали 8 535 общедоступных метагеномов в базе данных IMG / M, которые были созданы из образцов из различных мест обитания по всей нашей планете (27). Мы обнаружили отдаленные гомологи АТФазы Yaravirus (NCVOG0249) с аминокислотной гомологией до 33,9% в метагеномных данных, в то время как ближайшим гомологом в базе данных NCBI nr был гомолог Pleurochrysis sp.эндемический вирус 1a — 33,1%. В филогенетическом дереве вирусной АТФазы Yaravirus разветвился в пределах Mimiviridae как часть высоко поддерживаемой клады, состоящей из его дальних метагеномных родственников и трех вирусов, геномы которых были депонированы в NCBI Genbank и названы Pleurochrysis sp. эндемический вирус 1a, 1b и 2 (рис. 5). В отличие от известных представителей Mimiviridae , вирусные контиги и вирусные геномы в этой кладе имели высокое содержание GC до 62%. Мы также искали белки, подобные предполагаемому MCP Yaravirus, но не смогли найти близкородственные последовательности в метагеномных данных.
Рисунок 5Филогенетическое положение Yaravirus и связанных вирусных последовательностей в Mimiviridae на основе вирусной АТФазы (NCVOG0249). АТФаза Yaravirus выделена желтым цветом. Поддержка ветви обозначена цветными кружками для значений поддержки 90 или ниже. Дерево уходит корнями в поксвирусы. Масштабная полоса указывает замены для каждого сайта. Содержание GC вирусных геномов и контигов, содержащих NCVOG0249, показано вместе со средним содержанием GC свернувшихся клад. Кроме того, показано экологическое происхождение и размеры сборки Yaravirus и связанных вирусных контигов и геномов.Номера доступа (IMG / M) (REF) метагеномных последовательностей указаны в виде цифр перед первым тире в названии последовательности.
Протеомика вируса Yaravirus
Как упоминалось выше, у большинства белков Yaravirus не было обнаруживаемых гомологов в общедоступных базах данных, и, с первой точки зрения, вирус не кодировал белки капсида. Эта особенность побудила нас поближе взглянуть на белки, ответственные за формирование зрелых частиц яравируса. Протеомика выявила в общей сложности 26 вирусных белков, присутствующих в очищенных частицах.Затем мы проанализировали предсказанные трехмерные структуры этих 26 белков, используя две платформы для сравнения доменов, Phyre2 и инструменты Swiss-model (28–33). Примечательно, что только 4 последовательности (гены 11, 12, 41 и 46) имели структурные особенности, сходные с известными белками (таблица 2). Это означает, что почти 90% протеома вириона состоит из ORF. Важно отметить, что тот же подход (предсказание структуры in silico) использовался параллельно для оценки всех 74 предсказанных генов в геноме Yaravirus, что привело к открытию еще двух генов со структурным сходством с другими общедоступными белками. базы данных (ген 02 и 70) (таблица 2).
Таблица 2Аннотация белков Yaravirus, основанная на предсказанной трехмерной структуре белков, кодируемых вирусом.
Данные протеомики показали, что наиболее распространенные белки в вирусных частицах соответствуют генам 41, 46 и 51 (от наибольшего к менее массовому) (Таблица 2). В то время как для третьего по величине экспрессируемого белка мы не смогли найти никаких структурных кандидатов с известной биологической функцией, для последовательностей, представленных генами 41 и 46, мы наблюдали фрагменты белка, напоминающие трехмерную структуру капсида других вирусов (Таблица 2 ).С достоверностью 97% было обнаружено, что соответствующая часть (65%) гена 41 имеет структурную конвергенцию с доменом двойного желеобразного валика MCP вируса Paramecium bursaria Chlorella типа 1. Ген 46, кодируемый предсказанным белком, был Обнаружено, что они имеют структурную конвергенцию с бактериальным секретируемым белком pcsB и белком хвостовой иглы, частью, состоящей из длинной альфа-спирали. Функции белка, кодируемого геном 46, еще предстоит исследовать. Следовательно, нам не удалось убедительно найти какой-либо минорный белок капсида.Также важно отметить, что последовательности, представленные геном 46, идентичны описанным ранее, чтобы быть высококонсервативными (хотя и с неизвестной функцией) в марсельлевирусах и медусавирусах (таблица 1). Наконец, последние два белка, наблюдаемые в протеомике, которые имеют структурные отложения в общедоступных базах данных, представлены генами 11 и 12, оба экспрессируют предсказанные C1-q-подобные белки комплемента.
Обсуждение
В последние годы амебные большие и гигантские вирусы часто обнаруживались по всему миру (5–9, 20, 22, 25, 34–37).Здесь мы описываем Yaravirus brasiliensis, вирус размером 80 нм с геномом, содержащим значительную долю генов (~ 90%), которые ранее никогда не наблюдались. Используя стандартные протоколы, наш самый первый генетический анализ не смог найти какие-либо узнаваемые последовательности капсида или других классических вирусных генов в Yaravirus. Это актуальная особенность, чтобы подчеркнуть важность исследований, связанных с выделением новых вирусных образцов, поскольку, следуя текущим метагеномным протоколам для обнаружения вирусов, яравирус даже не будет распознаваться как вирусный агент (38, 39).По нашим данным, Yaravirus представляет собой первый вирус, выделенный из Acanthamoeba spp. это потенциально не является частью сложной группы NCLDV. Ранее открытые амебные вирусы объединяют несколько характеристик: вирионы большого размера, геномы, кодирующие от сотен до тысяч генов, и предположительно монофилетическое происхождение, что отражается в наличии набора из примерно 20 наиболее вероятных вертикально наследуемых генов (16, 17). Ни одна из этих особенностей не присутствует в Yaravirus, и это делает его потенциально первым изолятом новой группы bona fide амебного вируса.Конечно, мы не можем исключить возможность того, что Yaravirus может представлять собой уменьшенный NCLDV, представляющий сильно дивергентные или даже отсутствующие отличительные белки NCLDV. Недавно подобный случай был описан для трех небольших вирусов ракообразных. Однако, несмотря на их уменьшенный геном по сравнению с другими членами NCLDV, важное количество отличительных генов было общим с этой группой, в отличие от Yaravirus (40). В этом, не менее захватывающем сценарии, Yaravirus будет представлять на сегодняшний день самый маленький член NCLDV как по размеру частиц, так и по размеру генома.Присутствие шести копий тРНК в Yaravirus также впечатляет при анализе с точки зрения избирательного давления, вынуждающего поддерживать эти гены в таком маленьком геноме, по сравнению с более крупными вирусами амеб. Еще более интересно то, что ни один из изоакцепторов, связанных с тРНК Yaravirus, не соответствует кодонам аминокислот, широко используемых вирусом или амебой. Учитывая сложный цикл заражения Yaravirus в Acanthamoeba , можно предположить, что в природе другой организм может выступать в качестве предпочтительного хозяина Yaravirus.
Большинство представителей выделенных на сегодняшний день гигантских вирусов амебы демонстрируют капсид, специально составленный из копий MCP, родственных D13L вируса осповакцины (14, 41). Пандоравирусы являются исключением, поскольку у них, по-видимому, отсутствует белковая оболочка для защиты своих геномов (25). Интересно, что даже некоторые из амеб-хозяев этих вирусов могут нести копии генов MCP, что указывает на возможный горизонтальный перенос генов между вирусом и протистом-хозяином (42, 43). Несмотря на то, что капсид Yaravirus, кажется, не гомологичен NCLDV MCP, один из его наиболее распространенных белков имеет тот же архитектурный двойной желеобразный валик, который наблюдается в MCP гигантских вирусов.Это подчеркивает, как белки с полностью неописанными последовательностями могут быть сформированы эволюционной конвергенцией для выполнения важных биологических функций (44). В совокупности мы можем заключить, что Yaravirus представляет собой новую линию вирусов, выделенных из клеток A. castellanii . Количество неизвестных белков, составляющих частицы яравируса, отражает изменчивость, существующую в вирусном мире, и то, какой потенциал новых вирусных геномов еще предстоит открыть.
Методы
Происхождение образцов и выделение вируса
В 2017 году в целях выделения новых вариантов вирусных амеб мы собрали образцы мутной воды из ручья озера Пампулья, искусственной лагуны, расположенной в городе Белу-Оризонти, Бразилия (19 ° 51 0.60S и 43 ° 58 18,90 Вт). Как только они были собраны, образцы были быстро доставлены в нашу лабораторию и хранились при 4 ° C до дальнейшей обработки. Следуя протоколу, 4 × 10 4 амеб штамма Acanthamoeba castellanii Neff (ATCC 30010) были засеяны в каждую лунку 96-луночного планшета, инокулируя в каждую из них объемом около 100 мкл собранных образцов, первоначально разбавлен 1:10 в буфере PBS. Затем планшеты инкубировали в течение 7 дней при 32 ° C и ежедневно наблюдали за появлением цитопатического эффекта, что может указывать на вероятную вирусную инфекцию.Затем все содержимое лунок было собрано и подверглось трем процессам замораживания и оттаивания и анализа возможных изолятов методом отрицательного окрашивания. К концу собранное содержимое было подвергнуто еще двум слепым пассажам в свежих культурах амеб, но на этот раз в 25 см. 2 Колбы для обработанных культур клеток Nunc ™ с фильтрующими крышками (Thermo Fisher Scientific, США), содержащие около 1 миллиона амебные клетки. После выделения вируса были проведены все следующие эксперименты путем инфицирования клеток Acanthamoeba castellanii при низкой множественности инфекции (MOI) с учетом требовательного цикла репликации вируса Yaravirus.
Просвечивающая электронная микроскопия (ПЭМ), ПЭМ-томография, криоэлектронная микроскопия
Для заливки смол и просвечивающей электронной микроскопии (ПЭМ) Клетки Acanthamoeba castellanii , инфицированные Yaravirus, фиксировали через 20 часов после заражения 2,5% глютаральдегидом в 0,1 Какодилат натрия M буфер. Клетки промывали трижды раствором 0,2 М сахарозы в 0,1 М какодилате натрия. Клетки постфиксировали в течение 1 часа 1% OsO4, разведенным в 0,2 М гексацианоферрате калия (III) / 0.1M какодилат натрия. После промываний дистиллированной водой клетки постепенно обезвоживали этанолом в последовательных 10-минутных ваннах в 30, 50, 70, 96, 100 и 100% этаноле. Замена была достигнута путем последовательного помещения клеток в 25, 50 и 75% растворы Epon на 15 мин. Клетки помещали на 1 ч в 100% раствор Epon и в свежий 100% Epon на ночь при комнатной температуре. Полимеризация происходила с клетками в свежем 100% эпоне в течение 48 ч при 60 °. Ультратонкие срезы толщиной 70 или 300 нм вырезали на ультрамикротоме UC7 (Leica) и помещали на сетки HR25 300 Mesh Copper / Rhodium (TAAB, UK).Контрастирование ультратонких срезов проводили по Рейнольдсу (45). Электронные микрофотографии получали на ТЕМ Tecnai G 20 , работающем при 200 кэВ, оборудованном камерой Eagle с разрешением 4096◻ × 4096 пикселей (FEI)). Для томографии наночастицы золота диаметром 10 нм (Ref. 741957; Sigma-Aldrich) были нанесены на обе стороны срезов перед контрастированием. Серия томографических изображений наклона была получена на G 20 Cryo TEM (FEI) с программным обеспечением Explore 3D (FEI) для диапазонов наклона 110 ° с шагом 1 °.Средняя применяемая дефокусировка составляла -2 мкм. Увеличение варьировалось от 3500 до 29000 с размером пикселей от 3,13 до 0,37 нм соответственно. Размер изображения составил 4096 2 пикселей. Ряды наклона были выровнены с помощью ETomo из программного пакета IMOD (Университет Колорадо, США) методом взаимной корреляции (46). Томограммы были восстановлены с использованием алгоритма взвешенной обратной проекции в программе ETomo от IMOD. Средняя толщина полученных томограмм составила 268,40 ± 64 нм ( n = 16).Fiji / ImageJ (NIH, США) использовался для создания томографических фильмов (47).
Для анализов с помощью криоэлектронной микроскопии супернатант инфицированных культур Acanthamoeba castellanii собирали через 7 дней после заражения и подвергали первому циклу центрифугирования при 1500 g в течение 10 минут, чтобы осаждать остатки клеток из вирус присутствует в супернатанте. Затем часть, содержащую Yaravirus, затем подвергали второму раунду центрифугирования, и вирус концентрировали ультрацентрифугированием при 100.000г в течение 2ч. Следующие шаги были ранее описаны Клозе и др. (21). Вкратце, мкл вирусного раствора помещали на решетку C-Flat 2/2 с тлеющим разрядом (EMS) и погружали замороженными в жидкий этан с использованием Gatan Cryoplunge 3. Затем образцы визуализировали на Talos F200C (ThermoFisher Scientific), оборудованном Ceta. камера (ThermoFisher Scientific).
Последовательность генома и анализ
Геном Yaravirus секвенировали два раза с использованием платформы Illumina Miseq (Illumina Inc., Сан-Диего, Калифорния, США) с приложением парного конца. Затем сгенерированные чтения были собраны de novo с использованием программного обеспечения ABYSS и SPADES, с полученными контигами, упорядоченными программным обеспечением CONTIGuator.py на основе Python. После этого были сделаны прогнозы генов с помощью инструмента GeneMarkS (48). Функциональная аннотация для белков, предсказанных Yaravirus, была сделана путем поиска в базе данных неизбыточных последовательностей белков (nr) GenBank NCBI, с учетом гомологичных белков только последовательностей, которые имели значение е <1 × 10 -3 .Для анализов кПЦР увеличение репликации генома оценивалось в культурах клеток Acanthamoeba castellanii , инфицированных Yaravirus в различные моменты времени (h5, H6, H8, h22, h34, H72, H96 и h268), с использованием праймеров, которые были сконструированы. на основе последовательности гена 69 Yaravirus (праймеры: 5’TGCAGCAAGTCGGTCAAGAT3 ‘и 5’AACTTCCACATGCGAAACGC3’). Условия, используемые в анализе, были описаны ранее (49).
Данные об использовании аминокислот и кодонов сравнивали с данными, представленными Acanthamoeba castellanii и различными штаммами вирусов амеб.Для этого последовательности были загружены из базы данных NCBI и проанализированы с помощью программного обеспечения Artemis 18.0.3. Процент содержания ГХ и перекоса ГХ также были проанализированы с использованием того же программного обеспечения. Последовательности транспортной РНК (тРНК) идентифицировали с помощью инструмента ARAGORN.
Филогенетический анализ был проведен для шести белков Yaravirus, имеющих сходство с другими организмами в базе данных NCBI (Таблица 1). Используя инструмент Clustal W в программе Mega 10.0.5, аминокислотные последовательности этих белков Yaravirus были предварительно выровнены с соответствующими последовательностями представителей виросферы и других клеточных организмов, принадлежащих к трем доменам жизни.Все деревья были построены с использованием метода эволюции максимального правдоподобия с использованием модели на основе матрицы JTT и начальной загрузки 1000 повторов (50).
Протеомика вируса Yaravirus
Для идентификации белков, составляющих частицы Yaravirus, выделенным вирусом инфицировали тридцать колб для клеточных культур размером 75 см2 (Nunc, США), содержащих 7 × 10 6 Acanthamoeba castellanii и цитопатический эффект прослеживался до 7 dpi После тяжелого амебного лизиса содержимое собирали и подвергали первому раунду центрифугирования при 1500 g в течение 10 мин с целью осаждения клеточного дебриса вируса, присутствующего в супернатанте.Затем эту вирусную часть подвергали второму раунду центрифугирования, и вирус концентрировали ультрацентрифугированием при 100000 g в течение 2 часов. Для завершения готовили осадок вируса для 2D-гель-электрофореза и анализа с помощью MALD-TOF и LC-MS / MS, как описано ранее Reteno и соавторами (51)
Метагеномный обзор
АТФаза Yaravirus (NCVOG0249) и предполагаемый Major Capsid Protein (MCP) использовался для запроса 8 535 общедоступных метагеномов в базе данных IMG / M (27) с помощью diamond blastp (v0.9.25.126, (52)). Полученные совпадения белков с охватом более 30% запросов и субъектов и значением E не менее 1e-5 были извлечены из метагеномных данных. Параллельно с этим был использован hmmsearch (версия 3.1b2, hmmer.org) для идентификации и извлечения АТФаз (NCVOG0249) и MCP из 235 эталонных геномов NCDLV с использованием конкретных скрытых марковских моделей (https://bitbucket.org/berkeleylab/mtg-gv- ехр /). Затем извлеченные белки были объединены с запросами Yaravirus, выровнены с MAFFT-linsi (v7.294b, (53)) (ATPase) и MAFFT (MCP), и полученные аминокислотные выравнивания были обрезаны с помощью trimal (v1.4, -gt 0.9, (54)). Филогенетические деревья были построены с использованием IQ-tree (v1.6.12, (55)) с LG + F + R5 (ATPase) и LG + F + R8 (MCP) на основе встроенной функции выбора модели (56) и 1000 ultrafast bootstrap реплики (57). Филогенетическое дерево АТФазы визуализировали с помощью iTol (v5, (58)).
Доступность данных
Данные о геноме и протеомике яравируса будут доступны после публикации рукописи.
Благодарности
Мы благодарим наших коллег из IHU (Университет Экс Марсель) и из Лаборатории де Виру (Федеральный университет штата Минас-Жерайс) за их помощь, особенно Саида Могари, Иссама Хасни, Лину Баррасси, Присциллу Боно, Эрну Крохон, Клаудим , Пауло Феррейра, Джилиан Триндади и Бетания Драмонд.Кроме того, мы благодарим Méditerranée Infection Foundation, Centro de Microscopia da UFMG, CNPq (Conselho Nacional de Desenvolvimento Científico e Tecnológico), CAPES (Coordenação de Aperfeiçomento de Pessoal de Nível de Pessoal de Nível de Superior) и Gerais) за финансовую поддержку. J.A. является исследователем CNPq. B.L.S., J.A., P.C., P.V.M.B. и G.P.O. являются участниками проекта CAPES-COFECUB.
К поляризуемой термодинамике AMOEBA при фиксированной эффективности заряда с использованием подхода двойного силового поля: применение к органическим кристаллам
Первые принципы предсказания структуры, термодинамики и растворимости органических молекулярных кристаллов, которые играют центральную роль в химических, материальных, фармацевтических и технических науках, бросают вызов как функциям потенциальной энергии, так и методологиям отбора проб.Здесь мы рассчитываем абсолютную термодинамику осаждения кристаллов с использованием нового подхода с двойным силовым полем, цель которого состоит в том, чтобы поддерживать точность усовершенствованных мультипольных силовых полей (, например, поляризуемая модель AMOEBA) при выполнении более 95% отбора проб с недорогим фиксированным зарядом ( FC) силовое поле ( например, OPLS-AA). Абсолютные свободные энергии фазового перехода сублимации / осаждения кристаллов были определены с использованием алхимического пути, который вырастает кристаллическое состояние из эталонного состояния пара на основе отбора проб с силовым полем OPLS-AA с последующими термодинамическими поправками двойного силового поля для изменения между разрешениями FC и AMOEBA в обоих конечных состояниях (мы обозначаем трехступенчатый путь как AMOEBA / FC).Важно отметить, что в то время как фазовый переход требует порядка 200 нс отбора проб на соединение, для достижения термодинамических поправок двойного силового поля требовалось всего 5 нс отбора проб, чтобы достичь средней статистической погрешности 0,05 ккал моль −1 . Для пяти органических соединений средняя ошибка без знака между прямым использованием AMOEBA и двойным силовым полем AMOEBA / FC составила всего 0,2 ккал моль -1 и не была статистически значимой. По сравнению с экспериментальной термодинамикой осаждения средняя беззнаковая ошибка для AMOEBA / FC (1.4 ккал моль -1 ) было более чем вдвое меньше, чем нескорректированный OPLS-AA (3,2 ккал моль -1 ). В целом, термодинамические поправки двойного силового поля уменьшили выборку конденсированной фазы в дорогостоящем силовом поле в 40 раз и могут оказаться полезными для стабильности белка или термодинамики связывания в будущем.
У вас есть доступ к этой статье
Подождите, пока мы загрузим ваш контент… Что-то пошло не так. Попробуй еще раз?геном 121137 1882..1891
% PDF-1.4 % 74 0 объект > эндобдж 71 0 объект > поток Acrobat Distiller 7.0 (Windows) 2011-10-14T05: 06: 25 + 05: 30Arbortext Advanced Print Publisher 9.1.510 / W2021-05-24T14: 56: 33-07: 002021-05-24T14: 56: 33-07: 00application / pdf
Microsoft Word — Roe_et_al_6March27_final_copy (1)
% PDF-1.5 % 1 0 obj > эндобдж 5 0 obj > эндобдж 2 0 obj > поток application / pdf

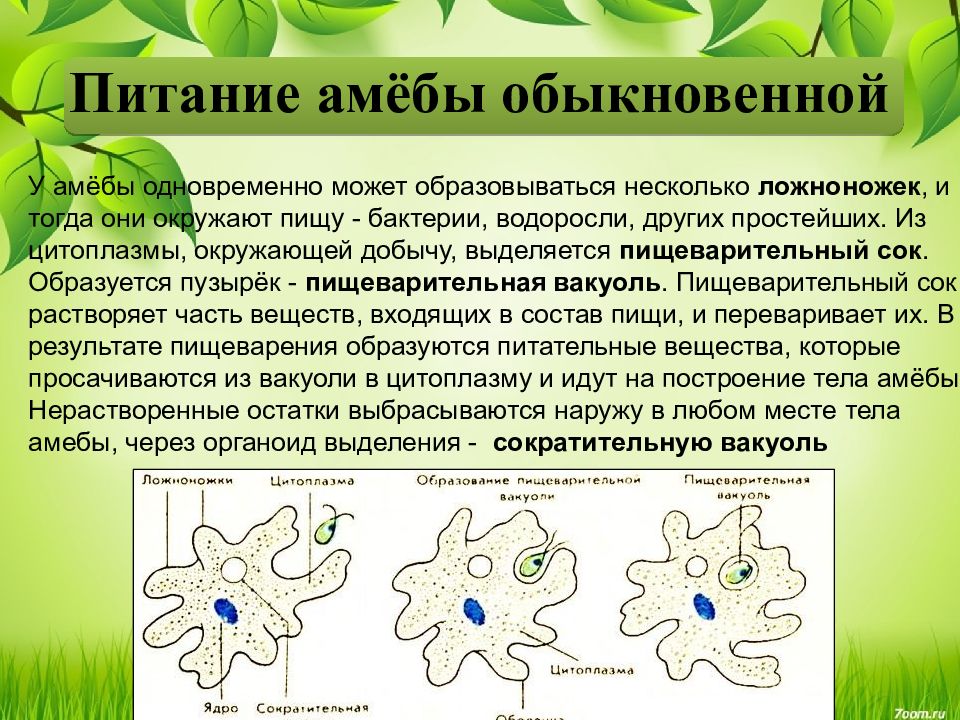 Ядро
Ядро