Тест по биологии для 10 класса по теме «Экология»
Тест по теме «Экология»
1. В экосистеме смешанного леса симбиотические отношения устанавливаются между
1) березами и елями
2) березами и грибами-трутовиками
3) тлями и муравьями
4) ежами и насекомоядными птицами
5) березами и подберезовиками
6) черемухой и опыляющими ее мухами
2. Выберите три верных ответа из шести и запишите в таблицу цифры, под которыми они указаны. Какие антропогенные факторы оказывают влияние на численность популяции ландыша майского в лесном сообществе?
1) вырубка деревьев
2) увеличение затененности
3) недостаток влаги в летний период
4) сбор дикорастущих растений
5) низкая температура воздуха зимой
6) вытаптывание почвы
3. Выберите три верных ответа из шести и запишите в таблицу цифры, под которыми они указаны. Какие биотические факторы могут привести к увеличению численности мышевидных грызунов в еловом лесу?
1) сокращение численности сов, ежей, лис
2) большой урожай семян ели
3) увеличение численности паразитов
4) рубка деревьев
5) глубокий снежный покров зимой
6) уменьшение численности паразитов
4. Смешанный лес – более устойчивая
экосистема, чем березовая роща, так как в лесу
Смешанный лес – более устойчивая
экосистема, чем березовая роща, так как в лесу
1) более плодородная почва
2) больше видов
3) более длинные и разветвленные цепи питания
4) есть продуценты, консументы и редуценты
5) замкнутый круговорот веществ
6) сложные пищевые сети
5. В экосистеме смешанного леса к первичным консументам относятся
1) лоси, зубры
2) кроты, бурозубки
3) зайцы, косули
4) клесты, снегири
5) волки, лисицы
6) синицы, поползни
6. В экосистеме тайги первый трофический уровень в цепях питания составляют
1) ели, лиственницы
2) копытень, кислица
3) шляпочные грибы, бактерии — сапротрофы
4) мхи, папоротники
5) личинки насекомых, дождевые черви
6) бактерии гниения
7. Увеличение численности популяций мышей приводит к увеличению численности
1) белок
2) лисиц
3) ласок
4) дроздов
5) паразитов
6) кротов
8. В водной экосистеме по сравнению с
наземной
В водной экосистеме по сравнению с
наземной
1) стабильный тепловой режим
2) низкая плотность среды
3) пониженное содержание кислорода
4) высокое содержание кислорода
5) резкие колебания теплового режима
6) низкая прозрачность среды
9. Установите последовательность расположения организмов в цепи питания. Запишите в таблицу соответствующую последовательность цифр.
1) чайка
2) окунь
3) мальки рыб
4) водоросль
5) хищная птица
10. Установите соответствие между примерами и видами взаимодействий в экосистемах: к каждой позиции, данной в первом столбце, подберите соответствующую позицию из второго столбца.
ПРИМЕР |
| ВИД ВЗАИМОДЕЙСТВИЯ |
А) птица египетский бегунок и крокодил Б) воловьи птицы и носорог В) широкий лентец и циклоп Г) кишечная палочка и человек Д) комар и человек Е) акула и рыба-лоцман |
| 1) симбиоз 2) паразитизм |
Запишите
в таблицу выбранные цифры под соответствующими буквами.
А | Б | В | Г | Д | Е |
|
|
|
|
|
|
11. Установите соответствие между примерами и типом отношений организмов в экосистеме.
ПРИМЕРЫ |
| ТИП ОТНОШЕНИЙ |
A) распространение пыльцы некоторых растений одним видом насекомых Б) акула и рыба-прилипало B) орхидеи, поселяющиеся на деревьях Г) бактерии в организме человека и животных Д) клубеньковые бактерии Е) микориза |
| 2) комменсализм |
Запишите в ответ цифры, расположив их в порядке, соответствующем буквам:
A | Б | В | Г | Д | Е |
|
|
|
|
|
|
12. Установите соответствие между
примерами и типами межвидового взаимодействия: к каждой позиции, данной в
первом столбце, подберите соответствующую позицию из второго столбца.
Установите соответствие между
примерами и типами межвидового взаимодействия: к каждой позиции, данной в
первом столбце, подберите соответствующую позицию из второго столбца.
ПРИМЕРЫ |
| ТИПЫ ВЗАИМОДЕЙСТВИЯ |
А) аскарида и человек Б) подберёзовик и берёза В) клевер и клубеньковые бактерии Г) малярийный плазмодий и комар Д) актиния и рак-отшельник Е) головня и пшеница |
| 1) паразит-хозяин 2) симбиоз |
Запишите в таблицу выбранные цифры под соответствующими буквами.
А | Б | В | Г | Д | Е |
|
|
|
|
|
|
13. Рассмотрите таблицу «Уровни
организации живой природы» и заполните пустую ячейку, вписав соответствующий
термин.
Рассмотрите таблицу «Уровни
организации живой природы» и заполните пустую ячейку, вписав соответствующий
термин.
Уровень | Пример |
Симбиоз рака отшельника и актинии | |
Видовой | Слон африканский |
14. Проанализируйте таблицу «Биотические взаимодействия между организмами». Заполните пустые ячейки таблицы, используя термины и понятия, приведённые в списке. Для каждой ячейки, обозначенной буквой, выберите соответствующий термин или соответствующее понятие из предложенного списка.
Название взаимодействия | Характеристика взаимодействия | Примеры организмов |
Симбиоз | ____________(Б) | Сосна и белый гриб |
Хищничество | Поедание одного организма другим | ___________(В) |
___________(А) | Использование одним организмом другого в качестве источника питания и места обитания | Спорынья и пшеница |
Список терминов и понятий:
1) нахлебничество
2) конкуренция
3) паразитизм
4) хорёк и куница
5) лисица и мышь
6) взаимное ослабление организмов
7) взаимовыгодное сожительство организмов
8) нейтрализм
Запишите в ответ цифры, расположив их в порядке, соответствующем буквам:
A | Б | |
|
|
|
15. Выберите три верных ответа из шести
и запишите в таблицу цифры, под которыми они указаны.
Выберите три верных ответа из шести
и запишите в таблицу цифры, под которыми они указаны.
Для экосистемы суходольного луга характерно
1. преобладание продуцентов одного вида
2. разнообразный видовой состав трав
3. сбалансированный круговорот веществ
4. отсутствие консументов и редуцентов
5. разветвлённые пищевые цепи
6. преобладание действия искусственного отбора
16. Проанализируйте график, отражающий пищевую специализацию животного, на котором по оси Х обозначен характер питания данного организма, а по оси У – относительное количество перечисленных животных в %, составляющих рацион питания этого организма.
Выберите утверждения, которые можно сформулировать на основании анализа представленных данных.
Запишите в ответе номера выбранных утверждений.
1) Более половины рациона животного составляют крупные грызуны.
2)
Животное — крупный хищник, стоящий в конце пищевой цепи.
3) Животное ведёт стайный образ жизни.
4) Животное относится к всеядным.
5) Населяет разнообразные открытые и наполовину открытые ландшафты.
17. Установите соответствие между животными и группой, к которой оно относится по способу питания
ЖИВОТНОЕ |
| ГРУППА |
А) волк Б) пресноводная гидра В) полевая мышь Г) божья коровка Д) заяц-беляк Е) колорадский жук |
| 1) растительноядные 2) плотоядные |
18. Выберите три верных ответа из шести и запишите цифры, под которыми они указаны. Чем характеризуется биоценоз смешанного леса?
1) ярусностью
2) плохой освещённостью всех ярусов
3) отсутствием сбалансированного круговорота веществ
4) разнообразием древесных растений
5) наличием только консументов второго порядка
6) наличием консументов 1, 2, 3-го порядков
19. Проанализируйте гистограмму состава
рациона животного Z.
Проанализируйте гистограмму состава
рациона животного Z.
По оси х расположены таксоны позвоночных животных, которыми питается животное Z, а по оси у — их количество в рационе. Выберите утверждения, которые можно сформулировать на основании анализа гистограммы.
Животное Z относят к
1) всеядным животным
2) консументам II порядка
3) производителям органических веществ
4) полуводным животным
5) обитателям тундры
20. Выберите три верных ответа из шести и запишите в таблицу цифры, под которыми они указаны.
Численность консументов I порядка в пресноводном водоёме может сократиться вследствие.
1) увеличения численности налима и окуня
2) сокращения численности щук
3) увеличения длины светового дня
4) проявления действия стабилизирующего отбора
5) сокращения численности водорослей и водных растений
6) глубокого промерзания водоёма зимой
21. Выберите три верных ответа из шести
и запишите в таблицу цифры, под которыми они указаны.
Выберите три верных ответа из шести
и запишите в таблицу цифры, под которыми они указаны.
Какие из перечисленных организмов образуют второй трофический уровень?
1) ежа сборная
2) ёж европейский
3) косуля европейская
4) прыткая ящерица
5) полёвка обыкновенная
6) муха-журчалка
22. Установите правильную последовательность звеньев в пищевой цепи, используя все названные объекты.
1) инфузория-туфелька
2) сенная палочка
3) чайка
4) рыба
5) моллюск
6) ил
23. Проанализируйте гистограмму, в которой представлены организмы или их отдельные части и продукты жизнедеятельности, составляющие пищевой рацион животного Z.
Выберите утверждения, которые можно сформулировать на основании анализа представленных данных. Запишите в ответе цифры, под которыми указаны выбранные утверждения.
Животное Z можно отнести к
1) животным, ведущим социальный образ жизни
2) обитателям сухих открытых пространств и перелесков
3) всеядным животным
4) теплокровным животным
5) консументам I порядка
24. Попадание в водоёмы органических
веществ со сточными водами с животноводческих ферм может непосредственно
привести к увеличению численности популяций
Попадание в водоёмы органических
веществ со сточными водами с животноводческих ферм может непосредственно
привести к увеличению численности популяций
1) гетеротрофных бактерий
2) ракообразных
3) цветковых растений
4) многоклеточных водорослей
5) одноклеточных водорослей
6) бактерий-редуцентов
25. Консументом леса является лисица обыкновенная, так как она
1) гетеротроф, хищник
2) поедает растительноядных животных
3) потребляет солнечную энергию
4) выполняет роль редуцента
5) регулирует численность особей в популяции мышей
6) накапливает в теле глюкозу
Экология. Часть в
В заданиях выберите три верных ответа из шести. Запишите выбранные вами буквы в алфавитном порядке или цифры в порядке возрастания.
1. К сокращению численности травянистых растений в лесу могут привести следующие антропогенные факторы:
увеличение численности лосей и зубров
вытаптывание растений туристами
увеличение нор грызунов
сбор редких растений для букетов
вырубка дуплистых деревьев
загрязнение среды обитания растений
2. Какие
биотические факторы могут привести к
увеличению численности мышевидных
грызунов в еловом лесу?
Какие
биотические факторы могут привести к
увеличению численности мышевидных
грызунов в еловом лесу?
сокращение численности сов, ежей, лис
большой урожай семян ели
увеличение численности паразитов
рубка деревьев
глубокий снежный покров зимой
уменьшение численности паразитов
3. Среди экологических факторов укажите биотические.
наводнение
конкуренция между особями вида
понижение температуры
хищничество
недостаток света
образование микоризы
4. В экосистеме смешанного леса симбиотические отношения устанавливаются
между
березами и елями
березами и грибами-трутовиками
тлями и муравьями
ежами и насекомоядными птицами
березами и подберезовиками
черемухой и опыляющими ее мухами
5. В
экосистеме смешанного леса к первичным
консументам относятся
В
экосистеме смешанного леса к первичным
консументам относятся
лоси, зубры
кроты, бурозубки
зайцы, косули
клесты, снегири
волки, лисицы
синицы, поползни
6. В смешанном лесу растения расположены ярусами, что уменьшает конкуренцию между березой и
майскими жуками
черемухой
грибами
шиповником
орешником
мышами
7. В экосистеме тайги первый трофический уровень в цепях питания составляют
ели, лиственницы
копытень, кислица
шляпочные грибы, бактерии — сапротрофы
мхи, папоротники
личинки насекомых, дождевые черви
бактерии гниения
8. Лишайники
первыми заселяют места, непригодные
для жизни других организмов, так как
Лишайники
первыми заселяют места, непригодные
для жизни других организмов, так как
представляют собой симбиоз грибов и одноклеточных водорослей
легко переносят загрязнение окружающей среды
нетребовательны к влажности, теплу, плодородию почвы
поглощают корнями воду и минеральные соли
обеспечиваются водой и минеральными солями с помощью гифов гриба
роль продуцентов в них выполняют гифы гриба
9. Биогеоценозы характеризуются:
сложными пищевыми цепями
простыми пищевыми цепями
отсутствием видового разнообразия
наличием естественного отбора
зависимостью от деятельности человека
устойчивым состоянием
10. Увеличение
численности популяций мышей приводит
к увеличению численности
Увеличение
численности популяций мышей приводит
к увеличению численности
белок
лисиц
ласок
дроздов
паразитов
кротов
11. В водной экосистеме по сравнению с наземной
стабильный тепловой режим
низкая плотность среды
пониженное содержание кислорода
высокое содержание кислорода
резкие колебания теплового режима
низкая прозрачность среды
12. Биогеоценоз пресного водоема характеризуется
наибольшим разнообразием видов в прибрежной зоне
наличием водоросли-ламинарии
3. )
наличием цветковых растений на мелководье
)
наличием цветковых растений на мелководье
отсутствием хищников
малым разнообразием видов
замкнутым круговоротом веществ
13. В экосистеме дубравы саморегуляция проявляется в
сокращении численности деревьев в результате вырубки
минерализации почвы дождевыми червями
усыхании деревьев при устойчивой засухе
зависимости численности белок от урожая желудей
полном уничтожении волками популяции кабанов
ограничении роста численности мышей хищниками
14. Поле капусты — неустойчивая агроэкосистема, так как в ней
отсутствуют пищевые сети
преобладают продуценты одного вида
небольшое число видов
нет пищевых цепей
короткие цепи питания
отсутствуют редуценты
15.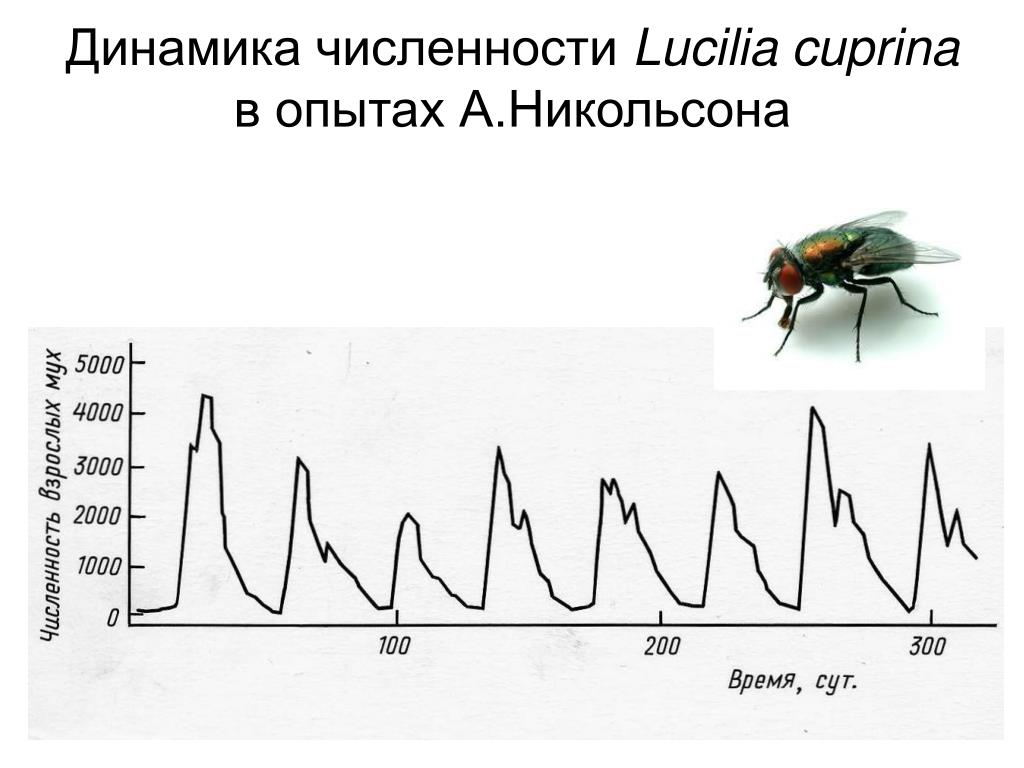 Агроценоз,
в отличие от биогеоценоза, характеризуется
Агроценоз,
в отличие от биогеоценоза, характеризуется
Сравнительная оценка различных моделей дистальной диабетической полинейропатии у крыс: преимущества и недостатки | Абдульвапова
Развитие осложнений сахарного диабета (СД) приводит к значимым социально-экономическим потерям. По данным Международной федерации диабета (IDF), распространенность СД среди взрослого населения планеты (20—79 лет) составляет примерно 9% (415 млн человек). По прогнозам экспертов, к 2040 г. число взрослых больных СД достигнет 642 млн. Неуклонный рост распространенности СД требует разработки эффективных лекарственных средств, методов своевременного выявления и профилактики заболевания. По данным IDF, в России СД страдают 12,1 млн человек, но зарегистрировано всего около 4 млн пациентов. Помощь больным с диабетическим поражением стоп является одной из самых актуальных проблем, поскольку число ампутаций нижних конечностей в большинстве развитых стран неуклонно растет. Это ведет к увеличению численности инвалидов и смертности лиц с СД, существенным образом увеличивает расходы на здравоохранение и социальное обеспечение.
Диабетическая полинейропатия (ДПН) является одним из наиболее распространенных поздних осложнений СД, а также главной причиной формирования язвенных дефектов стоп [1]. Данные о распространенности нейропатии среди лиц с СД варьируют от 28 до 65% и зависят от длительности заболевания и методов диагностики. Начальные признаки повреждения периферической нервной системы обнаруживаются уже у лиц с предиабетом [2].
Сведения о механизмах повреждения нервного волокна при СД достаточно ограничены. Неясно также, какие типы нервных волокон поражаются первыми, и как нарушаются регулируемые нервной системой репарация тканей и местный иммунный статус.
Важным шагом на пути решения этих вопросов является детальный анализ экспериментальных моделей СД (у крыс и мышей), арсенала методов диагностики ДПН и оценки влияния гипергликемии на сроки развития ДПН [3].
Экспериментальные модели СД1 у крыс
Стрептозотоцин (СТЗ)
СТЗ-индуцированный СД — одна из самых часто используемых моделей для изучения ДПН. СТЗ — 2-деокси-2-([(метилнитрозоамино) каринил]амино)-D-глюкопираноза — представляет собой антибиотик, продуцируемый Streptomycetes achromogenes. Гибель β-клеток под его влиянием обусловлена в основном алкилированием и последующим фрагментированием ДНК. В попытках восстановления поврежденной ДНК активируются процессы поли-АДФ-рибозилирования, истощается пул НАД+, нарушается работа митохондрий. Метилирование митохондриальной ДНК отягощает повреждение. Дополнительным механизмом действия СТЗ является активация ксантиноксидазы, что способствует развитию окислительного стресса и гибели клеток. Экспериментальный диабет развивается при однократной внутрибрюшинной или внутривенной инъекции СТЗ в дозе 40—80 мг/кг массы животного. Развитие СД документируется уровнем гликемии выше 15 мМ/л (270 мг/дл). Аллодиния и замедление проведения нервного импульса возникают уже на 2—4-й неделе после введения СТЗ, однако для формирования структурных изменений в нервных волокнах необходимо до 8—16 нед.
СТЗ — 2-деокси-2-([(метилнитрозоамино) каринил]амино)-D-глюкопираноза — представляет собой антибиотик, продуцируемый Streptomycetes achromogenes. Гибель β-клеток под его влиянием обусловлена в основном алкилированием и последующим фрагментированием ДНК. В попытках восстановления поврежденной ДНК активируются процессы поли-АДФ-рибозилирования, истощается пул НАД+, нарушается работа митохондрий. Метилирование митохондриальной ДНК отягощает повреждение. Дополнительным механизмом действия СТЗ является активация ксантиноксидазы, что способствует развитию окислительного стресса и гибели клеток. Экспериментальный диабет развивается при однократной внутрибрюшинной или внутривенной инъекции СТЗ в дозе 40—80 мг/кг массы животного. Развитие СД документируется уровнем гликемии выше 15 мМ/л (270 мг/дл). Аллодиния и замедление проведения нервного импульса возникают уже на 2—4-й неделе после введения СТЗ, однако для формирования структурных изменений в нервных волокнах необходимо до 8—16 нед.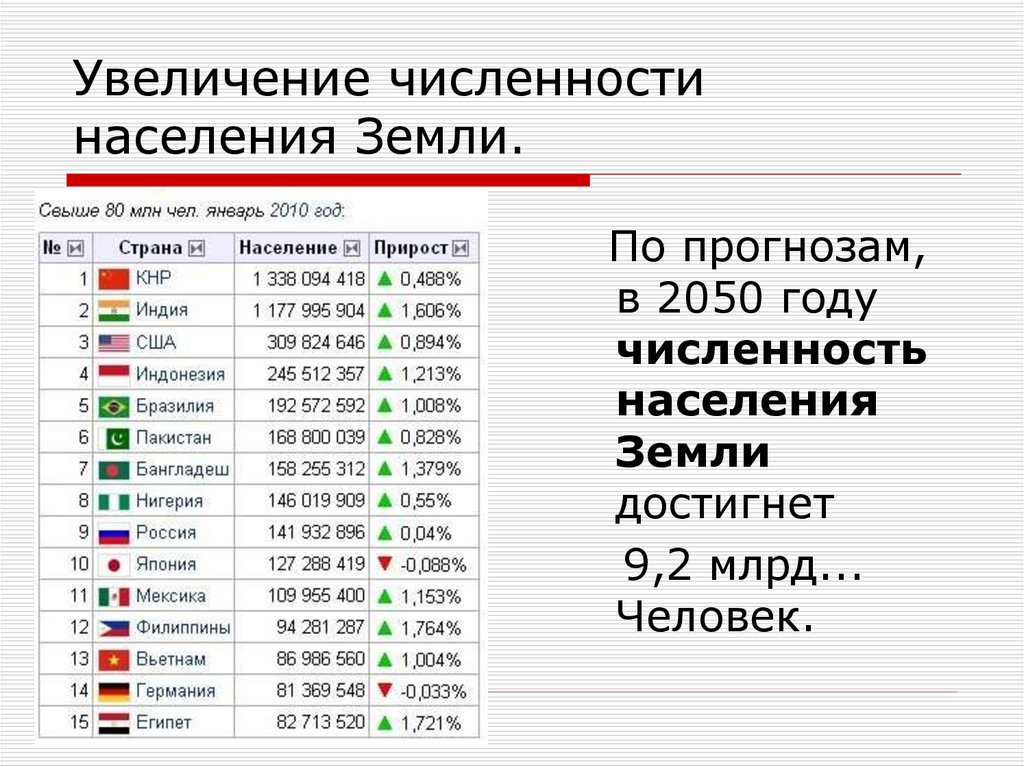 Хотя высокие дозы СТЗ нейротоксичны, убедительно доказано, что нейропатия, развивающаяся при СТЗ-диабете, наиболее сопоставима с ДПН у человека [4].
Хотя высокие дозы СТЗ нейротоксичны, убедительно доказано, что нейропатия, развивающаяся при СТЗ-диабете, наиболее сопоставима с ДПН у человека [4].
У данной модели СД есть ряд очевидных преимуществ. Наибольшее количество исследований проводилось именно на этой модели. Определенным плюсом является и невысокая стоимость эксперимента. У таких животных наблюдаются ранние признаки нейропатии, выявляемые в ходе электрофизиологических тестов, и умеренные изменения в структуре нервных волокон. Однако введение СТЗ не приводит к демиелинизации и потере волокон в нервных пучках (кроме случаев очень длительной патологии). Животные стремительно теряют в весе, у них развивается кетоз, что (при необходимости длительного эксперимента) требует применения поддерживающих доз инсулина [3].
Аллоксан
Для моделирования СД используют и аллоксан (2,4,5,6-оксипиримидин). Это вещество токсично для β-клеток, структурно сходно с глюкозой и легко транспортируется GLUT-2 в клетки поджелудочной железы. В клетках аллоксан восстанавливается и запускает цепочку окислительно-восстановительных реакций с образованием супероксид аниона, который превращается в гидроксил-радикал, обладающий чрезвычайной реакционной способностью. Аллоксан ингибирует глюкокиназу, снижает чувствительность клеток поджелудочной железы к глюкозе и нарушает синтез инсулина [5]. После введения аллоксана у животных быстро развивается стойкая гипергликемия. В настоящее время из двух «химических» моделей чаще используют стрептозотоциновую, так как СТЗ более избирательно действует на β-клетки и менее токсичен для других клеток организма. С помощью ДТЗ можно вызвать частичную гибель β-клеток и спровоцировать «умеренно выраженный» СД. Кроме того, аллоксан менее стабилен в растворах и оказывает токсическое действие на гепатоциты.
В клетках аллоксан восстанавливается и запускает цепочку окислительно-восстановительных реакций с образованием супероксид аниона, который превращается в гидроксил-радикал, обладающий чрезвычайной реакционной способностью. Аллоксан ингибирует глюкокиназу, снижает чувствительность клеток поджелудочной железы к глюкозе и нарушает синтез инсулина [5]. После введения аллоксана у животных быстро развивается стойкая гипергликемия. В настоящее время из двух «химических» моделей чаще используют стрептозотоциновую, так как СТЗ более избирательно действует на β-клетки и менее токсичен для других клеток организма. С помощью ДТЗ можно вызвать частичную гибель β-клеток и спровоцировать «умеренно выраженный» СД. Кроме того, аллоксан менее стабилен в растворах и оказывает токсическое действие на гепатоциты.
Крысы BB/Wor
У склонных к развитию СД крыс BB/Wor отсутствуют Т-лимфоциты, экспрессирующие RT6-аллоантиген, который препятствует аутоиммунной реакции к клеткам собственной поджелудочной железы. У самцов крыс этой линии в возрасте 70—80 дней спонтанно развивается СД1 с абсолютной недостаточностью инсулина/С-пептида, так что им необходима ежедневная инсулинотерапия. Нарушения нервной проводимости развиваются спустя 2 нед от начала заболевания, а через 4 мес наблюдаются потеря нервных волокон и структурные изменения в икроножном нерве [6]. После развития СД животных можно наблюдать более года, поддерживая инсулином необходимый уровень гликемии. Ключевым преимуществом модели BB/Wor является максимальное приближение к естественному развитию СД1. Однако такие животные довольно дороги, а уход за ними трудоемок.
У самцов крыс этой линии в возрасте 70—80 дней спонтанно развивается СД1 с абсолютной недостаточностью инсулина/С-пептида, так что им необходима ежедневная инсулинотерапия. Нарушения нервной проводимости развиваются спустя 2 нед от начала заболевания, а через 4 мес наблюдаются потеря нервных волокон и структурные изменения в икроножном нерве [6]. После развития СД животных можно наблюдать более года, поддерживая инсулином необходимый уровень гликемии. Ключевым преимуществом модели BB/Wor является максимальное приближение к естественному развитию СД1. Однако такие животные довольно дороги, а уход за ними трудоемок.
Модели СД у мышей
Преимуществом мышиных моделей СД является возможность использования разных генетических линий, имитирующих различные механизмы развития патологии. Недостатком же является небольшой размер животных, что требует применения специальных экспериментальных техник.
СД может быть смоделирован у мышей как инбредных, так и аутбредных линий однократным введением СТЗ в дозе 150—200 мг/кг или последовательным в течение нескольких дней его введением по схеме 90+90, 85+70+55 или 100+40+40 мг/кг. Наиболее удачными моделями на сегодняшний день являются линии Swiss—Webster (аутбредные), С57/В16 и CD1 (инбредные). Снижение скорости проведения по нервному волокну, нарушение ответа в сенсорных тестах, потеря нервных волокон происходит на 2—8-й неделе СД. Спустя несколько месяцев возникают истончение миелиновой оболочки и аксональная атрофия. После введения СТЗ у мышей может восстановиться эугликемия, обусловленная пролиферацией остаточных β-клеток, но в отсутствие инсулинотерапии смертность животных достаточно высока.
Наиболее удачными моделями на сегодняшний день являются линии Swiss—Webster (аутбредные), С57/В16 и CD1 (инбредные). Снижение скорости проведения по нервному волокну, нарушение ответа в сенсорных тестах, потеря нервных волокон происходит на 2—8-й неделе СД. Спустя несколько месяцев возникают истончение миелиновой оболочки и аксональная атрофия. После введения СТЗ у мышей может восстановиться эугликемия, обусловленная пролиферацией остаточных β-клеток, но в отсутствие инсулинотерапии смертность животных достаточно высока.
Существует две основные генетические мышиные модели СД1 NOD (non-obese diabetic) и Akita [7—9]. NOD отличаются спонтанным развитием аутоимунного диабета; у мышей Akita наблюдается мутация в гене инсулина. Сроки развития нейропатии у мышей этих линий недостаточно выяснены. У мышей линии Akita развивается средняя или тяжелая нейропатия. Соответствующих животных дорого и трудно содержать; им необходимо ежедневное введение инсулина.
Экспериментальные модели СД2 у крыс
Крысы линии Zucker
Крысы линии Zucker — стандартная модель для изучения метаболического синдрома и СД2.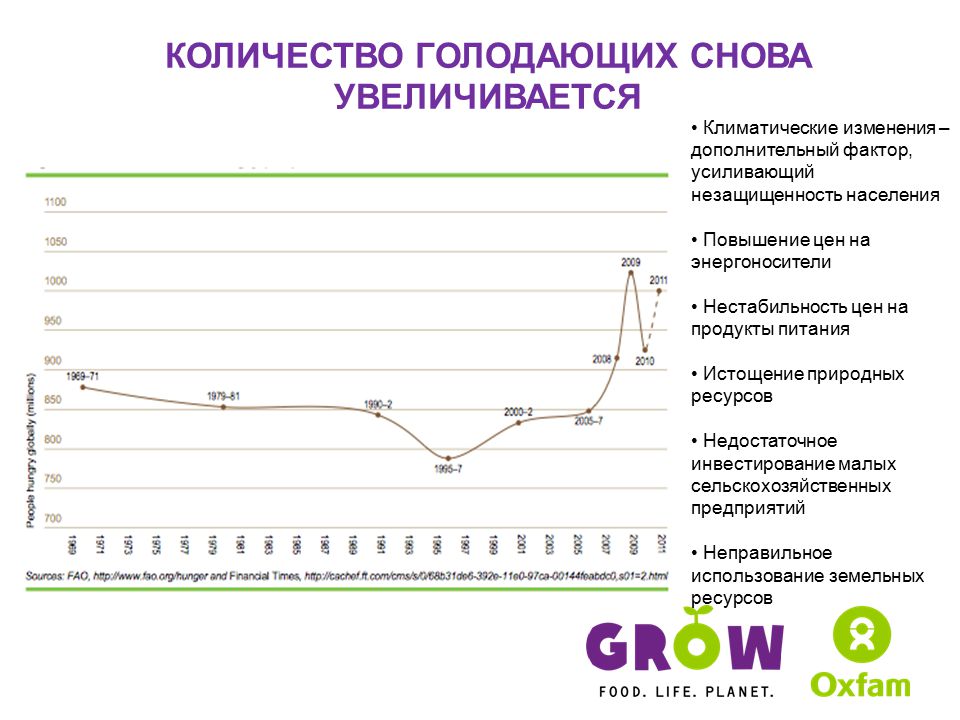 При спонтанной рецессивной мутации fa в гене Lepr гипоталамический рецептор лептина содержит пролин вместо глутамина. Лептин теряет способность взаимодействовать со своим рецептором, что приводит к отсутствию насыщения, и крысы едят в течение всего периода бодрствования [10]. В возрасте 8—10 нед у них развиваются ожирение и гипергликемия [11, 12]. Данную линию крыс использовали для изучения механизмов развития болевой нейропатии [13, 14] и для оценки эффективности различных методов лечения ДПН [15—19].
При спонтанной рецессивной мутации fa в гене Lepr гипоталамический рецептор лептина содержит пролин вместо глутамина. Лептин теряет способность взаимодействовать со своим рецептором, что приводит к отсутствию насыщения, и крысы едят в течение всего периода бодрствования [10]. В возрасте 8—10 нед у них развиваются ожирение и гипергликемия [11, 12]. Данную линию крыс использовали для изучения механизмов развития болевой нейропатии [13, 14] и для оценки эффективности различных методов лечения ДПН [15—19].
Крысы линии Torii с спонтанным развитием СД
В 1988 г. у 5-годовалых крыс линии Sprague—Dawley (SD), страдающих ожирением, развились полидипсия, полиурия и глюкозурия. Для закрепления данной линии животные были скрещены с молодыми самками того же штамма и было получено первое поколение крыс с СД. В 1991 г. у некоторых самцов этой колонии в возрасте 4—5 мес спонтанно развился СД с глюкозурией. В 1997 г. был получен новый инбредный штамм крыс, страдающих ожирением и СД2. Эта линия крыс получила название Torii (SDT) [20]. В настоящее время дистрибьютером крыс линии Torii является «Clea Japan, Inc.» (Токио, Япония). В процессе селекции штамма распространенность СД2 у крыс-самцов в генерации F4 составила 90%, в генерации F9 и последующих — 100%. В генерации F7 СД развивается примерно у 4-месячных самцов. Выживаемость животных с гипергликемией без инсулинотерапии среди самцов к 65 нед составляет 92%, среди самок — 97% [21]. Гликемия натощак значимо увеличивается, достигая к 30 нед 38 ммоль/л (700 мг/дл) и более. У животных регистрируются полидипсия, полифагия, полиурия, глюкозурия. Гипергликемия в большей степени обусловлена снижением секреции инсулина, чем инсулинорезистентностью [22]. На 35-й неделе и позже отмечается значимое увеличение уровня гликированного гемоглобина, степени протеинурии, уровней мочевины и триглицеридов в крови [21]. Таким образом, линия крыс SDT является моделью СД2 с нарушенной секрецией инсулина, но без ожирения.
Эта линия крыс получила название Torii (SDT) [20]. В настоящее время дистрибьютером крыс линии Torii является «Clea Japan, Inc.» (Токио, Япония). В процессе селекции штамма распространенность СД2 у крыс-самцов в генерации F4 составила 90%, в генерации F9 и последующих — 100%. В генерации F7 СД развивается примерно у 4-месячных самцов. Выживаемость животных с гипергликемией без инсулинотерапии среди самцов к 65 нед составляет 92%, среди самок — 97% [21]. Гликемия натощак значимо увеличивается, достигая к 30 нед 38 ммоль/л (700 мг/дл) и более. У животных регистрируются полидипсия, полифагия, полиурия, глюкозурия. Гипергликемия в большей степени обусловлена снижением секреции инсулина, чем инсулинорезистентностью [22]. На 35-й неделе и позже отмечается значимое увеличение уровня гликированного гемоглобина, степени протеинурии, уровней мочевины и триглицеридов в крови [21]. Таким образом, линия крыс SDT является моделью СД2 с нарушенной секрецией инсулина, но без ожирения.
Диабетическая периферическая полинейропатия (ДПН)
Признаки ДПН в эксперименте манифестируют в острую метаболическую фазу, которая чаще всего обратима.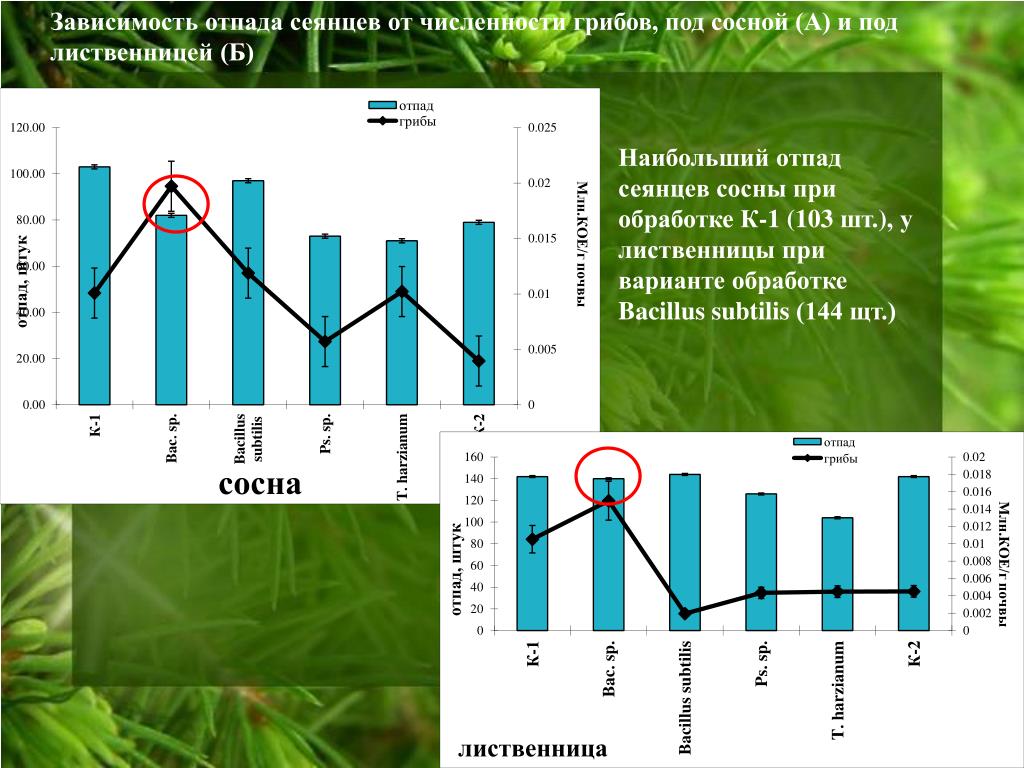 На этой стадии замедляется распространение возбуждения по нервному волокну и развивается гипералгезия. При сохранении гипергликемии нарушения прогрессируют и формируются структурные изменения нерва (хроническая «структурная» фаза).
На этой стадии замедляется распространение возбуждения по нервному волокну и развивается гипералгезия. При сохранении гипергликемии нарушения прогрессируют и формируются структурные изменения нерва (хроническая «структурная» фаза).
При электрофизиологических исследованиях скорость проведения импульса по двигательному волокну у крыс SDT моложе 6 мес не отличалась от нормальных SD крыс, но к 10-му и 12-му месяцам резко снижалась [20, 23]. Скорость проведения по чувствительному волокну также снижалась. Увеличение содержания сорбитола и фруктозы в нерве и снижение миоинозитола указывает на роль полиолового пути в развитии ДПН. Ранирестат (ингибитор альдозоредуктазы) снижает уровень сорбитола в седалищном нерве и увеличивает скорость проведения импульса по двигательному волокну [24].
При морфометрическом анализе у крыс линий SD и SDT моложе 6 мес не отмечалось нарушений структуры миелина, однако в возрасте 12 мес у крыс SDT регистрировалось снижение миелинизации. Количество кровеносных сосудов в оболочке нерва у животных обеих линий не отличалось, однако у крыс SDT наблюдались окклюзированные и истонченные эпиневральные артериолы. Утолщение интимы, возможно, приводит к снижению перфузии нерва, что играет роль в развитии ДПН у SDT крыс. Таким образом, у крыс линии SDT после дебюта СД2 наблюдается ДПН с функциональными и морфологическими изменениями периферических нервов и сосудов [23].
Утолщение интимы, возможно, приводит к снижению перфузии нерва, что играет роль в развитии ДПН у SDT крыс. Таким образом, у крыс линии SDT после дебюта СД2 наблюдается ДПН с функциональными и морфологическими изменениями периферических нервов и сосудов [23].
Диабетическая автономная нейропатия (ДАП)
Гастроинтестинальная форма ДАП у крыс про является диареей. В диагностических тестах (charcoal propulsion test) у крыс линии SDT на 28-й неделе регистрируется усиление моторики желудочно-кишечного тракта [25]. У них увеличены масса тонкой кишки и слизистых оболочек, а также диаметр просвета и высота ворсинок [26].
Крысы линии Zucker Sprague—Dawley
Крысы линии Zucker, как отмечено выше, несут рецессивную мутацию fa в гене Lepr, что приводит к отсутствию насыщения. Однако у людей, как правило, дефицит рецепторов лептина отсутствует. С учетом этого обстоятельства путем скрещивания крыс линии Sprague—Dawley (c алиментарным ожирением) и крыс линии Zucker получены крысы Zucker Sprague—Dawley (ZDSD).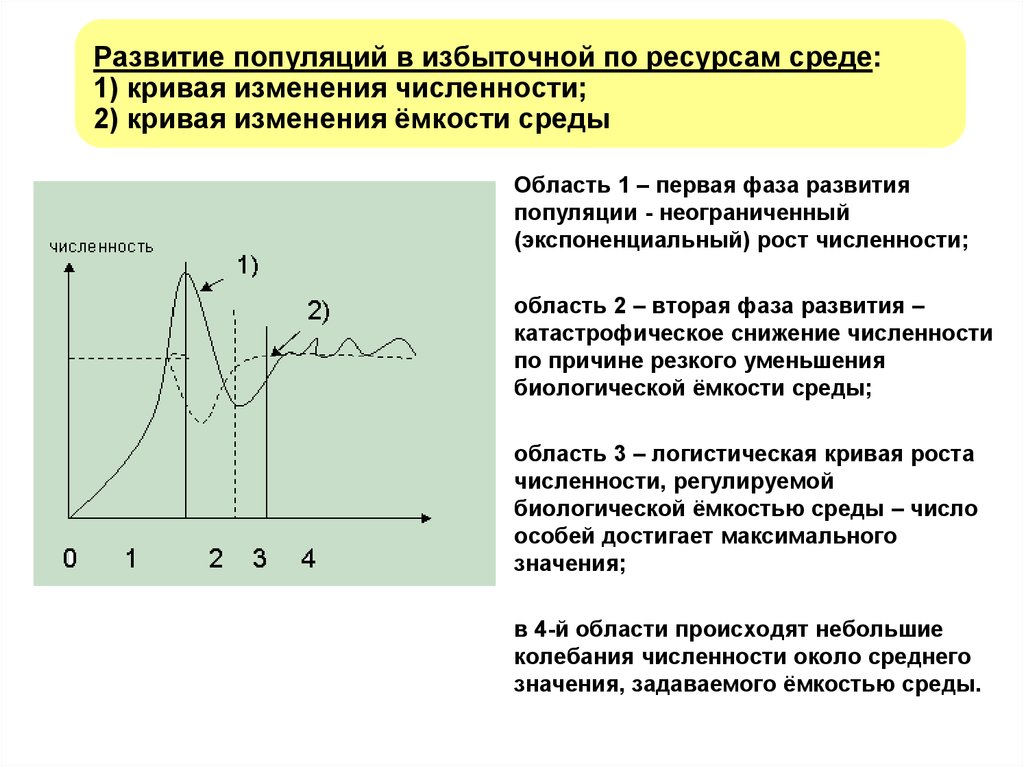 Эти животные предрасположены к ожирению и развитию СД на 15—21-й неделе жизни при высококалорийном питании [27, 28]. У них не нарушен сигнальный путь лептина и накап ливается меньше жира. Хроническая гипергликемия у крыс ZDSD сопровождается повреждением нервов и сосудов, как и в других моделях СД2 [29—32].
Эти животные предрасположены к ожирению и развитию СД на 15—21-й неделе жизни при высококалорийном питании [27, 28]. У них не нарушен сигнальный путь лептина и накап ливается меньше жира. Хроническая гипергликемия у крыс ZDSD сопровождается повреждением нервов и сосудов, как и в других моделях СД2 [29—32].
Однако хроническая гипергликемия у крыс этой линии не приводит к снижению плотности интра эпидермальных нервных волокон, хотя и снижает количество клеток Лангерганса в эпидермисе. После дебюта СД у животных уменьшается количество нервов в субэпителиальном слое роговицы (суррогатный маркер диабетической нейропатии). Крысы линии ZDSD с сохранным сигнальным путем лептина служат хорошей моделью для исследований терапии диабетической нейропатии (ДН).
Крысы линии Goto—Kakizaki (GK)
Крысы линии GK являются одной из лучших моделей ожирения и СД2 [33]. У крыс этой линии на фоне нарушенной толерантности к глюкозе и дефицита инсулина развивается повреждение периферических нервов, прогрессирующее при нарастании гипергликемии.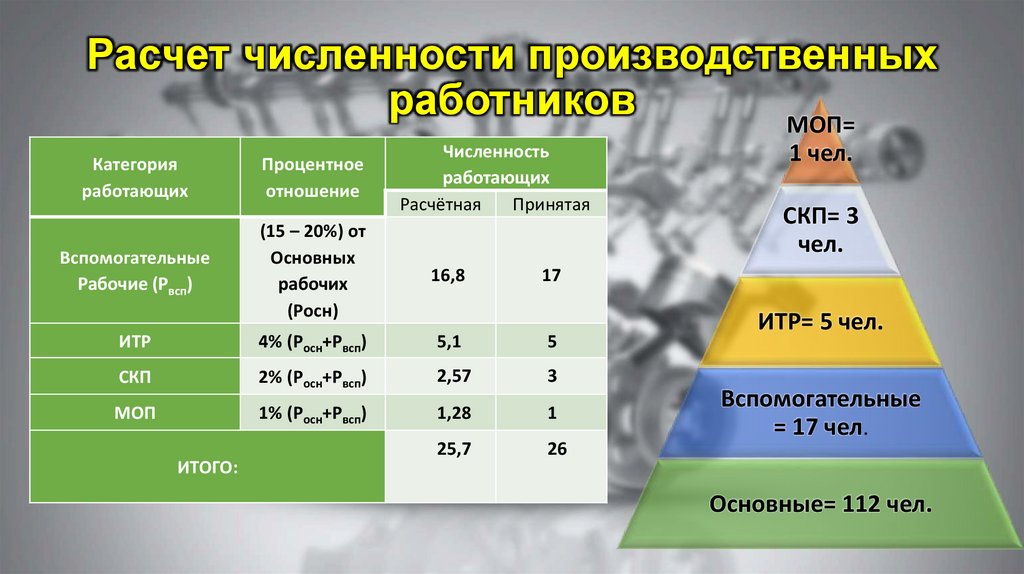 Нормализация гликемии улучшает состояние нервов. У крыс линии GK наблюдалось также повреждение нервов роговицы [34]. Предполагается, что повреждение нервов роговицы способствует развитию диабетической кератопатии у пациентов с СД.
Нормализация гликемии улучшает состояние нервов. У крыс линии GK наблюдалось также повреждение нервов роговицы [34]. Предполагается, что повреждение нервов роговицы способствует развитию диабетической кератопатии у пациентов с СД.
Крысы линии Biobreeding Zucker (BBZDR/Wor)
Крысы линии BBZDR/Wor были получены путем скрещивания резистентных к развитию СД крыс BB/Wor с крысами линии Zucker (дефект рецепторов лептина и инсулинорезистентность) [35]. Линия BBZDR/Wor также характеризуется развитием СД у самцов в возрасте 70—80 дней. Однако диабету у них предшествует ожирение, что позволяет считать это моделью СД2. У этих крыс наблюдаются инсулинорезистентность, гиперинсулинемия, гипергликемия, гиперхолестеринемия, дислипидемия и (на поздних сроках) артериальная гипертензия. Снижение скорости распространения возбуждения по нервному волокну и терминальная гипералгезия развиваются уже к концу 4-й недели заболевания. Структурные изменения, включая потерю волокон икроножного нерва, качественно отличаются от таковых в модели BB/Wor. Основным преимуществом линии BBZDR/Wor является спонтанное развитие гипергликемии, которая длительно сохраняется [6, 35]. К недостаткам модели относится стоимость животных и необходимость инсулинотерапии.
Основным преимуществом линии BBZDR/Wor является спонтанное развитие гипергликемии, которая длительно сохраняется [6, 35]. К недостаткам модели относится стоимость животных и необходимость инсулинотерапии.
Otsuka Long-evans Tokushima Fatty Rats (OLETF)
У крыс OLETF в возрасте 10 мес отмечено значительное снижение тепловой чувствительности и скорости проведения нервного импульса по двигательному волокну [36]. Включение в рацион сахарозы приводило к прогрессированию ДПН, снижению кровотока в седалищном нерве и активности в нем Na+, K+-АТФазы [37].
Заключение
На съезде Европейской группы по изучению ДН были сформулированы минимальные требования к дизайну экспериментальных исследований с оценкой влияния нарушений углеводного обмена на развитие ДПН [3]. Следует рандомизировать животных в группах и подбирать нужное их количество для обес печения статистически и биологически значимых результатов. Важно анализировать исследуемые параметры до индукции СД, а также предусматривать сопоставимую по возрасту и полу группу контроля. Необходимо проводить динамическую оценку массы тела, уровня глюкозы в крови, гликированного гемоглобина и, в зависимости от типа СД, измерять артериальное давление, содержание инсулина и липидов в крови. Исследователи должны указывать условия содержания животных (светлое время суток, продолжительность сна/бодрствования, особенности рациона, количество животных в клетке). План статистического анализа с определением конечных точек исследования должен оставаться неизменным, учитывая и положительные и отрицательные результаты работы. Диагностика ДПН в экспериментальной группе должна проводиться в сравнении с контрольной и подтверждаться наличием как минимум двух из трех исследуемых параметров: поведенческих тестов, скорости проведения импульса по нервному волокну и/или морфологии нервов. Учитывая стремительно растущую заболеваемость преимущественно СД2, необходимо проводить больше экспериментальных исследований на моделях именно этого типа СД2, сопровождающегося гиперлипидемией и другими метаболическими нарушениями, а также артериальной гипертензией.
Необходимо проводить динамическую оценку массы тела, уровня глюкозы в крови, гликированного гемоглобина и, в зависимости от типа СД, измерять артериальное давление, содержание инсулина и липидов в крови. Исследователи должны указывать условия содержания животных (светлое время суток, продолжительность сна/бодрствования, особенности рациона, количество животных в клетке). План статистического анализа с определением конечных точек исследования должен оставаться неизменным, учитывая и положительные и отрицательные результаты работы. Диагностика ДПН в экспериментальной группе должна проводиться в сравнении с контрольной и подтверждаться наличием как минимум двух из трех исследуемых параметров: поведенческих тестов, скорости проведения импульса по нервному волокну и/или морфологии нервов. Учитывая стремительно растущую заболеваемость преимущественно СД2, необходимо проводить больше экспериментальных исследований на моделях именно этого типа СД2, сопровождающегося гиперлипидемией и другими метаболическими нарушениями, а также артериальной гипертензией.
Важнейшим аспектом доклинических исследований является определение четких критериев инструментальной диагностики ДПН для своевременного выявления обратимых и необратимых функциональных нарушений, а также морфологических изменений на клеточном уровне. Моделирование дистальной ДПН у животных позволяет анализировать различные стороны патогенеза этого распространенного осложнения СД и открывает возможность поиска и разработки новых лекарственных препаратов.
Дополнительная информация
Конфликт интересов. Авторы декларируют отсутствие явных и потенциальных конфликтов интересов, связанных с проведенной работой и публикацией настоящей статьи.
Источники финансирования. Поисково-аналитическая работа по подготовке рукописи проведена при финансовой поддержке Российского научного фонда (грант РНФ № 161510365).
Участие авторов: поиск и анализ информации в международных базах данных, написание текста публикации — Абдульвапова З. Н., Артемова Е.В., Горбачева А.М., написание текста публикации, редактирование рукописи — Галстян Г.Р., Гаврилова С.А., Токмакова А.Ю.
Н., Артемова Е.В., Горбачева А.М., написание текста публикации, редактирование рукописи — Галстян Г.Р., Гаврилова С.А., Токмакова А.Ю.
Все авторы прочли и одобрили финальную версию рукописи перед публикацией.
1. Gordois A, Scuffham P, Shearer A, et al. The health care costs of diabetic peripheral neuropathy in the U.S. Diabetes Care. 2003;26(6):1790-1795. doi: 10.2337/diacare.26.6.1790
2. Ziegler D, Strom A, Lobmann R, et al. High prevalence of diagnosed and undiagnosed polyneuropathy in subjects with and without diabetes participating in a nationwide educational initiative (PROTECT study). J Diabetes Complications. 2015; 29(8):998-1002. doi: 10.1016/j.jdiacomp.2015.09.008
3. Biessels GJ, Bril V, Calcutt NA, et al. Phenotyping animal models of diabetic neuropathy: a consensus statement of the diabetic neuropathy study group of the EASD (Neurodiab). J Peripher Nerv Syst. 2014;19(2):77-87. doi: 10.1111/jns5.12072
4. Davidson E, Coppey L, Lu B, et al. The roles of streptozotocin neurotoxicity and neutral endopeptidase in murine experimental diabetic neuropathy. Exp Diabetes Res. 2009;2009:431980. doi: 10.1155/2009/431980
Exp Diabetes Res. 2009;2009:431980. doi: 10.1155/2009/431980
5. Lenzen S. The mechanisms of alloxan- and streptozotocin-induced diabetes. Diabetologia. 2008;51(2):216-226. doi: 10.1007/s00125-007-0886-7
6. Sima AA, Zhang W, Xu G, et al. A comparison of diabetic polyneuropathy in type II diabetic BBZDR/Wor rats and in type I diabetic BB/Wor rats. Diabetologia. 2000;43(6):786-793. doi: 10.1007/s00125005137
7. Sullivan KA, Hayes JM, Wiggin TD, et al. Mouse models of diabetic neuropathy. Neurobiol Dis. 2007;28(3):276-285. doi: 10.1016/j.nbd.2007.07.022
8. Choeiri C, Hewitt K, Durkin J, et al. Longitudinal evaluation of memory performance and peripheral neuropathy in the Ins2C96Y Akita mice. Behav Brain Res. 2005;157(1):31-38. doi: 10.1016/j.bbr.2004.06.005
9. Chang H-J, Gurley SB. Assessment of Diabetic Nephropathy in the Akita Mouse. In: Joost HG, Al-Hasani H, Schürmann A, editors. Animal Models in Diabetes Research. New York: Humana Press; 2012;17-29. doi: 10. 1007/978-1-62703-068-7
1007/978-1-62703-068-7
10. Schmidt I. Metabolic diseases: the environment determines the Odds, even for genes. News Physiol Sci. 2002;17(3):115-121. doi: 10.1152/nips.01380.2001
11. Clark JB, Palmer CJ, Shaw WN. The Diabetic Zucker Fatty Rat. Proc Soc Exp Biol Med. 1983;173(1):68-75. doi: 10.3181/00379727-173-41611
12. Schmidt RE, Dorsey DA, Beaudet LN, Peterson RG. Analysis of the Zucker Diabetic Fatty (ZDF) type 2 diabetic rat model suggests a neurotrophic role for insulin/IGF-I in diabetic autonomic neuropathy. Am J Path. 2003;163(1):21-28. doi: 10.1016/s0002-9440(10)63626-7
13. Jaggi AS, Jain V, Singh N. Animal models of neuropathic pain. Fundam Clin Pharmacol. 2011;25(1):1-28. doi: 10.1111/j.1472-8206.2009.00801.x
14. Lirk P, Flatz M, Haller I, et al. In Zucker diabetic fatty rats, subclinical diabetic neuropathy increases in vivo lidocaine block duration but not in vitro neurotoxicity. Reg Anesth Pain Med. 2012;37(6):601-606. doi: 10.1097/AAP.0b013e3182664afb
15. Li F, Abatan OI, Kim H, et al. Taurine reverses neurological and neurovascular deficits in Zucker diabetic fatty rats. Neurobiol Dis. 2006;22(3):669-676. doi: 10.1016/j.nbd.2006.01.012
Li F, Abatan OI, Kim H, et al. Taurine reverses neurological and neurovascular deficits in Zucker diabetic fatty rats. Neurobiol Dis. 2006;22(3):669-676. doi: 10.1016/j.nbd.2006.01.012
16. Lupachyk S, Watcho P, Hasanova N, et al. Triglyceride, nonesterified fatty acids, and prediabetic neuropathy: role for oxidative-nitrosative stress. Free Radic Biol Med. 2012;52(8):1255-1263. doi: 10.1016/j.freeradbiomed.2012.01.029
17. Lupachyk S, Watcho P, Obrosov AA, et al. Endoplasmic reticulum stress contributes to prediabetic peripheral neuropathy. Exp Neurol. 2013;247:342-348. doi: 10.1016/j.expneurol.2012.11.001
18. Oltman CL, Davidson EP, Coppey LJ, et al. Vascular and neural dysfunction in Zucker diabetic fatty rats: a difficult condition to reverse. Diabetes Obes Metab. 2008;10(1):64-74. doi: 10.1111/j.1463-1326.2007.00814.x
19. Oltman CL, Davidson EP, Coppey LJ, et al. Treatment of Zucker diabetic fatty rats with AVE7688 improves vascular and neural dysfunction. Diabetes Obes Metab. 2009;11(3):223-233. doi: 10.1111/j.1463-1326.2008.00924.x
2009;11(3):223-233. doi: 10.1111/j.1463-1326.2008.00924.x
20. Sasase T, Ohta T, Masuyama T, et al. The spontaneously diabetic torii rat: an animal model of nonobese type 2 diabetes with severe diabetic complications. J Diabetes Res. 2013;2013:976209. doi: 10.1155/2013/976209
21. Shinohara M, Masuyama T, Shoda T, et al. A new spontaneously diabetic non-obese Torii rat strain with severe ocular complications. Int J Exp Diabetes Res. 2000;1(2):89-100. doi: 10.1155/edr.2000.89
22. Masuyama T, Komeda K, Hara A, et al. Chronological characterization of diabetes development in male spontaneously diabetic Torii rats. Biochem Biophys Res Commun. 2004;314(3):870-877. doi: 10.1016/j.bbrc.2003.12.18
23. Yamaguchi T, Sasase T, Mera Y, et al. Diabetic peripheral neuropathy in spontaneously diabetic Torii-Leprfa (SDT Fatty) rats. J Vet Med Sci. 2012;74(12):1669-1673. doi: 10.1292/jvms.12-0149
24. Matsumoto T, Ono Y, Kuromiya A, et al. Long-term treatment with ranirestat (AS-3201), a potent aldose reductase inhibitor, suppresses diabetic neuropathy and cataract formation in rats. J Pharmacol Sci. 2008;107(3):340-348. doi: 10.1254/jphs.08071FP
J Pharmacol Sci. 2008;107(3):340-348. doi: 10.1254/jphs.08071FP
25. Yamada K, Hosokawa M, Fujimoto S, et al. The spontaneously diabetic Torii rat with gastroenteropathy. Diabetes Res Clin Pract. 2007;75(2):127-134. doi: 10.1016/j.diabres.2006.06.034
26. Sasase T, Morinaga H, Yamamoto H, et al. Increased fat absorption and impaired fat clearance cause postprandial hypertriglyceridemia in spontaneously diabetic Torii rat. Diabetes Res Clin Pract. 2007;78(1):8-15. doi: 10.1016/j.diabres.2007.02.020
27. Davidson EP, Coppey LJ, Holmes A, et al. Characterization of diabetic neuropathy in the Zucker diabetic Sprague-Dawley rat: a new animal model for type 2 diabetes. J Diabetes Res. 2014;2014:714273. doi: 10.1155/2014/714273
28. Gonzalez AD, Gallant MA, Burr DB, Wallace JM. Multiscale analysis of morphology and mechanics in tail tendon from the ZDSD rat model of type 2 diabetes. J Biomech. 2014;47(3):681-686. doi: 10.1016/j.jbiomech.2013.11.045
29. Coppey L, Davidson E, Lu B, et al. Vasopeptidase inhibitor ilepatril (AVE7688) prevents obesity- and diabetes-induced neuropathy in C57Bl/6J mice. Neuropharmacology. 2011;60(2-3):259-266. doi: 10.1016/j.neuropharm.2010.09.008
Vasopeptidase inhibitor ilepatril (AVE7688) prevents obesity- and diabetes-induced neuropathy in C57Bl/6J mice. Neuropharmacology. 2011;60(2-3):259-266. doi: 10.1016/j.neuropharm.2010.09.008
30. Coppey LJ, Gellett JS, Davidson EP, et al. Changes in endoneurial blood flow, motor nerve conduction velocity and vascular relaxation of epineurial arterioles of the sciatic nerve in ZDF-obese diabetic rats. Diabetes Metab Res Rev. 2002;18(1):49-56. doi:10.1002/dmrr.257
31. Davidson EP, Coppey LJ, Calcutt NA, et al. Diet-induced obesity in Sprague-Dawley rats causes microvascular and neural dysfunction.Diabetes Metab Res Rev. 2010;26(4):306-318. doi: 10.1002/dmrr.1088
32. Oltman CL, Coppey LJ, Gellett JS, et al. Progression of vascular and neural dysfunction in sciatic nerves of Zucker diabetic fatty and Zucker rats. Am J Physiol Endocrinol Metab. 2005;289(1):E113-E122. doi: 10.1152/ajpendo.00594.2004
33. Akash M, Rehman K, Chen S. Goto-kakizaki rats: its suitability as non-obese diabetic animal model for spontaneous type 2 diabetes mellitus. Curr Diabetes Rev. 2013;9(5):387-396. doi: 10.2174/15733998113099990069
Curr Diabetes Rev. 2013;9(5):387-396. doi: 10.2174/15733998113099990069
34. Wang F, Gao N, Yin J, Yu FS. Reduced innervation and delayed re-innervation after epithelial wounding in type 2 diabetic Goto-Kakizaki rats. Am J Pathol. 2012;181(6):2058-2066. doi: 10.1016/j.ajpath.2012.08.029
35. Tirabassi RS, Flanagan JF, Wu T, et al. The BBZDR/Wor Rat Model for investigating the complications of type 2 diabetes mellitus. ILAR Journal. 2004;45(3):292-302. doi: 10.1093/ilar.45.3.292
36. Kamenov Z, Higashino H, Todorova M, et al. Physiological characteristics of diabetic neuropathy in sucrose-fed Otsuka long-evans Tokushima fatty rats. Methods Find Exp Clin Pharmacol. 2006;28(1):13-18. doi: 10.1358/mf.2006.28.1.962772
37. Nakamura J, Hamada Y, Sakakibara F, et al. Physiological and morphometric analyses of neuropathy in sucrose-fed OLETF rats. Diabetes Res Clin Pract. 2001;51(1):9-20. doi: 10.1016/s0168-8227(00)00205-9
Популяция мышей увеличивается из-за изменения климата, так как спрос на средства для борьбы с вредителями в США резко возрастает
В своем доме в Рокфорде, штат Иллинойс, Рита Дэвиссон сказала, что «одна или две» мыши, которых она обычно видит в уходящие зимние месяцы, «превратились в больше похоже на 10 или 15 дюймов за последние пару лет.
Ученые говорят, что более теплая погода может иметь к этому какое-то отношение.
66-летняя женщина сказала, что наплыв людей побудил ее впервые за более чем 30 лет, которые она прожила в своем доме, обратиться в службу по борьбе с вредителями.
«Они крадутся по подвалу, гаражу, моему заднему двору», — сказала она. «Одной ловушки, которая у меня есть, в последнее время недостаточно».
Исследователи говорят, что потепление и более мягкие зимы увеличили популяцию белоногих мышей, самых многочисленных мелких грызунов, обитающих на большей части востока США и Канады, что означает дополнительную работу для специалистов по борьбе с вредителями.
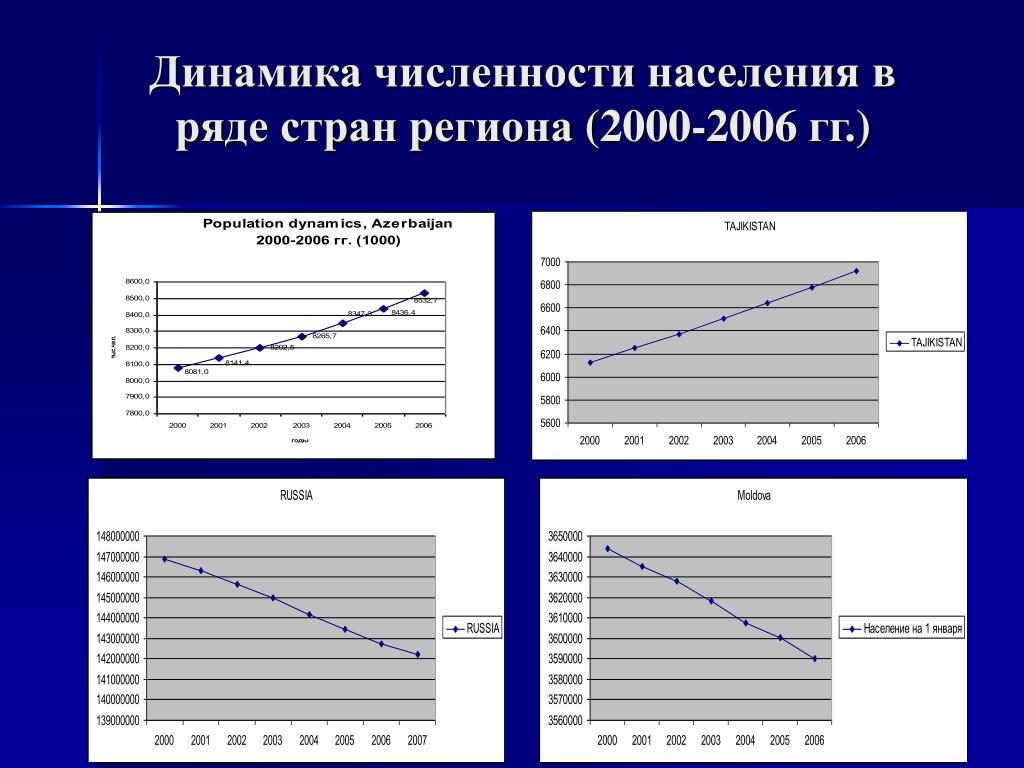
Температуры выше среднего были зарегистрированы прошлой зимой в большинстве восточных и центральных штатов США . С 1970 года средние зимние температуры увеличились как минимум на один градус по Фаренгейту (0,6 по Цельсию) в каждом штате, а в штатах на северо-востоке и в районе Великих озер потепление составило более 3 градусов по Фаренгейту (1,7 по Цельсию).
Исследователи говорят, что потепление и более мягкие зимы увеличили популяцию белоногих мышей.
В то время как популяция мышей обычно сокращается в течение долгих зим, более теплые зимы, вызванные изменением климата, означают, что меньше мышей умирает до весны, сказал Кристиан Флойд, биолог дикой природы из Университета Род-Айленда.
«Эти маленькие млекопитающие всю жизнь дрожат. Они так быстро теряют тепло», — сказал Флойд. «Когда у вас будет более мягкая зима, они выживут лучше. Мышам не нужно так сильно дрожать, и у них меньше шансов умереть от голода, потому что у них больше возможностей охотиться за едой ».
Сьюзен Хоффман, адъюнкт-профессор биологии Университета Майами в Оксфорде, штат Огайо, сказала, что белоногие мыши мигрировали мимо переходного лесного региона, который долгое время служил разделительной линией для многих видов, отметив, что они расширились «на удивление». быстро» в Северной Америке — около 125 миль за 30 лет, в 15 раз дальше, чем ожидалось ранее.
Больше мышей представляют опасность для домовладельцев?
Белоногие мыши, которые исторически распространились из долины Теннесси через северное побережье Атлантического океана, уже расширили свои северные пределы до Квебека, сказал Хоффман.
Прогнозируется, что к 2050 году популяция мышей мигрирует на север в еще большем количестве, особенно потому, что потепление климата отодвигает их предпочтительные лесные места обитания еще дальше на север.
Ава Дикман, техник из AAA Exterminating Inc., заправляет родентицид в приманку для уничтожения мышей и крыс возле дома в Индианаполисе. Кейси Смит/Авторское право 2022 Ассошиэйтед Пресс. Все права защищены.Эта миграция также была зарегистрирована для других видов, включая бурундуков, белок-летяг и мышей-прыгунов с лугов, сказала она.
«Множество доказательств указывают на то, что более высокие температуры и общие климатические эффекты позволяют (белоногим мышам) выживать дальше на север», — сказал Хоффман, добавив, что люди также, вероятно, несут ответственность за непреднамеренное перемещение некоторых мышей на север в автомобилях. лодки и внедорожники.
лодки и внедорожники.
Ученые говорят, что распространение грызунов может привести к увеличению количества мышей в домах и вокруг них.
Майкл Бентли, директор по обучению и обучению Национальной ассоциации по борьбе с вредителями, отметил, что повышенная активность мышей также требует, чтобы специалисты по борьбе с вредителями тратили больше времени на устранение источников пищи и точек входа в дома для контроля популяции мышей.
Сейчас я бы сказал, что от 30% до 40% наших звонков связаны с мышами, что довольно удивительно, учитывая время года. Они просто адаптируются и расширяются… и их становится больше.
Это уже имеет место в Индиане, где Элли Дикман, директор AAA Pest Control, сказала, что технические специалисты заметили всплеск звонков от мышей этой зимой. Призывы к большему количеству мышей в сельских и пригородных домах, а также в городских зданиях продолжались до весны.
«Сейчас я бы сказал, что от 30 до 40 процентов наших звонков связаны с мышами, что довольно удивительно, учитывая время года», — сказал Дикман. «Они просто больше адаптируются и расширяются… и их становится больше».
«Они просто больше адаптируются и расширяются… и их становится больше».
Как насчет последствий для здоровья человека?
Эксперты также предупреждают о более серьезных последствиях для общественного здравоохранения , учитывая, что белоногие мыши являются естественными резервуарами бактерий болезни Лайма, которые затем могут заражать клещей, способных передавать болезнь Лайма людям.
Бактериальное заболевание, вызывающее лихорадку, утомляемость, боль в суставах и кожную сыпь, а также более серьезные осложнения на суставы и нервную систему, является наиболее распространенным трансмиссивным заболеванием в США.
В штатах Мэн, Вермонт и Нью-Гемпшир до сих пор наблюдался самый большой рост числа зарегистрированных случаев, которые Агентство по охране окружающей среды США отчасти связывает с изменением климата.
53-летний Эллиот Смайт, владеющий фермой недалеко от Рэндольфа, штат Вермонт, сказал, что уделяет больше внимания растущему количеству мышей и клещей, а также собственности после своего 15-летнего сына прошлой осенью заразился болезнью Лайма .
«Живя в сельской местности, как и я, я не особо возражал против мышей, — сказал Смайт. «Но когда они продолжают приходить и превращаются в неприятности… ну, теперь у меня проблема».
Со временем смещение мышей на север может означать, что в более южных регионах США будет меньше грызунов, сказал Флойд, но в районах Среднего Запада, Новой Англии и Канады их может быть больше.
«Нам потребуются дополнительные исследования, чтобы лучше понять, где и как быстро двигаются (мыши)», — сказал он. «Нам также нужно больше узнать о том, какую роль могут играть более влажные условия из-за изменения климата. Нам еще многому предстоит научиться».
Здоровье: Ресурсный центр по эпидемиологии: Крысы и мыши
ВВЕДЕНИЕ
House Mouse
The Rat
, распознавая заражение грызунами
Сохраняйте грызуны на улице
Коммерческие и фермерские постройки
Хищники
ловушки
Электронные устройства
878. Усказание грызунов и грызунов. можно найти в каждом городе и ферме страны и вокруг них. Подсчитано, что на каждого человека, живущего в Соединенных Штатах, приходится одна крыса. Грызуны последовали за человеком почти во все части света. У них нет уважения к социальному классу; они вредители равных возможностей.
можно найти в каждом городе и ферме страны и вокруг них. Подсчитано, что на каждого человека, живущего в Соединенных Штатах, приходится одна крыса. Грызуны последовали за человеком почти во все части света. У них нет уважения к социальному классу; они вредители равных возможностей.
Крысы и мыши настолько тесно связаны с человеком, что их называют домашними грызунами. Человек удовлетворяет их три основные потребности: пищу, кров и воду.
Грызуны представляют угрозу для здоровья и мешают нашему экономическому и физическому благополучию.
- Это разрушительные вредители и серьезная угроза безопасности.
- Они разжигают огонь, перегрызая электрические кабели. В следующий раз, когда вы услышите фразу «пожар неизвестного происхождения», подумайте о крысах и мышах.
- Они едят большое количество пищи и еще больше загрязняют их мочой, фекалиями и волосами. Каждый год не менее 20 процентов продуктов питания в мире потребляются или загрязняются крысами и мышами.
- Они повреждают постройки, книги, мебель и даже технику, грызя и закапывая норы.
- Хуже того, они передают болезни людям и другим животным через укусы, перенося блох, вшей, клещей и клещей, а также оставляя свой помет в пище и других материалах, с которыми люди контактируют. Грызуны являются переносчиками бубонной чумы, лихорадки крысиных укусов, лептоспироза, хантавируса, трихинеллеза, инфекционной желтухи, клещевого дерматита, сальмонеллеза, легочной лихорадки и сыпного тифа. Мыши были связаны с астмой.
- Крысы кусают младенцев в их кроватках, потому что запах молока или другой пищи от младенца привлекает крысу, ищущую пищу. Чистый ребенок в чистой кроватке намного безопаснее от нападения крыс. Чтобы защитить ребенка, уберите бутылочку, как только она закончится, и вымойте ему руки и лицо. Сделайте то же самое для всех инвалидов или пожилых людей в вашей семье, которые не могут позаботиться о себе.
Грызунов можно найти в наших домах, супермаркетах, ресторанах, загонах для скота и на фермах. Склады, зерновые мельницы, элеваторы, силосы и зернохранилища особенно уязвимы для заражения грызунами. Грызуны будут есть все, что ест человек или его домашний скот. Они активны ночью. Крыс редко можно увидеть днем, за исключением случаев, когда их популяция чрезвычайно велика. Крысы и мыши могут пролезать в очень маленькие щели, что затрудняет ограничение их движения. Даже если вы их не видите, вы можете услышать их движение после наступления темноты. Если ваш питомец лапает стену или шкаф, возможно, он охотится за затаившимся грызуном. Однако кошки и собаки не являются сдерживающим фактором для грызунов.
Склады, зерновые мельницы, элеваторы, силосы и зернохранилища особенно уязвимы для заражения грызунами. Грызуны будут есть все, что ест человек или его домашний скот. Они активны ночью. Крыс редко можно увидеть днем, за исключением случаев, когда их популяция чрезвычайно велика. Крысы и мыши могут пролезать в очень маленькие щели, что затрудняет ограничение их движения. Даже если вы их не видите, вы можете услышать их движение после наступления темноты. Если ваш питомец лапает стену или шкаф, возможно, он охотится за затаившимся грызуном. Однако кошки и собаки не являются сдерживающим фактором для грызунов.
Обычно первым признаком серьезной проблемы с грызунами является их помет на кухонном столе, в кухонных ящиках, шкафах или кладовой. Если заражено одно жилище, то, скорее всего, заразятся и ближайшие соседи. Вот почему одному домовладельцу так трудно контролировать грызунов. Грызуны — проблема общества. Эффективный контроль требует, чтобы все домовладельцы в сообществе работали вместе, чтобы устранить источники пищи, воды и жилья. Грызуны настойчивы в своих попытках проникнуть в дом, но вы можете эффективно бороться с ними, если знаете их возможности.
Грызуны настойчивы в своих попытках проникнуть в дом, но вы можете эффективно бороться с ними, если знаете их возможности.
Домовая мышь
Домовая мышь ( Mus musculus ) — самое распространенное млекопитающее на Земле. Родом из Центральной Азии, мышь прибыла в Северную Америку с первыми европейскими колонистами. Мышей теперь можно найти по всей Северной Америке, в каждом штате, включая прибрежную Аляску, и во всей Канаде, кроме самой северной.
- Взрослая мышь имеет маленькое стройное тело весом от ½ унции до унции.
- У них большие, редко опушенные уши; маленькие черные выпуклые глаза; слегка заостренный нос; и ряды чешуи, окружающие их длинный, заостренный, редко опушенный хвост.
- Обычно они имеют мех от светло-коричневого до серого или черного цвета с белым или желтовато-коричневым мехом под ним.
- Продолжительность их жизни составляет 9-18 месяцев, хотя некоторые доживают до двух лет в неволе.
Мышь легко адаптируется. Отличный пловец, бегун, альпинист и прыгун. Он может прыгать на высоту до 12 дюймов. У мышей отличное обоняние, вкус и осязание. Хотя у мышей плохое зрение, у мышей хорошее периферическое зрение, которое позволяет им обнаруживать движение. На открытом воздухе мыши гнездятся в сорняках, мусоре, трещинах в скалах или стенах или строят сеть туннелей под землей с камерами для гнезд и складов и несколькими выходами.
Отличный пловец, бегун, альпинист и прыгун. Он может прыгать на высоту до 12 дюймов. У мышей отличное обоняние, вкус и осязание. Хотя у мышей плохое зрение, у мышей хорошее периферическое зрение, которое позволяет им обнаруживать движение. На открытом воздухе мыши гнездятся в сорняках, мусоре, трещинах в скалах или стенах или строят сеть туннелей под землей с камерами для гнезд и складов и несколькими выходами.
Каждую осень с наступлением холодов мыши вынуждены искать пищу и убежище. Мыши любопытны и проникают в любую дыру или трещину размером до ¼ дюйма. Если им нравится то, что они находят внутри, больше, чем то, что у них было снаружи, у вас будут проблемы с мышами. Мыши будут гнездиться в любом скрытом месте рядом с источником пищи. Их гнезда сделаны из тряпок или бумаги, выстланной мелко нарезанным материалом, и выглядят как свободно сплетенный шар диаметром 4-6 дюймов. Если пища доступна, мышь обычно перемещается не более чем на 10-50 футов от своего гнезда. Мыши территориальны и будут постоянно исследовать, чтобы узнать больше об их окружении. Они запоминают пути, препятствия, пищу, воду, убежище и другие элементы в своей среде обитания. Они быстро обнаруживают новые объекты в своем окружении, и они скорее любопытны, чем боятся чего-либо нового.
Мыши территориальны и будут постоянно исследовать, чтобы узнать больше об их окружении. Они запоминают пути, препятствия, пищу, воду, убежище и другие элементы в своей среде обитания. Они быстро обнаруживают новые объекты в своем окружении, и они скорее любопытны, чем боятся чего-либо нового.
Из-за плохого зрения мыши ориентируются с помощью усов, обычно перемещаясь по стене или другому объекту. Если вы не двигаетесь, мышь вас не увидит. Они будут исследовать, когда думают, что они одни… обычно ночью, но и в любое другое время, когда они не обнаруживают движения. Люди обычно видят мышей только тогда, когда они сидят неподвижно, например, когда читают или смотрят телевизор. В отличие от крыс, тот факт, что вы видели мышь, не обязательно означает, что у них высокая плотность популяции.
Семья мышей состоит из доминирующего самца, нескольких самок и их детенышей. Женщины устанавливают свободную иерархию на своей территории. Взрослые мыши заставят своих детенышей разойтись, хотя некоторые самки могут оставаться рядом со своими родителями. Мышь — одно из самых плодовитых млекопитающих.
Мышь — одно из самых плодовитых млекопитающих.
- Самки мышей начинают размножаться в возрасте 40-45 дней.
- Беременность длится всего 18 дней, в помете 3-12 детенышей (в среднем 5-6).
- Самки мышей производят 12 и более пометов в год.
- Новорожденные мыши лишены меха и слепы. Но они быстро растут. Через 2-3 недели они покрыты шерстью, а глаза и уши открыты. В 3 недели щенки начинают совершать короткие вылазки из гнезда и начинают есть твердую пищу.
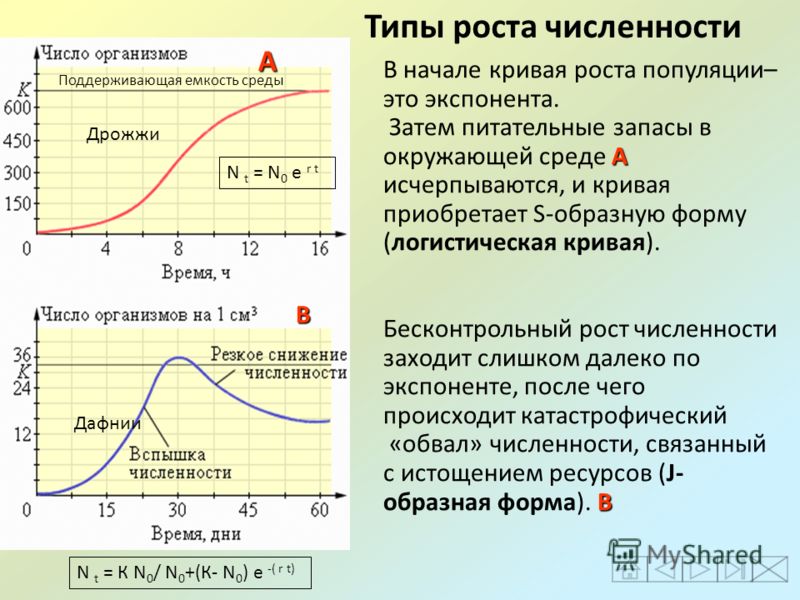
Легко понять, почему популяция мышей может экспоненциально расти при правильных условиях. К счастью, размножение заметно замедляется по мере увеличения популяции мышей.
В то время как они будут пить воду, когда она будет доступна, мыши могут жить в сухой среде обитания, получая всю необходимую им воду из пищи, которую они едят. В дикой природе мыши питаются семенами, корнями, листьями и стеблями, личинками жуков, гусеницами, тараканами и падалью, но предпочитают семена и зерно. Хотя мыши могут питаться крохами, обычно они съедают 3 грамма пищи в день (10-15% от массы тела) или около 8 фунтов в год. Когда доступна человеческая пища, продукты с высоким содержанием жира, белка или сахара часто употребляются в пищу, а не семенам и зерну. Некоторые из их любимых человеческих продуктов включают бекон, шоколад, масло и орехи. Мыши от природы любопытны и не стесняются пробовать новые продукты. Они даже съедят клей или мыло, если мыло содержит животный жир.
Хотя мыши могут питаться крохами, обычно они съедают 3 грамма пищи в день (10-15% от массы тела) или около 8 фунтов в год. Когда доступна человеческая пища, продукты с высоким содержанием жира, белка или сахара часто употребляются в пищу, а не семенам и зерну. Некоторые из их любимых человеческих продуктов включают бекон, шоколад, масло и орехи. Мыши от природы любопытны и не стесняются пробовать новые продукты. Они даже съедят клей или мыло, если мыло содержит животный жир.
Мыши грызут любую доступную пищу, съедая небольшими порциями, чтобы найти то, что им нравится больше всего. Таким образом, мыши уничтожают гораздо больше пищи, чем съедают. В год одна мышь производит около 18 000 фекалий. В них будут храниться продукты, что может привести к заражению насекомыми. Хотя это не их предпочтение, мыши будут жить в морозильных камерах, питаясь только замороженной пищей. Обычно это происходит в крупных коммерческих предприятиях, где есть встроенные холодильники.
Крыса
Норвежская крыса ( Rattus norvegicus ) сильна, очень агрессивна и способна адаптироваться к холодному климату.
- Крысы имеют длину 12-18 дюймов и вес до 16 унций.
- Крысиные морды тупые, а тела кажутся толстыми и тяжелыми.
- У них маленькие глаза, голые уши и грубый мех.
- Крысиные хвосты 6-9 дюймов в длину, чешуйчатые и почти голые.
- У них мех от коричневого до темно-серого, с разбросанными черными волосками, а нижняя часть серая, серовато-коричневая или грязно-белая.
Каждый год крыса теряет более 500 000 волос на теле. Если оставить нетронутыми резцы крысы, они вырастут на 4 дюйма за год. Таким образом, крысы должны постоянно жевать, чтобы изнашивать свои резцы. Крысы будут жевать дерево, алюминиевый сайдинг, стеновые панели, штукатурку, панели, мерзлую землю, бетон… все, кроме стекла и большинства металлов.
- Продолжительность их жизни составляет 9-12 месяцев, хотя некоторые крысы живут до 3 лет.
- Они хорошие пловцы, прыгуны и альпинисты, у них острый слух, обоняние, вкус и осязание.
- Они в основном ведут ночной образ жизни, оставляя свои гнезда в поисках корма в сумерках.
Из-за того, что они так искусно прячутся и бегают, крысы могут существовать в больших количествах без ведома своих соседей-людей. В отличие от мыши, крысы боятся всего нового. Тем не менее, они быстро адаптируются к новым местам жизни, новым распорядкам, новым местам питания и новым видам пищи.
Люди чаще видят крыс с апреля по июнь (весеннее размножение), а затем снова в октябре и ноябре по мере смены сезона. Но крысы активны круглый год. На открытом воздухе крысы зарываются в земляные насыпи, вдоль стен, под мусор или бетонные плиты, но всегда располагаются вблизи источников пищи и воды. Крысы ходят по одним и тем же маршрутам, каждую ночь совершая обход в поисках пищи, поэтому они оставляют очевидные ходы в траве. Крысы часто перемещаются под такими объектами, как тюки, доски, зернохранилища и механизмы, чтобы скрыть свое движение. Крыса обычно перемещается не более чем на 150 футов от своего гнезда, но во время сбора урожая крысы уходят гораздо дальше в поисках корма для кукурузы, пшеницы или бобов, оставленных на полях фермы.
Крыса обычно перемещается не более чем на 150 футов от своего гнезда, но во время сбора урожая крысы уходят гораздо дальше в поисках корма для кукурузы, пшеницы или бобов, оставленных на полях фермы.
На улице или в помещении крысы оставляют явные масляные пятна на своих следах и входных отверстиях. Они могут проникнуть в любое отверстие диаметром более ½ дюйма, что означает, что они могут протиснуться в ваш дом через
- пространство вокруг трубы или канала,
- под дверью (особенно двери гаража, которые остаются открытыми или негерметично),
- через отверстие в сетке или полу,
- или через щель между окном и его рамой.
Крысы проделывают дыры в стенах или полу вскоре после нашествия. Крысиные норы круглые, в среднем 2-3 дюйма в диаметре и обычно находятся всего в нескольких дюймах от пола. Дыры в полах, как правило, расположены близко к стенам. Крысы оставляют характерный мускусный запах, особенно если они ограничены небольшим пространством.
Как и мыши, крысы создают территории и колонии. Доминирующий самец постоянно охраняет свой гарем самок и агрессивно препятствует спариванию других самцов. Самки активно защищают свою группу от чужаков и часто гнездятся вместе. Их гнезда строятся из листьев, бумаги, тряпок, веток и всего, что они могут найти. Крысы ведут ночной образ жизни, но в районах с большой популяцией крыс некоторые низкоранговые крысы будут кормиться днем, потому что другие крысы отказывают им в доступе к еде ночью.
Крысы также очень плодовиты. При достаточном питании и укрытии крысы будут размножаться в течение всего года, хотя зимой рождается меньше пометов.
- Размножение происходит в основном весной и осенью.
- Самка крысы начинает размножаться в возрасте 40-45 дней.
- Самки часто спариваются в течение 18 часов после родов.
- Беременность длится всего 21 день, а в помете 2-14 детенышей (в среднем 7).
- Самки производят 8 и более пометов в год.
- Крысы продолжают размножаться до возраста от 18 до 24 месяцев.
- Новорожденные крысы лишены меха и слепы. Но они быстро растут.
- Через 2-3 недели у них открываются глаза и уши.
- Щенки отнимаются от груди через 3 недели и становятся половозрелыми через 3 месяца. Однако щенки мужского пола должны достаточно развиться, чтобы бросить вызов взрослому самцу за превосходство.
Легко понять, почему популяция крыс может расти в геометрической прогрессии. В идеальных условиях пара крыс может произвести 15 000 потомков за один год. К счастью, размножение заметно замедляется по мере увеличения популяции.
У крыс ненасытный аппетит. Крыса может съедать треть своего веса каждый день. Крыса — настоящее всеядное животное. Он будет есть все, включая мыло, кожу, меха, конфеты, молоко, мясо, овощи, птицу, яйца, зерно, семена, фрукты, орехи, улиток и других грызунов. Крысы ловят рыбу и охотно едят падаль. Вблизи домов крысы питаются кормом для домашних животных, птичьим кормом, семенами трав, мусором, собачьими фекалиями и несъеденной или испорченной пищей, которую мы выбрасываем. Хотя крысы едят почти все, они предпочитают зерно, корм для скота и мясо. В отличие от мышей, которые грызут понемногу, крысы, если это возможно, насытятся за один присест. Крысы будут копить и хранить пищу, что может привести к заражению насекомыми. Как и мыши, крысы будут жить в морозильных камерах, питаясь только замороженной пищей. Крысы едят так много, что одна крыса может оставить после себя 25 000 экскрементов в год . Главный недостаток крысы заключается в том, что она не может долго обходиться без воды, если только ее рацион не обеспечивает достаточного количества воды. Крысам требуется до одной унции воды каждый день.
Хотя крысы едят почти все, они предпочитают зерно, корм для скота и мясо. В отличие от мышей, которые грызут понемногу, крысы, если это возможно, насытятся за один присест. Крысы будут копить и хранить пищу, что может привести к заражению насекомыми. Как и мыши, крысы будут жить в морозильных камерах, питаясь только замороженной пищей. Крысы едят так много, что одна крыса может оставить после себя 25 000 экскрементов в год . Главный недостаток крысы заключается в том, что она не может долго обходиться без воды, если только ее рацион не обеспечивает достаточного количества воды. Крысам требуется до одной унции воды каждый день.
Количество и поведение крыс меняется в течение года. Многие крысы умирают зимой, так как становится трудно найти еду на открытом воздухе. Размножение зимой сравнительно низкое, поэтому популяция крыс самая низкая. Мягкая зима означает, что меньше крыс погибнет по естественным причинам, поэтому весной можно ожидать большего. Но если с крысами бороться зимой, их будет меньше, чтобы возобновить цикл размножения весной. Тяжелое размножение начинается в марте, когда погода меняется. Весенние дожди подстегивают растительность, которая обеспечивает укрытие и дополнительную пищу. Так что поздней весной крыс больше. Молодым крысам приходится искать пищу и новые гнезда. Летом корма и растительности в избытке, поэтому крысы продолжают размножаться. Пик размножения приходится на начало сентября, когда температура начинает падать. Осенью количество пищи и укрытий начинает уменьшаться, поэтому крысы ищут убежища внутри зданий и домов.
Но если с крысами бороться зимой, их будет меньше, чтобы возобновить цикл размножения весной. Тяжелое размножение начинается в марте, когда погода меняется. Весенние дожди подстегивают растительность, которая обеспечивает укрытие и дополнительную пищу. Так что поздней весной крыс больше. Молодым крысам приходится искать пищу и новые гнезда. Летом корма и растительности в избытке, поэтому крысы продолжают размножаться. Пик размножения приходится на начало сентября, когда температура начинает падать. Осенью количество пищи и укрытий начинает уменьшаться, поэтому крысы ищут убежища внутри зданий и домов.
Избавиться от крыс сложно. Отлов или отравление нескольких крыс по соседству мало что даст. Чтобы победить их, сообщество должно сотрудничать в их поимке или убийстве, в то же время морить их голодом, отказывать им в убежище и отключать их источники воды. Лишившись источника пищи, крысы начнут убивать и поедать друг друга, что еще больше снижает заражение.
Распознавание заражения грызунами
Существует двенадцать индикаторов активности грызунов:
- Помет — Обычно первым признаком серьезной проблемы с грызунами является их помет на кухонном столе, в кухонных ящиках и шкафах или в кладовой.
 Ищите мышиный помет в подсобных помещениях, на чердаках, в гаражах и подвалах. Мышиный помет гладкий с заостренными концами и имеет длину от 1/8 до ¼ дюйма. Крысиный помет имеет форму гранул, затупленных с обоих концов, размером с оливковую косточку и блестяще-черного цвета. Вскоре они становятся серо-белыми. Экскременты разбрасываются случайным образом, но, как правило, рядом с беговыми путями грызунов, местами кормления или рядом с убежищем.
Ищите мышиный помет в подсобных помещениях, на чердаках, в гаражах и подвалах. Мышиный помет гладкий с заостренными концами и имеет длину от 1/8 до ¼ дюйма. Крысиный помет имеет форму гранул, затупленных с обоих концов, размером с оливковую косточку и блестяще-черного цвета. Вскоре они становятся серо-белыми. Экскременты разбрасываются случайным образом, но, как правило, рядом с беговыми путями грызунов, местами кормления или рядом с убежищем. - Следы — Следы грызунов можно увидеть в грязи, пыли или голой грязи. Часто следы оставляют и хвосты грызунов. В доме следы мышей можно увидеть на пыльных поверхностях. Вы также можете проверить следы мыши, посыпав подозрительные участки тонким слоем неароматизированного талька или меловой пыли. Подождите день, а затем посветите фонариком на местность. Если в порошке есть небольшие следы, там побывали мыши.
- Грызение — Крысы должны постоянно жевать, чтобы стирать свои резцы. Ищите дыры в стенах или потолках, а также следы в подпольях, за или под шкафами, прилавками, ваннами, душевыми кабинами или возле водонагревателей или печей.

- Норы — Норы можно найти вдоль канав, стен или заборов, а также под зданиями, мусором, низкой растительностью, поленницами или бетонными плитами.
- Взлетно-посадочные полосы — Крысы ходят по одним и тем же маршрутам каждую ночь в поисках пищи. При этом они оставляют взлетно-посадочные полосы шириной 2 дюйма в грязи или траве, обычно рядом со зданиями или заборами.
- Жирные следы — Жирные следы от трения появляются в результате многократного контакта маслянистой шерсти крысы со стенами или входными отверстиями.
- Пятна мочи — Пятна мочи лучше видны при черном свете.
- Гнезда — Мышиные гнезда можно найти в подсобных помещениях, на чердаках, в гаражах и подвалах. Обычно они сделаны из ткани или измельченной бумаги, выстланной мелко измельченным материалом. Крысиные гнезда выглядят как рыхло сплетенный шар диаметром 4-6 дюймов.
- Частично съеденный корм — Мыши оставляют частично съеденный корм.
 Хотя крысы съедают большую часть найденной ими пищи, даже они оставляют характерные признаки, такие как раковины или другие несъедобные предметы.
Хотя крысы съедают большую часть найденной ими пищи, даже они оставляют характерные признаки, такие как раковины или другие несъедобные предметы. - Живые или мертвые грызуны — Люди обычно видят мышей только тогда, когда они сидят неподвижно, например, когда читают или смотрят телевизор. Крысы ведут ночной образ жизни, но в районах с большой популяцией крыс некоторые низкоранговые крысы будут кормиться днем, потому что им отказывают в доступе к еде ночью. Если вы видите крыс днем, это признак серьезного заражения.
- Звуки — Хотя вы можете их не видеть, вы, вероятно, можете слышать, как грызуны передвигаются после наступления темноты. Если ваш питомец цепляется лапами за стену или шкаф, возможно, он пытается добраться до затаившегося грызуна.
- Запахи — Часто можно почувствовать запах мочи грызунов или их мускусный запах, особенно в плохо проветриваемом помещении.
Держите грызунов на открытом воздухе
Лучший способ борьбы с грызунами — это не допускать их в дом . Так как грызуны любят прятаться в растительности, ваша первая линия защиты — обрезать растительность рядом с вашим домом. Чистые дворы лишают грызунов пищи и крова, необходимых им для размножения, и ограничивают способность молодых грызунов переселяться. Груды скошенной травы или обрезков деревьев являются идеальным убежищем для грызунов, поэтому правильно храните и утилизируйте эти материалы. Постарайтесь оставить пару футов свободного пространства между вашим домом и любой растительностью. Грызуны также любят прятаться под поленницами или пиломатериалами; в брошенных автомобилях, технике и мебели; и под мусорными баками. Так что удалите и правильно утилизируйте весь хлам. Храните любые пиломатериалы или древесину на стеллажах на высоте не менее 12 дюймов от земли и вдали от внешней части дома. Храните мусор и мусорные баки также на стеллажах или на бетонной подушке.
Так как грызуны любят прятаться в растительности, ваша первая линия защиты — обрезать растительность рядом с вашим домом. Чистые дворы лишают грызунов пищи и крова, необходимых им для размножения, и ограничивают способность молодых грызунов переселяться. Груды скошенной травы или обрезков деревьев являются идеальным убежищем для грызунов, поэтому правильно храните и утилизируйте эти материалы. Постарайтесь оставить пару футов свободного пространства между вашим домом и любой растительностью. Грызуны также любят прятаться под поленницами или пиломатериалами; в брошенных автомобилях, технике и мебели; и под мусорными баками. Так что удалите и правильно утилизируйте весь хлам. Храните любые пиломатериалы или древесину на стеллажах на высоте не менее 12 дюймов от земли и вдали от внешней части дома. Храните мусор и мусорные баки также на стеллажах или на бетонной подушке.
Ежегодно в конце лета или начале осени проверяйте периметр вашего дома, чтобы убедиться в отсутствии щелей, через которые можно было бы войти. Помните, что для входа мыши достаточно отверстия размером с карандаш . Обратите особое внимание на трубы, электропроводку, кабелепроводы, кабели, двери и окна. Даже там, где проходят подземные инженерные трубы, фундамент должен быть надежно герметизирован. Ночью попросите кого-нибудь осветить внутреннюю часть вашего подвала или стены подвала, пока вы будете кружить по периметру дома снаружи. Потенциальные входные отверстия или другие недостатки, о которых вы можете не знать, будут видны при свете. Закройте все обнаруженные отверстия листовым металлом, металлической тканью или проволочной сеткой. Из кусочков жести, вырезанных из кофейных банок, получаются отличные заплатки. Зачеканка не поможет . Закройте необходимые отверстия, такие как вентиляторы и дымоходы, проволочной сеткой толщиной ¼ дюйма. Проволочная сетка размером более ¼ дюйма не подойдет. Замените недостающие кирпичи. Заполните любые углубления под фундаментом бетоном.
Помните, что для входа мыши достаточно отверстия размером с карандаш . Обратите особое внимание на трубы, электропроводку, кабелепроводы, кабели, двери и окна. Даже там, где проходят подземные инженерные трубы, фундамент должен быть надежно герметизирован. Ночью попросите кого-нибудь осветить внутреннюю часть вашего подвала или стены подвала, пока вы будете кружить по периметру дома снаружи. Потенциальные входные отверстия или другие недостатки, о которых вы можете не знать, будут видны при свете. Закройте все обнаруженные отверстия листовым металлом, металлической тканью или проволочной сеткой. Из кусочков жести, вырезанных из кофейных банок, получаются отличные заплатки. Зачеканка не поможет . Закройте необходимые отверстия, такие как вентиляторы и дымоходы, проволочной сеткой толщиной ¼ дюйма. Проволочная сетка размером более ¼ дюйма не подойдет. Замените недостающие кирпичи. Заполните любые углубления под фундаментом бетоном.
Пристроенные гаражи являются серьезными слабыми местами , потому что гаражные ворота редко подходят так близко, как другие двери.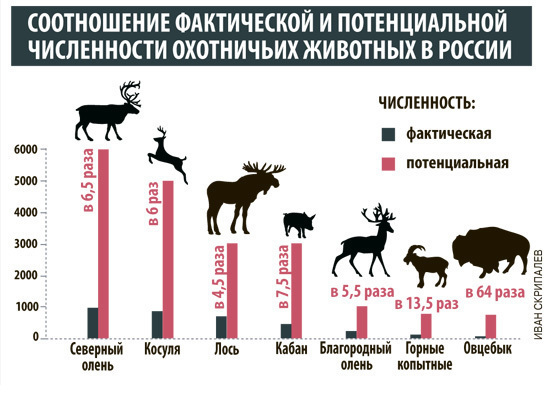 Как только грызун проник в пристроенный гараж, остальная часть дома становится легкой добычей. Поэтому, чтобы сделать гараж менее привлекательным, храните свой хлам и мусор в другом месте. Но если вы должны хранить его там, будьте особенно осторожны, чтобы использовать контейнеры в хорошем состоянии с плотно закрывающимися крышками. Никогда не оставляйте пластиковые мешки для мусора в пристроенном гараже. Опять же, посветите ночью по периметру двери гаража, чтобы увидеть, обеспечивает ли она легкий вход. Проверяйте ворота пристроенных гаражей чаще, чем раз в год.
Как только грызун проник в пристроенный гараж, остальная часть дома становится легкой добычей. Поэтому, чтобы сделать гараж менее привлекательным, храните свой хлам и мусор в другом месте. Но если вы должны хранить его там, будьте особенно осторожны, чтобы использовать контейнеры в хорошем состоянии с плотно закрывающимися крышками. Никогда не оставляйте пластиковые мешки для мусора в пристроенном гараже. Опять же, посветите ночью по периметру двери гаража, чтобы увидеть, обеспечивает ли она легкий вход. Проверяйте ворота пристроенных гаражей чаще, чем раз в год.
Окна и наружные двери должны подходить по размеру , иметь герметизирующие прокладки и быть закрытыми, когда они не используются. В дверях-сетках не должно быть отверстий. Экраны легко залатать. Все края окон и дверей, подверженные прогрызанию, должны быть покрыты металлом.
Даже луж дадут грызунам столько воды, сколько им нужно для питья . Таким образом, все утечки должны быть устранены, а все колеи и впадины должны быть осушены или засыпаны.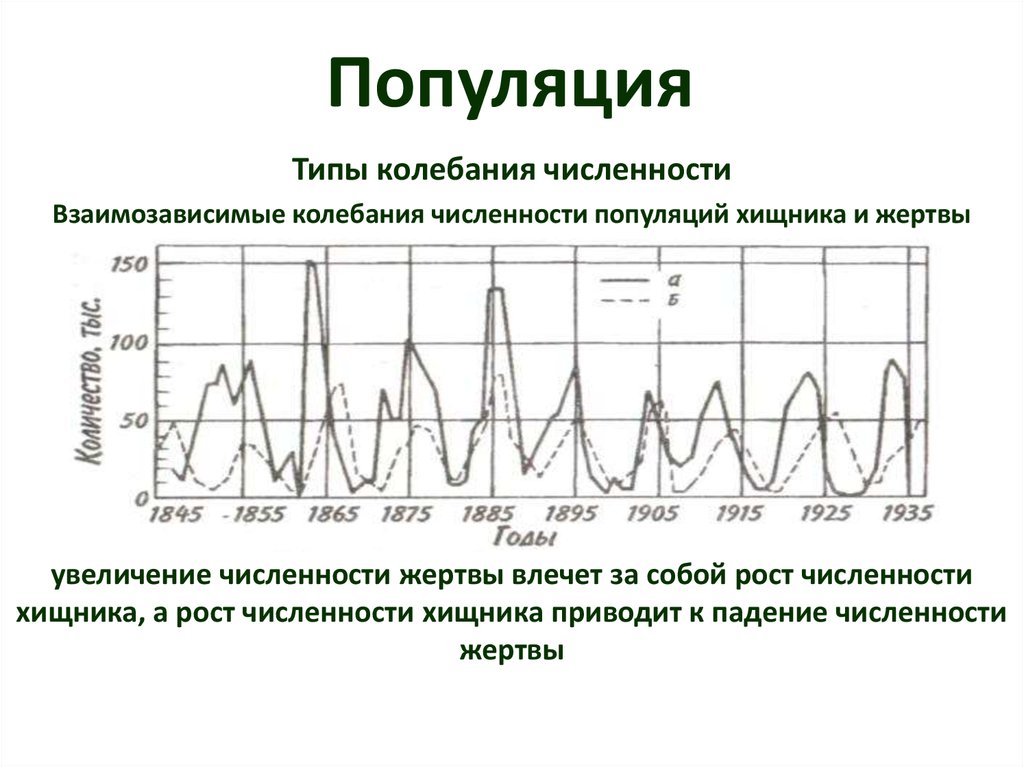 Держите все желоба в чистоте, чтобы вода не застаивалась. Убедитесь, что ваш оконный кондиционер не создает лужу. Накройте бассейны и гидромассажные ванны. Слейте воду из купален для птиц и декоративных прудов. Водяные шланги печально известны протечками в местах соединений; поэтому, когда вы закончите пользоваться шлангом, перекройте воду на кране, а не на насадке шланга. Прекратите полив газона на время заражения.
Держите все желоба в чистоте, чтобы вода не застаивалась. Убедитесь, что ваш оконный кондиционер не создает лужу. Накройте бассейны и гидромассажные ванны. Слейте воду из купален для птиц и декоративных прудов. Водяные шланги печально известны протечками в местах соединений; поэтому, когда вы закончите пользоваться шлангом, перекройте воду на кране, а не на насадке шланга. Прекратите полив газона на время заражения.
Внешние источники пищи, привлекающие грызунов, включают мусор, корм для собак и кошек, собачьи фекалии, птичий корм и фрукты или ягоды , упавшие на землю. Уберите их источники пищи на улицу, и грызуны будут искать другой район для жизни. Собирайте фрукты и овощи во дворе. Соты могут прокормить сотни мышей всю зиму, поэтому тщательно удалите все ульи в непосредственной близости. Птицы едят грязно, что особенно полезно для грызунов. Поэтому перестаньте кормить птиц на время заражения. Если вы кормите белок; вы также кормите грызунов. Если есть возможность, кормите своих питомцев в помещении.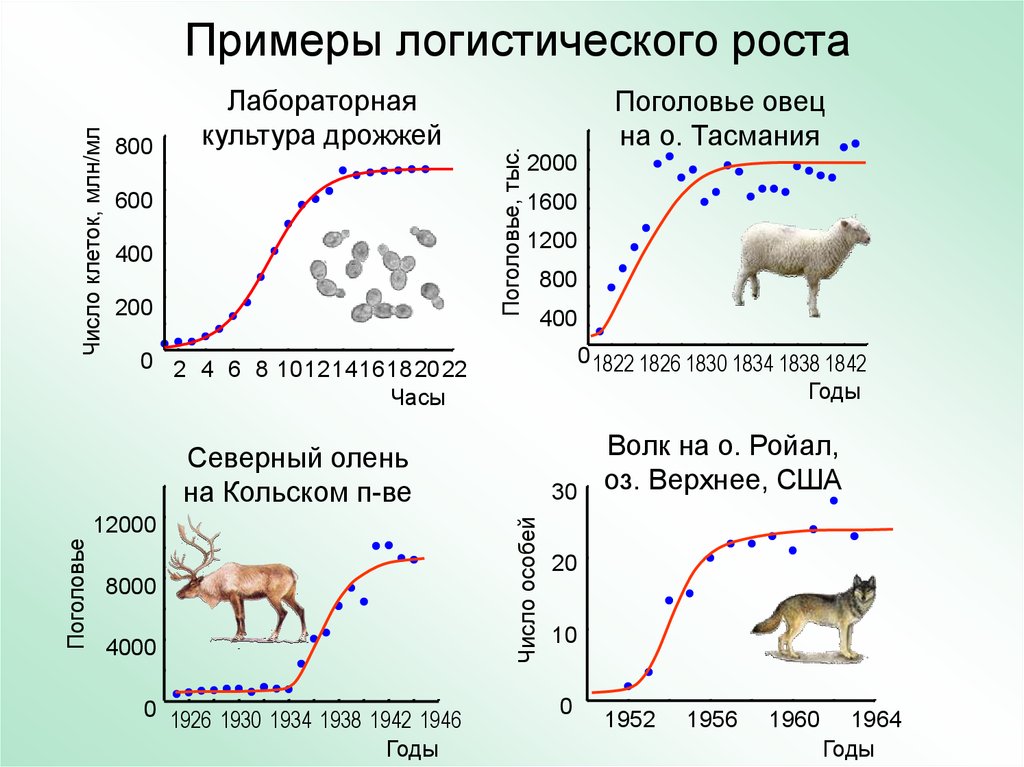 Если вам необходимо покормить своих питомцев на улице, уберите их еду через 30 минут после подачи. В противном случае то, что не съест ваш питомец, съедят грызуны. Поскольку крысы ведут ночной образ жизни, кормите своего питомца на открытом воздухе задолго до наступления темноты.
Если вам необходимо покормить своих питомцев на улице, уберите их еду через 30 минут после подачи. В противном случае то, что не съест ваш питомец, съедят грызуны. Поскольку крысы ведут ночной образ жизни, кормите своего питомца на открытом воздухе задолго до наступления темноты.
Храните мусор в контейнерах, желательно из металла, с плотно закрывающимися крышками . Никогда не оставляйте полиэтиленовые пакеты для мусора на улице. Регулярно переворачивайте компостные кучи и не компостируйте мясо, кости, молочные отходы, жиры или масла. Ежедневно убирайте собачьи фекалии со двора.
Коммерческие и сельскохозяйственные постройки
По возможности храните сыпучие продукты в защищенных от грызунов зданиях , комнатах или контейнерах. Складывайте упакованные продукты на поддоны, оставляя достаточно места вокруг и под хранящимися предметами, чтобы можно было проверить их на наличие крыс. Сливные отверстия в мусорных баках должны быть оборудованы съемной аппаратно-тканевой сеткой или же затыкаться после каждой уборки.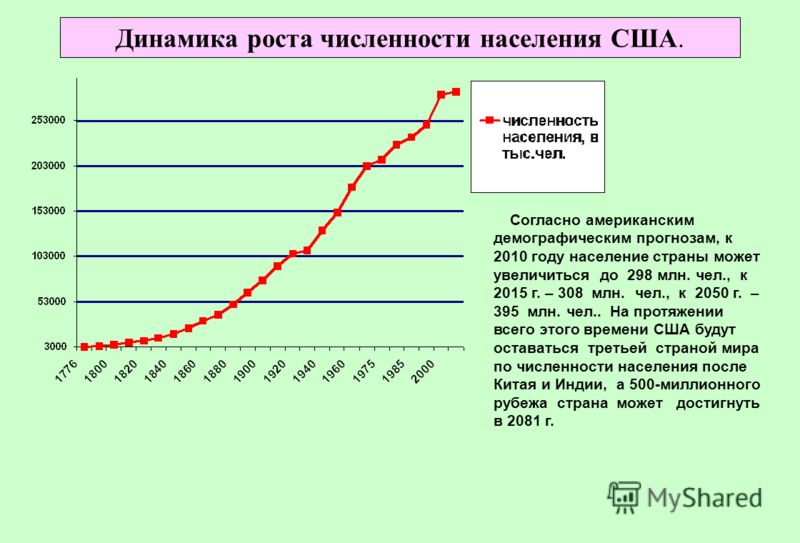
Хищники
Хотя кошки, собаки и другие хищники иногда убивают крыс, они не обеспечивают эффективной борьбы с грызунами. Они просто не могут убить крыс достаточно быстро. Крысы часто живут среди кошек и собак. Они используют еду и воду домашних животных, а иногда даже их убежище.
Ловушки
Используйте ловушки только после того, как вы предпримете все санитарные меры, описанные выше . Хотя отлов грызунов является очень важным инструментом борьбы с грызунами, он не может заменить хорошие санитарные условия. Если вы не контролируете их источники пищи и воды, грызуны будут размножаться быстрее, чем вы сможете их поймать . Отлов имеет то преимущество, что
- в нем не используются опасные пестициды;
- пользователь сразу узнает, когда ловушки сработали;
- и пойманных грызунов можно легко утилизировать до того, как они станут источником запаха, как это может произойти при отравлении (т.е. грызуны умирают в недоступных местах вокруг дома).
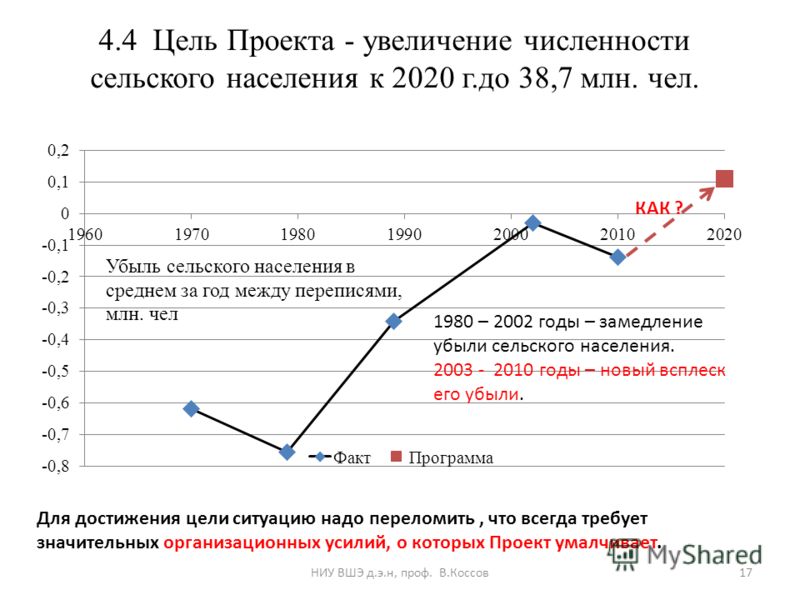
Ловушки особенно эффективны, если популяция грызунов невелика. Ловушки-защелки, клеевые доски и клетки-ловушки — все работает. Большинство ловушек можно использовать снова и снова. Ловушки на древесной основе недороги и доступны в большинстве хозяйственных магазинов. Большинство ловушек с защелкой предназначены для мышей, но доступны ловушки большего размера, разработанные специально для крыс. Купите достаточно ловушек, чтобы ваши усилия были короткими и решительными.
Ловушки не нуждаются в наживке , просто расположены там, где грызуны будут спотыкаться о спусковой крючок при обычном движении. Если вы хотите приманить ловушки, используйте очень небольшое количество арахисового масла, леденцов, сырого бекона, колбасы или ванильного экстракта (используйте ватный тампон, чтобы нанести ванильный экстракт). Что бы вы ни использовали, не нагромождайте это. Сделайте это, и вы увеличите вероятность заражения насекомыми. Вы также увеличиваете вероятность того, что грызун найдет способ убрать приманку, не будучи пойманным.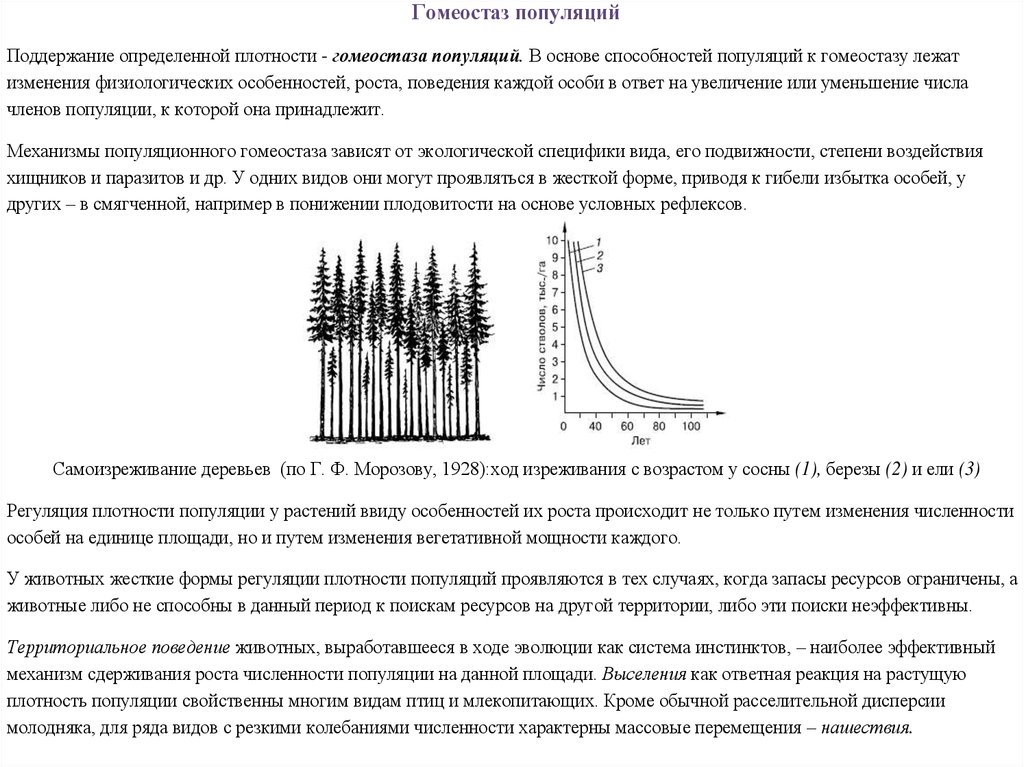 Вы также можете убить одного грызуна, но накормить нескольких других. Все, что вам действительно нужно, это запах еды. Вы также можете использовать в качестве приманки кусок ватного тампона, так как грызуны любят использовать его для строительства гнезд. Преимущество хлопка в том, что он не привлекает насекомых.
Вы также можете убить одного грызуна, но накормить нескольких других. Все, что вам действительно нужно, это запах еды. Вы также можете использовать в качестве приманки кусок ватного тампона, так как грызуны любят использовать его для строительства гнезд. Преимущество хлопка в том, что он не привлекает насекомых.
- Располагайте ловушки там, где вы обнаружите признаки активности грызунов, но желательно возле стен. Лучше всего ловушки работают под прямым углом к стене, так чтобы спусковой крючок касался стены. Это связано с тем, что грызуны предпочитают путешествовать по стенам.
- Не забывайте также держать ловушки в недоступном для домашних животных и маленьких детей месте .
- Несколько ловушек должны быть расположены в подозрительных местах. В идеале их следует перемещать в разные места каждый день, и, конечно же, их следует перемещать, если грызунов не ловят.
- Возможно, потребуется отрегулировать спусковой крючок ловушки, чтобы обеспечить легкое освобождение при касании грызуном.

- Поскольку крысы особенно пугливы ко всему новому, может оказаться необходимым оставить ловушку неустановленной до тех пор, пока приманка не будет съедена хотя бы один раз, чтобы снизить вероятность пугливости ловушки.
- Ежедневно проверяйте свои ловушки.
Другой формой ловушки является клеевая доска , имеющая липкую поверхность, которая удерживает любого грызуна, пытающегося пересечь ее. Расположите клейкие доски везде, где вы бы использовали другие ловушки, но помните, что клейкие доски настолько липкие, что они будут проблемой для любых детей, домашнего скота, домашних животных или других диких животных, которые вступят в контакт. Также имейте в виду, что пыль снижает эффективность клеевой доски. Попав на клейкую доску, мышь обычно умирает от остановки сердца. Клеевые доски со временем теряют свою эффективность, поэтому замените их, когда они перестанут быть липкими. Как и в случае с любой другой ловушкой, переместите клеевые доски в другое место, если грызуны не ловятся.
Электронные устройства
Ультразвуковые устройства излучают звуковые волны выше диапазона человеческого слуха, но их эффективность ограничена, поскольку производимые звуковые волны не могут проникать через твердые объекты, например стены. Они также быстро теряют интенсивность с расстоянием. Поскольку грызуны быстро привыкают к повторяющимся звукам, мало доказательств того, что звуковые устройства будут выгонять укоренившихся крыс или мышей из зданий . Точно так же мало доказательств того, что магнитные устройства или вибраторы оказывают какое-либо положительное влияние на грызунов.
Родентициды
Родентициды представляют собой отравленные приманки и фумиганты, используемые в основном профессионалами для борьбы с грызунами. Поскольку фумиганты представляют собой газы, высокотоксичные для человека, домашнего скота и других животных, их нельзя применять в зданиях, где люди могут подвергаться воздействию. Родентициды имеют широкий спектр активных ингредиентов.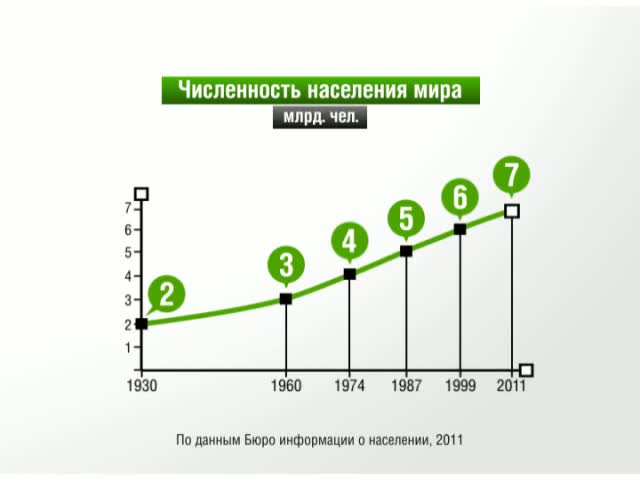 Это зарегистрированные пестициды, доступные на открытом рынке, но для их безопасного и эффективного применения требуется обучение и опыт. При неправильном применении эти пестициды могут убить или иным образом подвергнуть опасности детей, домашних или других животных , которые могут по ошибке съесть или вдохнуть их. Мы призываем вас не использовать эти материалы самостоятельно . Наймите лицензированного аппликатора пестицидов, хорошо разбирающегося в борьбе с грызунами, чтобы применить их. Иногда родентициды работают слишком хорошо. Он может убить грызуна до того, как тот выберется из дома. В этом случае у вас будут мертвые грызуны в неудобных местах, таких как чердаки, полости в стенах, подполье или за шкафами… они будут вонять в вашем доме и вызывать серьезные проблемы с насекомыми и мухами. Поскольку родентициды являются пестицидами, они также создают серьезные проблемы при хранении и утилизации.
Это зарегистрированные пестициды, доступные на открытом рынке, но для их безопасного и эффективного применения требуется обучение и опыт. При неправильном применении эти пестициды могут убить или иным образом подвергнуть опасности детей, домашних или других животных , которые могут по ошибке съесть или вдохнуть их. Мы призываем вас не использовать эти материалы самостоятельно . Наймите лицензированного аппликатора пестицидов, хорошо разбирающегося в борьбе с грызунами, чтобы применить их. Иногда родентициды работают слишком хорошо. Он может убить грызуна до того, как тот выберется из дома. В этом случае у вас будут мертвые грызуны в неудобных местах, таких как чердаки, полости в стенах, подполье или за шкафами… они будут вонять в вашем доме и вызывать серьезные проблемы с насекомыми и мухами. Поскольку родентициды являются пестицидами, они также создают серьезные проблемы при хранении и утилизации.
Утилизация грызунов и их помета
Старайтесь не прикасаться к мертвым или умирающим грызунам или их помету . Блохи на грызуне захотят сделать вас своим новым хозяином. Используйте резиновые перчатки или щипцы и утилизируйте грызунов и экскременты грызунов путем захоронения, сжигания или завернув их в полиэтиленовый пакет, прежде чем выбрасывать в плотно закрытый мусорный бак. Раненые или больные грызуны должны быть убиты (проще всего утонуть) перед тем, как избавиться от них. Сухая уборка или уборка пылесосом приведет к попаданию пыли и вирусов в воздух. Следовательно,
Блохи на грызуне захотят сделать вас своим новым хозяином. Используйте резиновые перчатки или щипцы и утилизируйте грызунов и экскременты грызунов путем захоронения, сжигания или завернув их в полиэтиленовый пакет, прежде чем выбрасывать в плотно закрытый мусорный бак. Раненые или больные грызуны должны быть убиты (проще всего утонуть) перед тем, как избавиться от них. Сухая уборка или уборка пылесосом приведет к попаданию пыли и вирусов в воздух. Следовательно,
- подметайте или пылесосьте помет грызунов только после того, как вы смочите пораженный участок водой с хлорной известью (1-2 чашки хлорной извести на каждый галлон).
- Используйте пульверизатор, чтобы нанести отбеливающую воду.
- Также обработайте те ловушки, в которые попали грызуны, и места, где грызуны были активны.
Вымойте руки с мылом и горячей водой после избавления от грызунов и экскрементов грызунов, даже если вы использовали перчатки.
Измерение успеха
Результаты нельзя измерить, просто подсчитав мертвых крыс и мышей. Заброшенные норы будут пыльными, а отверстия в них затянуты паутиной. Когда нет свежих следов или экскрементов, а живых крыс или мышей больше не видно, результаты настолько хороши, насколько можно ожидать.
Заброшенные норы будут пыльными, а отверстия в них затянуты паутиной. Когда нет свежих следов или экскрементов, а живых крыс или мышей больше не видно, результаты настолько хороши, насколько можно ожидать.
Дополнительные ресурсы
Дополнительную информацию о предотвращении заражения грызунами, заболеваниях от грызунов, уборке после грызунов и изображениях крыс и мышей можно получить на веб-сайте Центров по контролю и профилактике заболеваний (CDC).
Увеличение объема островков, но неизменное количество островков у мышей ob/ob | Диабет
Пропустить пункт назначения Nav
Исследования островков| 01 июля 2003 г.
Троэльс Бок;
Бенте Паккенберг;
Карстен Бушард
Адресуйте корреспонденцию и запросы на перепечатку Troels Bock, MD PhD, H:S Bartholin Institute, Copenhagen University Hospital, Bartholinsgade 2, DK-1399 Copenhagen K, Дания.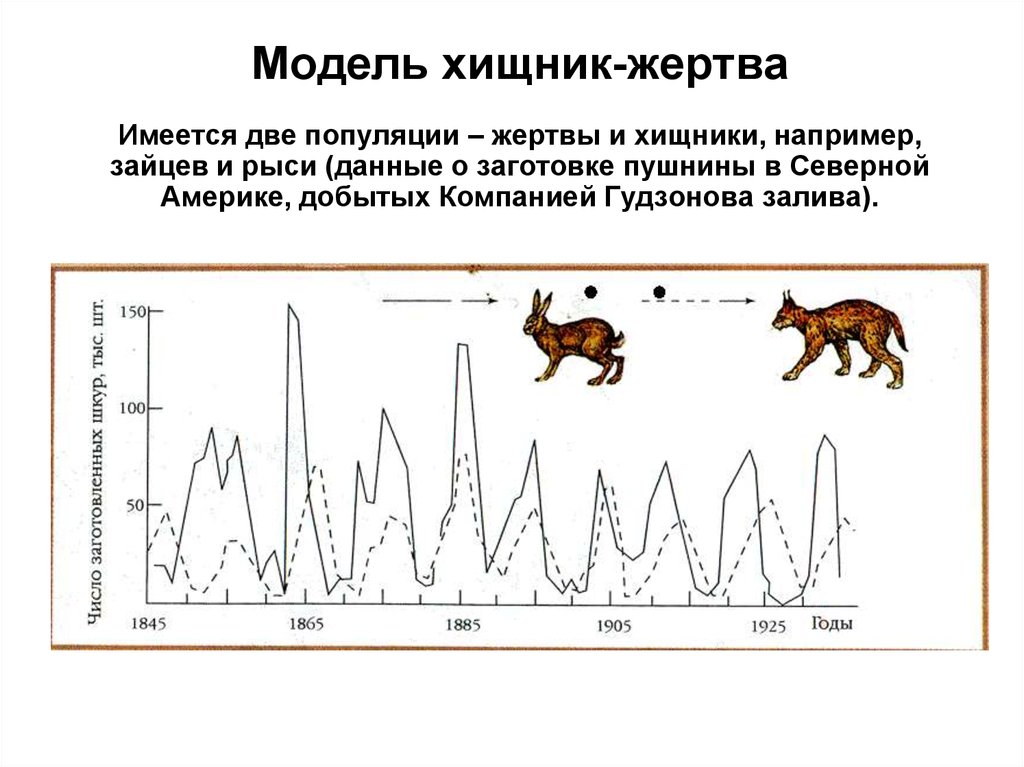 Электронная почта [email protected]
Электронная почта [email protected]
Диабет 2003;52(7):1716–1722
https://doi.org/10.2337/diabetes.52.7.1716
История статьи
Получено:
04 февраля 2003 г.
Принято:
31 марта 2003 г.
- Разделенный экран
- Просмотры
- Содержание артикула
- Рисунки и таблицы
- Видео
- Аудио
- Дополнительные данные
- Экспертная оценка
- Делиться
- MailTo
- Твиттер
Иконка Цитировать Цитировать
Получить разрешения
Citation
Троэльс Бок, Бенте Паккенберг, Карстен Бушар; Увеличение объема островков, но неизменное количество островков у мышей ob/ob . Диабет 1 июля 2003 г.; 52 (7): 1716–1722. https://doi.org/10.2337/diabetes.52.7.1716
Диабет 1 июля 2003 г.; 52 (7): 1716–1722. https://doi.org/10.2337/diabetes.52.7.1716
Скачать файл цитаты:
- Рис (Зотеро)
- Менеджер ссылок
- EasyBib
- Подставки для книг
- Менделей
- Бумаги
- КонецПримечание
- РефВоркс
- Бибтекс
Расширенный поиск
Для нашего понимания островков поджелудочной железы важно изучить, способны ли новые островки образовываться в интактной поджелудочной железе. Мы разработали новый метод для определения общего числа и среднего объема островков поджелудочной железы и использовали этот метод для изучения расширения массы островков в мышей ob/ob ( n = 8), используя мышей ob /+ ( n = 8) в качестве контроля. Общий объем островков был увеличен в 3,6 раза у мышей ob/ob по сравнению с мышами ob/ob /+, тогда как, что важно, общее количество островков не различалось у мышей ob/ob и мышей ob . /+ мышей (3193 ± 160 островков у мышей ob/ob против 3184 ± 142 островков у мышей ob/ob /+, P = 0,97). Коэффициент вариации распределения островков по объему был одинаковым в обеих группах, что свидетельствует о том, что в ob/ob , существующие островки увеличивают свой объем в той же пропорции без чистого образования новых островков. Мы предлагаем рассматривать панкреатические островки как анатомически настолько сложные структуры, что неогенез островков не происходит спонтанно в интактной поджелудочной железе. Клетки внутри существующих островков, по-видимому, являются наиболее важными источниками гиперплазии островковых клеток во время увеличения общей массы островков.
/+ мышей (3193 ± 160 островков у мышей ob/ob против 3184 ± 142 островков у мышей ob/ob /+, P = 0,97). Коэффициент вариации распределения островков по объему был одинаковым в обеих группах, что свидетельствует о том, что в ob/ob , существующие островки увеличивают свой объем в той же пропорции без чистого образования новых островков. Мы предлагаем рассматривать панкреатические островки как анатомически настолько сложные структуры, что неогенез островков не происходит спонтанно в интактной поджелудочной железе. Клетки внутри существующих островков, по-видимому, являются наиболее важными источниками гиперплазии островковых клеток во время увеличения общей массы островков.
Фундаментальным и до сих пор оставшимся без ответа вопросом в понимании патогенеза диабета 2 типа является ограничение образования достаточного количества дополнительных β-клеток для поддержания нормогликемии при повышенной потребности в инсулине; даже у людей со значительной резистентностью к инсулину не развивается диабет, если у них есть соответствующее количество функционирующих β-клеток, что подчеркивает патофизиологическое значение общей массы β-клеток.
Мышь ob/ob широко изучалась в качестве модели диабета 2 типа (1). Эти мыши страдают ожирением, у них развивается резистентность к инсулину и диабет из-за наследственной неспособности вырабатывать лептин (2), несмотря на заметное увеличение общей массы панкреатических островков. В литературе утверждается, что как гиперплазия островков, так и гипертрофия островков ответственны за увеличение общей массы островков у мышей ob/ob (3,4), но среди немногих исследований, которые действительно рассматривали этот вопрос с применением методов который теоретически мог бы измерить общее количество островков (5,6), на самом деле результаты расходятся. Ранее мы обнаружили линейную корреляцию между общим объемом островков и средним объемом, взвешенным по объему, у крыс (7). масса при физиологическом росте у крыс обусловлена ростом существующих островков без образования новых островков. Поэтому мы разработали метод, основанный на последних стереологических методах, для определения общего числа и среднего объема островков поджелудочной железы, и мы использовали этот метод для исследования расширения массы островков в ob/ob мышей. Понимание того, способны ли новые островки образовываться в интактной поджелудочной железе, важно для понимания островков как анатомической структуры, и, кроме того, это может быть важно для понимания того, какие клетки в поджелудочной железе важны для расширения всего островка. масса во время физиологических или патологических состояний.
Понимание того, способны ли новые островки образовываться в интактной поджелудочной железе, важно для понимания островков как анатомической структуры, и, кроме того, это может быть важно для понимания того, какие клетки в поджелудочной железе важны для расширения всего островка. масса во время физиологических или патологических состояний.
Животные.
Были приобретены восемь самцов мышей C57BL/6JBom- ob/ob и восемь самцов мышей C57BL/6Jbom- ob /+ (M&B, Ry, Дания). Всем мышам было 8 недель. Уровень глюкозы в крови натощак измеряли с помощью глюкометра Elite (Bayer, Леверкузен, Германия) до того, как мышей умерщвляли путем смещения шейных позвонков. Поджелудочную железу немедленно извлекали и фиксировали в 10% забуференном формалине, рН 7,4.
Гистология и забор срезов.
Каждую поджелудочную железу заливали парафином и тщательно разделяли на срезы толщиной 5 мкм. Рисунок 1 иллюстрирует выборку разделов.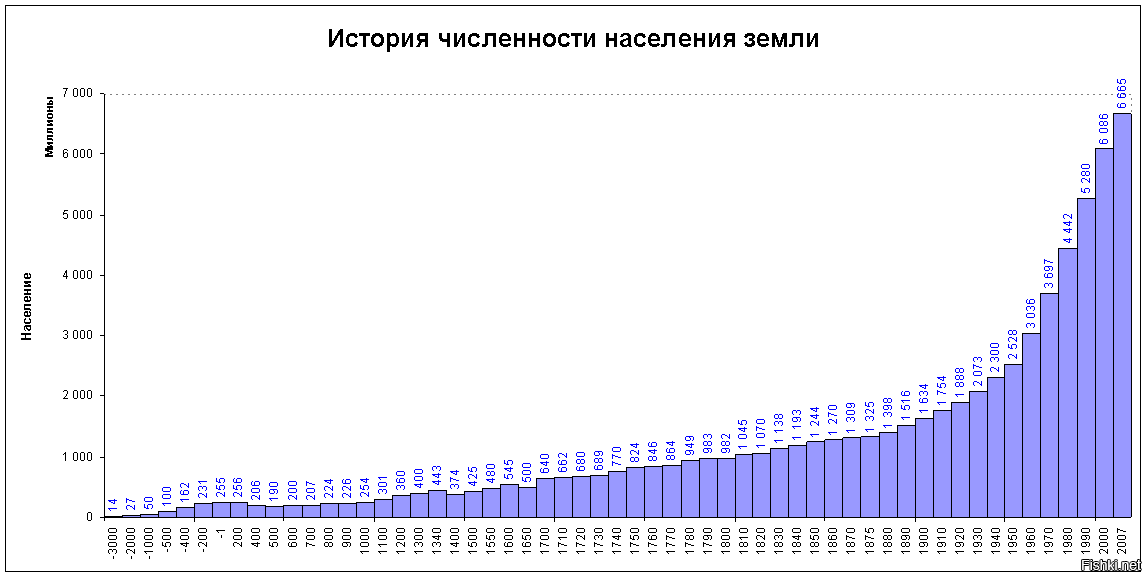 При случайном начале между первыми 50 секциями отбиралась каждая 50-я секция (первичные секции). Кроме того, для каждого отобранного первичного раздела в качестве эталонного раздела отбирался раздел, расположенный на два впереди. Поскольку каждый срез имел толщину 5 мкм, отсюда следует, что между первичными срезами было 250 мкм и 10 мкм между основным срезом и соответствующим эталонным участком. Все первичные и эталонные срезы окрашивали гематоксилином и эозином (H&E). Для четырех поджелудочных желез в каждой группе дополнительный набор систематически отобранных срезов окрашивали на инсулин путем инкубации с первичными антителами морской свинки к свиному инсулину (разведение 1:50; Dako, Glostrup, Дания) с последующей инкубацией с Envision-AP. (Dako), а затем визуализировали с помощью системы Sigma-FAST Fast Red (Sigma, Vallensbaek, Дания) и контрастировали гематоксилином.
При случайном начале между первыми 50 секциями отбиралась каждая 50-я секция (первичные секции). Кроме того, для каждого отобранного первичного раздела в качестве эталонного раздела отбирался раздел, расположенный на два впереди. Поскольку каждый срез имел толщину 5 мкм, отсюда следует, что между первичными срезами было 250 мкм и 10 мкм между основным срезом и соответствующим эталонным участком. Все первичные и эталонные срезы окрашивали гематоксилином и эозином (H&E). Для четырех поджелудочных желез в каждой группе дополнительный набор систематически отобранных срезов окрашивали на инсулин путем инкубации с первичными антителами морской свинки к свиному инсулину (разведение 1:50; Dako, Glostrup, Дания) с последующей инкубацией с Envision-AP. (Dako), а затем визуализировали с помощью системы Sigma-FAST Fast Red (Sigma, Vallensbaek, Дания) и контрастировали гематоксилином.
Микроскопы и оборудование.
Срезы исследовали с помощью микроскопа Leica DMLB (Leica, Glostrup, Дания), оснащенного выступающим рычагом для проецирования изображения на стол.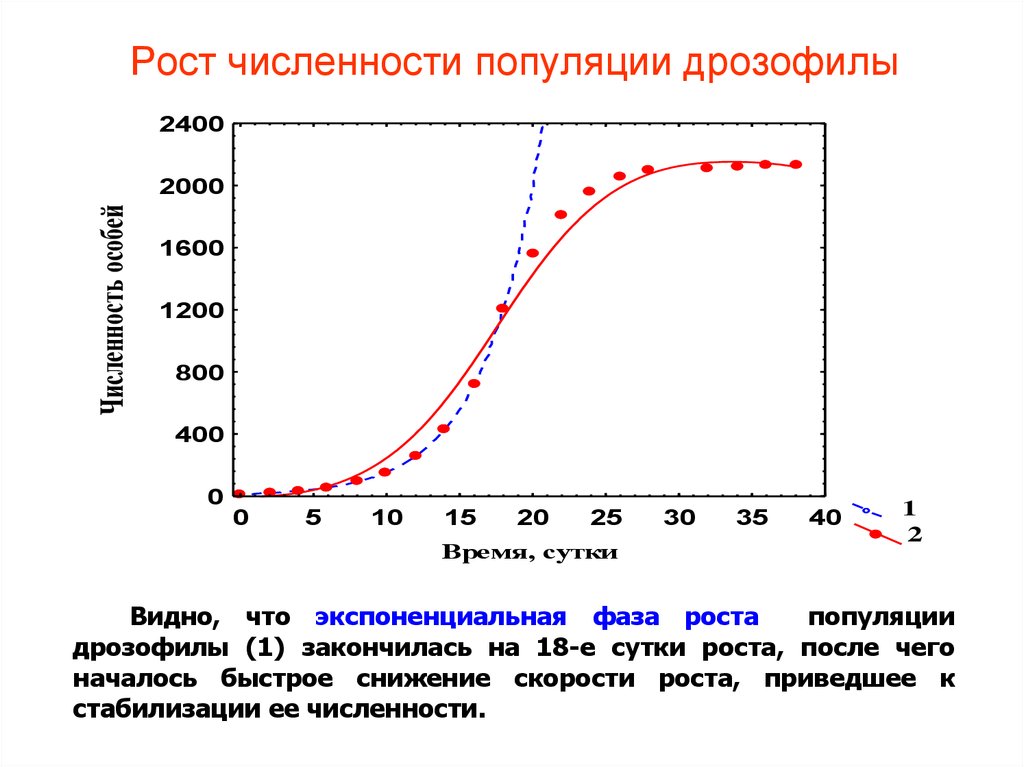 Систематическая равномерная случайная выборка в пределах среза была обеспечена с помощью предметного столика микроскопа ECO-Drive (Märzhäuser Wetzlar, Wetzlar, Германия), управляемого компьютером с программным обеспечением WIN-Commander 4.1.3.0 (Märzhäuser). Накладные зонды, используемые для стереологических исследований (сетка для подсчета точек или рамка для подсчета, как описано ниже), закрепляли на столе таким образом, чтобы микроскоп проецировал изображение на сетку. Для подсчета общего числа островков использовали дополнительный идентичный микроскоп с выступающим плечом, но с ручным предметным столиком.
Систематическая равномерная случайная выборка в пределах среза была обеспечена с помощью предметного столика микроскопа ECO-Drive (Märzhäuser Wetzlar, Wetzlar, Германия), управляемого компьютером с программным обеспечением WIN-Commander 4.1.3.0 (Märzhäuser). Накладные зонды, используемые для стереологических исследований (сетка для подсчета точек или рамка для подсчета, как описано ниже), закрепляли на столе таким образом, чтобы микроскоп проецировал изображение на сетку. Для подсчета общего числа островков использовали дополнительный идентичный микроскоп с выступающим плечом, но с ручным предметным столиком.
Суммарные объемы островков и поджелудочной железы.
Используя длину шага 900 мкм в направлении x (Δ x ) и 700 мкм в направлении y (Δ y ), все первичные срезы каждой поджелудочной железы систематически исследовали, как показано на рисунке. на рис. 2. Нанесена точечная сетка из 99 точек, 1 из них обведена кружком. Проходя через все первичные срезы поджелудочной железы, как показано на рис. 2, мы подсчитывали, сколько раз 1 из 99 точек попадала в островок. Островок определяли как скопление клеток с минимум тремя видимыми ядрами, демонстрирующими нормальные характеристики островковых эндокринных клеток (бледная цитоплазма с приблизительно сферическими ядрами). Параллельно подсчитывали, сколько раз точка, обведенная кружком, попадала в ткань поджелудочной железы (экзокринную ткань поджелудочной железы, протоки, сосуды, островки и т. д.). Затем были рассчитаны значения общего объема поджелудочной железы и островков Лангерганса на основе принципа Кавальери (8): 9{3}{\times}{\sum}\mathrm{P}(\mathrm{pan})\]
Проходя через все первичные срезы поджелудочной железы, как показано на рис. 2, мы подсчитывали, сколько раз 1 из 99 точек попадала в островок. Островок определяли как скопление клеток с минимум тремя видимыми ядрами, демонстрирующими нормальные характеристики островковых эндокринных клеток (бледная цитоплазма с приблизительно сферическими ядрами). Параллельно подсчитывали, сколько раз точка, обведенная кружком, попадала в ткань поджелудочной железы (экзокринную ткань поджелудочной железы, протоки, сосуды, островки и т. д.). Затем были рассчитаны значения общего объема поджелудочной железы и островков Лангерганса на основе принципа Кавальери (8): 9{3}{\times}{\sum}\mathrm{P}(\mathrm{pan})\]
, где V(pan) — общий объем поджелудочной железы, a/p(pan) — площадь на точку (в данном случае Δ x × Δ y , поскольку для подсчета точек, поражающих поджелудочную железу, использовалась только одна точка сетки), N sect (pp) — количество секций между первичными секциями (50 секций в в данном случае), T sect — толщина среза (5 мкм), а ΣP(pan) — общее количество точек, попавших в поджелудочную железу.
\[\ mathrm {V} (\ mathrm {isl}) {=} \ mathrm {a}/\ mathrm {p} (\ mathrm {isl}) {\ times} \ mathrm {N} _ {\ mathrm {секта}} (\ mathrm {p} {-} \ mathrm {p}) {\ times} \ mathrm {T} _ {\ mathrm {секта}} {\ times} {\ sum} \ mathrm {P} ( \mathrm{isl}){=}1,59{3}{\times}{\sum}\mathrm{P}(\mathrm{isl})\]
где V(isl) — общий объем островков, a/p(isl) — площадь на точку (в данном случае Δ x × Δ y /99, потому что в сетке использовалось 99 точек для подсчета точек, попадающих в островки), а ΣP(isl) — общее количество точек, попадающих в островки.
Средневзвешенный объем островков.
Для каждой точки, которая попала в островок, мы также измерили расстояние в горизонтальном направлении между точками пересечения горизонтальной линии, проходящей через точку и островок. Подробное теоретическое и практическое описание взвешенного по объему среднего объема островков как стереологического параметра было опубликовано ранее (7). Вкратце, средний объем островков, взвешенный по объему, представляет собой средний объем, если островки взвешены пропорционально их объему. Если все островки не имеют одинаковых объемов, тогда средневзвешенный по объему объем островков выше, чем средневзвешенный объем островков («обычный» средний объем островков). Затем средний объем островков, взвешенный по объему, можно рассчитать в соответствии с: 9{3}}\]
Вкратце, средний объем островков, взвешенный по объему, представляет собой средний объем, если островки взвешены пропорционально их объему. Если все островки не имеют одинаковых объемов, тогда средневзвешенный по объему объем островков выше, чем средневзвешенный объем островков («обычный» средний объем островков). Затем средний объем островков, взвешенный по объему, можно рассчитать в соответствии с: 9{3}}\]
, где v v — взвешенный по объему средний объем островка, а l 0 — длина линии между двумя пересечениями островка и горизонтальной линией, проходящей через точку, пересекающую островок.
Общее количество островков.
В другом сеансе выборка в первичных секциях была выполнена, как описано выше и изображено на рис. 2, но теперь к таблице была прикреплена несмещенная рамка подсчета (внизу слева на рис. 2). Правила счетной рамки определяют объекты полностью вне рамки или объекты, которые касаются линий исключения (сплошные линии на рисунке), как находящиеся вне рамки, тогда как объекты, которые полностью находятся внутри рамки или касаются только линий включения (штриховые линии). линии на рисунке) определяются как находящиеся внутри рамки. Мы применили дисекторный принцип (9) для подсчета островков, как показано на рис. 3. Всякий раз, когда профиль островков отбирался счетной рамкой, соответствующее положение в эталонном срезе определялось с помощью другого микроскопа, и мы определяли, был ли островок также виден в эталонном срезе. . Островок считали, если он появлялся в основном отделе, но не в контрольном отделе (островок С на рис. 3). Поскольку выборка секций, а также внутрисекционная выборка выполнялись с известными фракциями выборки, общее количество островков может быть рассчитано по принципу фракционирования (10) из: 9{{-}}(\mathrm{isl})\]
линии на рисунке) определяются как находящиеся внутри рамки. Мы применили дисекторный принцип (9) для подсчета островков, как показано на рис. 3. Всякий раз, когда профиль островков отбирался счетной рамкой, соответствующее положение в эталонном срезе определялось с помощью другого микроскопа, и мы определяли, был ли островок также виден в эталонном срезе. . Островок считали, если он появлялся в основном отделе, но не в контрольном отделе (островок С на рис. 3). Поскольку выборка секций, а также внутрисекционная выборка выполнялись с известными фракциями выборки, общее количество островков может быть рассчитано по принципу фракционирования (10) из: 9{{-}}(\mathrm{isl})\]
где N(isl) — общее количество островков в поджелудочной железе, N sect (p-p) — количество секций между первичными секциями, N sect (p-r) — количество отрезков между основным отрезком и соответствующим эталонным отрезком (в данном случае два), Δ x и Δ y — длины шагов, A(frame) — площадь счетного кадр с поправкой на увеличение (450 736 мкм 2 ), а ΣQ — (исл) — общее количество островков, подсчитанных в одной поджелудочной железе. 9{{-}}(\mathrm{isl})}\]
9{{-}}(\mathrm{isl})}\]
, где v N (isl) — средний объем островка (индекс N должен подчеркнуть, что это «обычный» или средневзвешенный объем ), а остальные сокращения описаны в пунктах выше.
Изменение распределения островков по объему.
Зная как средневзвешенный объем островков, так и средний объем островков, взвешенный по объему, можно рассчитать коэффициент вариации (стандартное отклонение, деленное на среднее) объемного распределения островков поджелудочной железы без предположений о типе распределение (7) по:
\[\mathrm{CV}_{\mathrm{N}}(\mathrm{isl}){=}\sqrt{\frac{\mathrm{v}_{\mathrm{V}}(\mathrm{ isl})}{\mathrm{v}_{N}(\mathrm{isl})}{-}1}\]
, где CV N (isl) — коэффициент вариации распределения объемов островков .
Количество профилей островков на площадь поджелудочной железы и средняя площадь островков.
При исследовании срезов с помощью счетной рамки, прикрепленной к столу, мы также подсчитывали количество профилей островков, отобранных в счетных рамках (островки B, C и D на рис. {2}{\times}\ \\frac{{\sum}\mathrm{P}(\mathrm{isl} )}{{\sum}\mathrm{N}_{\mathrm{prf}}(\mathrm{isl})}\]
{2}{\times}\ \\frac{{\sum}\mathrm{P}(\mathrm{isl} )}{{\sum}\mathrm{N}_{\mathrm{prf}}(\mathrm{isl})}\]
, где prf (isl) — средняя площадь профиля островка, а остальные коэффициенты определены в предыдущих параграфах.
В некоторых предыдущих исследованиях количество профилей островков на площадь поджелудочной железы рассматривалось как показатель общего числа островков, и параллельно средняя площадь профиля островков рассматривалась как показатель среднего объема островков. . Как показано ниже, ни один из этих подходов не может быть подтвержден теоретически. В предыдущей публикации (7) мы показали, что количество профилей островков на площадь поджелудочной железы и среднюю площадь островков можно, используя формулу, первоначально данную Аберкромби (11), выразить как:
\[\ mathrm {N} _ {\ mathrm {prf, A}} (\ mathrm {isl, pan}) {=} \ \ frac {\ mathrm {N} (\ mathrm {isl}) {\ times } (\ mathrm {h} {+} \ mathrm {T} _ {\ mathrm {секта}})} {\ mathrm {v} (\ mathrm {pan})} \]
\[\ mathrm {a} _ {\ mathrm {prf}} (\ mathrm {isl}) {=} \ \ frac {\ mathrm {v} _ {\ mathrm {N}} (\ mathrm {isl})} {(\ mathrm {h} {+}\mathrm{T}_{\mathrm{sect}}}}\]
, где N prf,A (isl,pan) — количество профилей островков на площадь поджелудочной железы, N(isl) — общее количество островков в поджелудочной железе, h — средняя протяженность островков, измеренная перпендикулярно направлению разреза (средняя высота островков), T sect — толщина среза, V(pan) — общий объем поджелудочной железы, a prf (isl) — средняя площадь профиля островка, а v N (isl) — средний объем островка.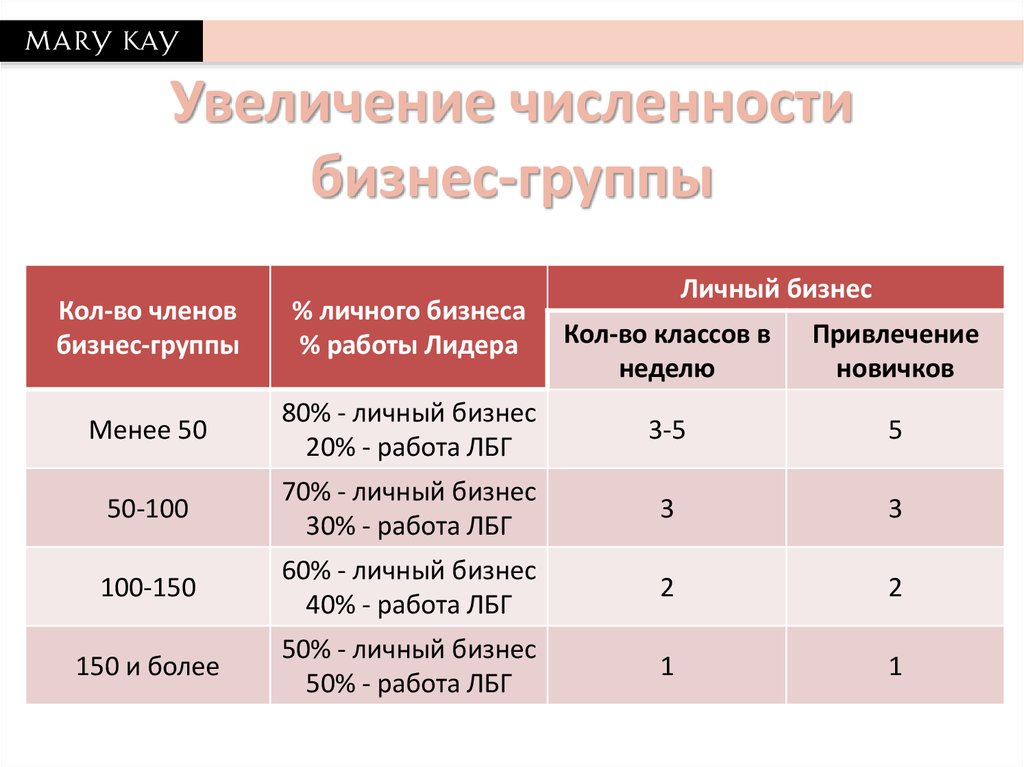
Уравнение 9 показывает, что количество профилей на площадь поджелудочной железы в одном или нескольких срезах не является надежным отражением изменений общего числа островков, поскольку оно, помимо общего числа островков, также зависит от объема поджелудочной железы, средняя высота островков и толщина среза. Как видно из уравнения 10, средняя площадь профиля островков прямо пропорциональна среднему объему островков, но обратно пропорциональна сумме средней высоты островков и толщины среза. Это дисквалифицирует этот параметр как надежный отражатель абсолютного значения или изменений среднего объема островков. Тем не менее, чтобы можно было сравнить выводы, сделанные с использованием теоретически подтвержденного набора стереологических методов, описанных выше, и выводы, которые были бы сделаны, если бы выводы были основаны на измерении количества профилей на площадь поджелудочной железы и средней площади островков. , мы также измерили последние два параметра в этом исследовании.
Последствие игнорирования отдельных эндокринных клеток.
Сколько эндокринных клеток поджелудочной железы должно быть сгруппировано вместе, прежде чем термин «островок Лангерганса» будет уместным, еще не определено и не имеет значения с клинической точки зрения. В этом исследовании мы использовали окрашивание H&E для идентификации островков и определили профиль островков как скопление эндокринных клеток по крайней мере с тремя видимыми ядрами. Чтобы получить представление о доле β-клеток, проигнорированной из-за выбора метода окрашивания, мы использовали набор окрашенных на инсулин срезов из четырех ob/ob и четыре мыши ob /+. Используя сетку подсчета точек с 99 точками и выборку, как описано выше, мы подсчитали количество точек, которые поражают β-клетки внутри островков в соответствии с определением, используемым для срезов, окрашенных гематоксилин-эозином, и мы подсчитывали количество точек, которые поражают β-клетки. -клетки, не входящие в кластеры, определяемые как островки. Для мышей ob/ob средняя доля точек, поражающих β-клетки вне островков, составила 1,3%, тогда как соответствующее значение для 9 мышей0120 ob /+ мышей составляла 1,7%, что свидетельствует о том, что β-клетки, не учитываемые в измеренных параметрах в этом исследовании, представляют собой очень небольшую долю от общего объема островков.
-клетки, не входящие в кластеры, определяемые как островки. Для мышей ob/ob средняя доля точек, поражающих β-клетки вне островков, составила 1,3%, тогда как соответствующее значение для 9 мышей0120 ob /+ мышей составляла 1,7%, что свидетельствует о том, что β-клетки, не учитываемые в измеренных параметрах в этом исследовании, представляют собой очень небольшую долю от общего объема островков.
Статистика.
Данные на рисунках представлены как среднее значение ± стандартная ошибка. Результаты мышей ob/ob и мышей ob /+ сравнивали с помощью теста Стьюдента t . Все значения P являются двусторонними, и уровень значимости был установлен на P <0,05.
Как и ожидалось, средняя масса тела и средний уровень глюкозы в крови были значительно выше у мышей ob/ob по сравнению с мышами ob/ob /+ (рис. 4А и В), тогда как общий объем поджелудочной железы (рис.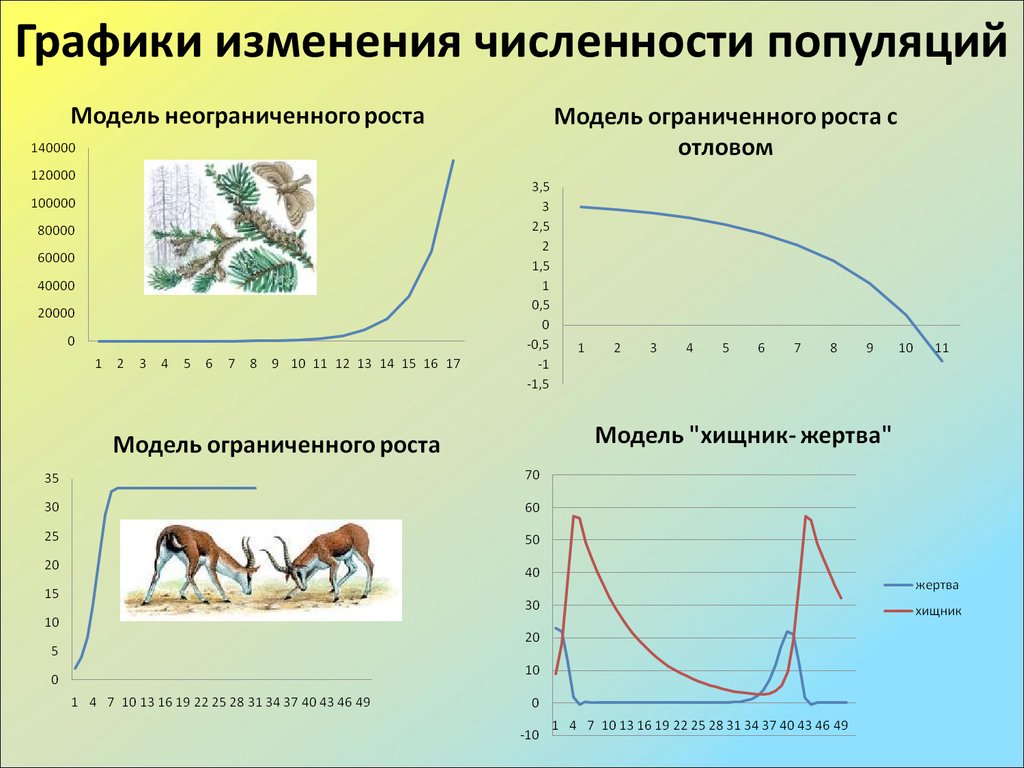 4С) был равен в двух группах. Общий объем островков (рис. 4D) был в 3,67 раза выше у мышей ob/ob (2,09 ± 0,19 мм 3 у мышей ob/ob против 0,57 ± 0,03 мм 3 у мышей ob /+). мыши, P < 10 -5 ). Как видно из рис. 4Е, общее количество островков было поразительно одинаковым в двух группах (3,193 ± 160 у мышей ob/ob и 3184 ± 142 у мышей ob/ob /+, P = 0,97), а 95% ДИ варьировал от +468 до -450 островков у мышей ob/ob по сравнению с мышами ob /+. Обычный средний объем островков (рис. 4F) составил 6,57 ± 0,52 × 10 5 мкм 3 у ob/ob мышей против 1,81 ± 0,12 × 10 5 мкм / 3 у мышей ob мыши ( P < 10 -6 ). Так, выраженное увеличение общего объема островков в ob/ob мышей была вызвана исключительно гипертрофией островков без участия чистого образования новых островков.
4С) был равен в двух группах. Общий объем островков (рис. 4D) был в 3,67 раза выше у мышей ob/ob (2,09 ± 0,19 мм 3 у мышей ob/ob против 0,57 ± 0,03 мм 3 у мышей ob /+). мыши, P < 10 -5 ). Как видно из рис. 4Е, общее количество островков было поразительно одинаковым в двух группах (3,193 ± 160 у мышей ob/ob и 3184 ± 142 у мышей ob/ob /+, P = 0,97), а 95% ДИ варьировал от +468 до -450 островков у мышей ob/ob по сравнению с мышами ob /+. Обычный средний объем островков (рис. 4F) составил 6,57 ± 0,52 × 10 5 мкм 3 у ob/ob мышей против 1,81 ± 0,12 × 10 5 мкм / 3 у мышей ob мыши ( P < 10 -6 ). Так, выраженное увеличение общего объема островков в ob/ob мышей была вызвана исключительно гипертрофией островков без участия чистого образования новых островков.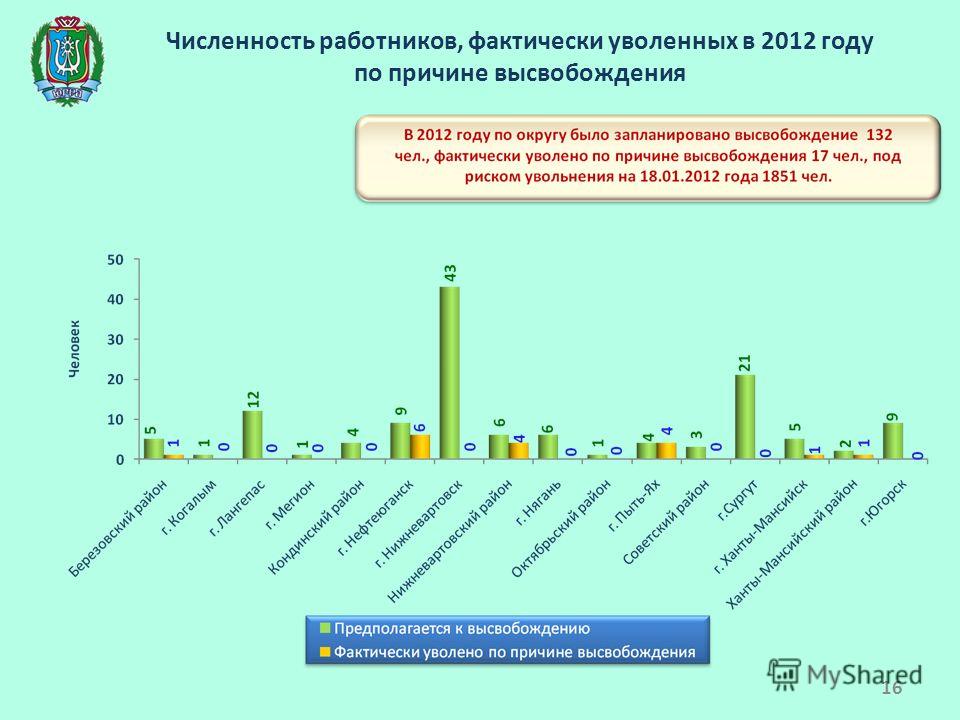
Средневзвешенный объем островков (рис. 4G) составлял 2,00 ± 0,25 × 10 7 мкм 3 у мышей ob/ob против 0,52 ± 0,05 × 10 дюймов 7 5 7 мкм 5 ob /+ мышей ( P < 10 -4 ). Другими словами, взвешенный по объему средний объем островков и средневзвешенный по количеству объем островков были увеличены в ob/ob мышей примерно на тот же коэффициент (3,88 для объемно-взвешенного среднего объема островков и 3,63 для среднечисленного средневзвешенного объема островков). Как следствие (уравнение 6), коэффициент вариации в распределении объемов островков (рис. 4H) был сходным в двух группах (5,39 ± 0,29 у мышей ob/ob против 5,27 ± 0,29 у мышей ob ). /+ мыши, P = 0,76). Это показывает, что не только количество островков не изменилось у мышей ob/ob , но и форма распределения объемов островков, по-видимому, идентична в двух группах. Таким образом, стереологическое исследование показало, что увеличенный общий объем островков, обнаруженный в 9Мыши 0120 ob/ob были результатом гипертрофии островков без заметного вклада гиперплазии островков, и гипертрофию островков можно было бы объяснить, как если бы теоретически все островки увеличивали свой объем на один и тот же фактор.
Число островков на площадь поджелудочной железы (рис. 5А) составило 1,52 ± 0,10 мм -1 у мышей ob/ob и 0,82 ± 0,04 мм -1 у мышей ob /+ ( P < 10 -4 ), тогда как средняя площадь островков (рис. 5В) составила 1,18 ± 0,07 × 10 4 мкм 2 у мышей ob/ob против 0,64 ± 0,04 × 10 4 мкм 2 у мышей ob /+ ( 605 5 6 < P 0 ). Если бы количество островков на площадь поджелудочной железы и средняя площадь островков интерпретировались как надежные параметры общего числа островков и среднего объема островков соответственно, то (ошибочный) вывод состоял бы в том, что гиперплазия и гипертрофия островков вносят примерно равный вклад. к увеличению общего объема островков, потому что количество островков на площадь поджелудочной железы и средняя площадь островков увеличились примерно в один и тот же раз (1,85 для числа островков на площадь поджелудочной железы и 1,84 для средней площади островков) в 9Мыши 0120 ob/ob по сравнению с мышами ob/ob /+.
На основе стереологических методов, таких как фракционная выборка и подсчет диссекторов (методы, основанные на принципах современной стереологии, основанной на проверенных математических и статистических принципах), мы обнаружили заметное увеличение общего объема островков в ob/ob мышей по сравнению с ob /+ мышами, увеличение, которое было полностью вызвано гипертрофией островков, тогда как общее количество островков было одинаковым в двух группах с достаточно узким доверительным интервалом для различия средних значений.
При определении островка как группы эндокринных клеток, содержащих по крайней мере три видимых ядра, мы обнаружили, что окрашивание H&E предпочтительнее, поскольку 1 ) оно позволяет однозначно идентифицировать островки; 2 ) легко воспроизводим, дает одинаковую интенсивность окрашивания на всех срезах; и 3 ) внешний вид островковых клеток при окрашивании гематоксилин-эозином одинаков у животных с диабетом и без него.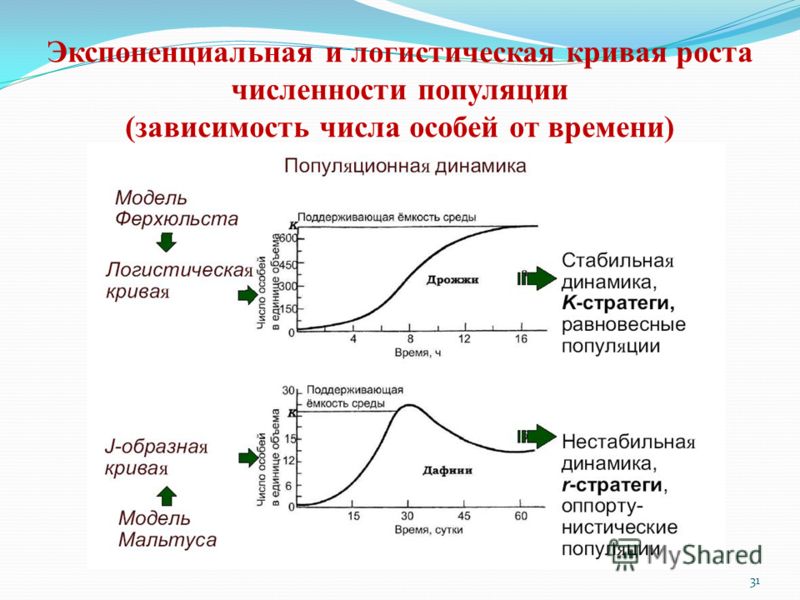 Альтернативой может быть использование иммунохимически окрашенных срезов, то есть использование коктейля первичных антител, направленных против островковых гормонов. По сравнению с окрашиванием гематоксилин-эозином это теоретически позволяет установить определение островка только на одной или нескольких эндокринных клетках. С другой стороны, недостатком иммунохимического окрашивания является то, что β-клетки, наиболее часто встречающийся тип клеток в островках, постепенно дегранулируются по мере прогрессирования диабетического состояния, что делает этот подход чувствительным к, по крайней мере, теоретической возможности того, что единичные или небольшие кластеры β-клеток могут не попасть в пробу в поджелудочной железе из ob/ob мышей. Таким образом, хотя как иммунохимическое, так и физико-химическое окрашивание имеют свои преимущества и недостатки, мы посчитали последнее наиболее надежным для методов, применяемых при сравнении лиц с диабетом и без него.
Альтернативой может быть использование иммунохимически окрашенных срезов, то есть использование коктейля первичных антител, направленных против островковых гормонов. По сравнению с окрашиванием гематоксилин-эозином это теоретически позволяет установить определение островка только на одной или нескольких эндокринных клетках. С другой стороны, недостатком иммунохимического окрашивания является то, что β-клетки, наиболее часто встречающийся тип клеток в островках, постепенно дегранулируются по мере прогрессирования диабетического состояния, что делает этот подход чувствительным к, по крайней мере, теоретической возможности того, что единичные или небольшие кластеры β-клеток могут не попасть в пробу в поджелудочной железе из ob/ob мышей. Таким образом, хотя как иммунохимическое, так и физико-химическое окрашивание имеют свои преимущества и недостатки, мы посчитали последнее наиболее надежным для методов, применяемых при сравнении лиц с диабетом и без него.
В этом исследовании мы обнаружили очень значительное увеличение числа профилей островков на площадь поджелудочной железы у мышей ob/ob .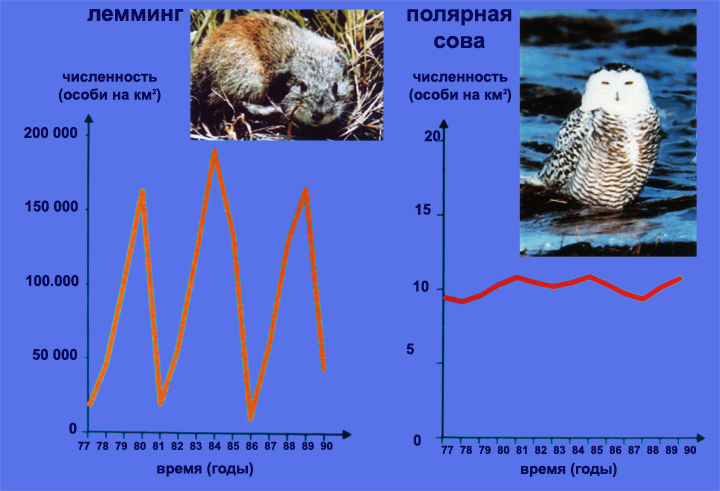 Этот результат, однако, не противоречит обнаружению неизменного общего числа островков, и это действительно то, чего следует ожидать, поскольку средняя высота островков (h в уравнении 9) увеличивается с увеличением среднего объема островков. Конфликт возникает только в том случае, если увеличенное количество профилей островков на площадь поджелудочной железы приводит к выводу, что общее число островков увеличено, что, как описано, было бы необоснованным заключением. Мы обнаружили, что средняя площадь островков у мышей ob/ob увеличилась в 1,8 раза, тогда как средний объем островков увеличился в 3,6 раза. Таким образом, если бы вывод об увеличении среднего объема островков был основан на измерении средней площади профиля островков, этот вывод был бы правильным в том смысле, что средний объем островков действительно увеличился, хотя впечатление о величине увеличения было бы неправильный.
Этот результат, однако, не противоречит обнаружению неизменного общего числа островков, и это действительно то, чего следует ожидать, поскольку средняя высота островков (h в уравнении 9) увеличивается с увеличением среднего объема островков. Конфликт возникает только в том случае, если увеличенное количество профилей островков на площадь поджелудочной железы приводит к выводу, что общее число островков увеличено, что, как описано, было бы необоснованным заключением. Мы обнаружили, что средняя площадь островков у мышей ob/ob увеличилась в 1,8 раза, тогда как средний объем островков увеличился в 3,6 раза. Таким образом, если бы вывод об увеличении среднего объема островков был основан на измерении средней площади профиля островков, этот вывод был бы правильным в том смысле, что средний объем островков действительно увеличился, хотя впечатление о величине увеличения было бы неправильный.
В литературе указано, что у мышей ob/ob увеличивается как количество, так и размер островков (3,4), со ссылками на более ранние публикации таких авторов, как Bleisch et al. (12), Хеллман и др. (5), а Гептс и соавт. (6). Блейш и др. (12) использовали количество островков на площадь поджелудочной железы и среднюю площадь островков, чтобы сделать вывод, что островки у мышей линии ob/ob были более многочисленными и большими по сравнению с нормальными швейцарскими мышами. Критическое обсуждение этих методов дано выше. Хеллман и др. (5) и Гептс и соавт. (6) оба использовали метод, описанный Wicksell (13,14), который основан на предположении о сферической или эллипсоидальной трехмерной форме островков. В то время, когда проводились эти исследования, этот метод был современным, но теперь он был вытеснен последними достижениями в области стереологии. Хеллман и др. (5) был сосредоточен в первую очередь на распределении островков по размерам (что имеет смысл, поскольку именно в этом заключается сила метода, основанного на Викселле), а общее количество островков не рассчитывалось. Однако из данных, приведенных в статье, ясно, что расчет общего количества островков привел бы к увеличению числа островков в ob/ob мышей.
(12), Хеллман и др. (5), а Гептс и соавт. (6). Блейш и др. (12) использовали количество островков на площадь поджелудочной железы и среднюю площадь островков, чтобы сделать вывод, что островки у мышей линии ob/ob были более многочисленными и большими по сравнению с нормальными швейцарскими мышами. Критическое обсуждение этих методов дано выше. Хеллман и др. (5) и Гептс и соавт. (6) оба использовали метод, описанный Wicksell (13,14), который основан на предположении о сферической или эллипсоидальной трехмерной форме островков. В то время, когда проводились эти исследования, этот метод был современным, но теперь он был вытеснен последними достижениями в области стереологии. Хеллман и др. (5) был сосредоточен в первую очередь на распределении островков по размерам (что имеет смысл, поскольку именно в этом заключается сила метода, основанного на Викселле), а общее количество островков не рассчитывалось. Однако из данных, приведенных в статье, ясно, что расчет общего количества островков привел бы к увеличению числа островков в ob/ob мышей.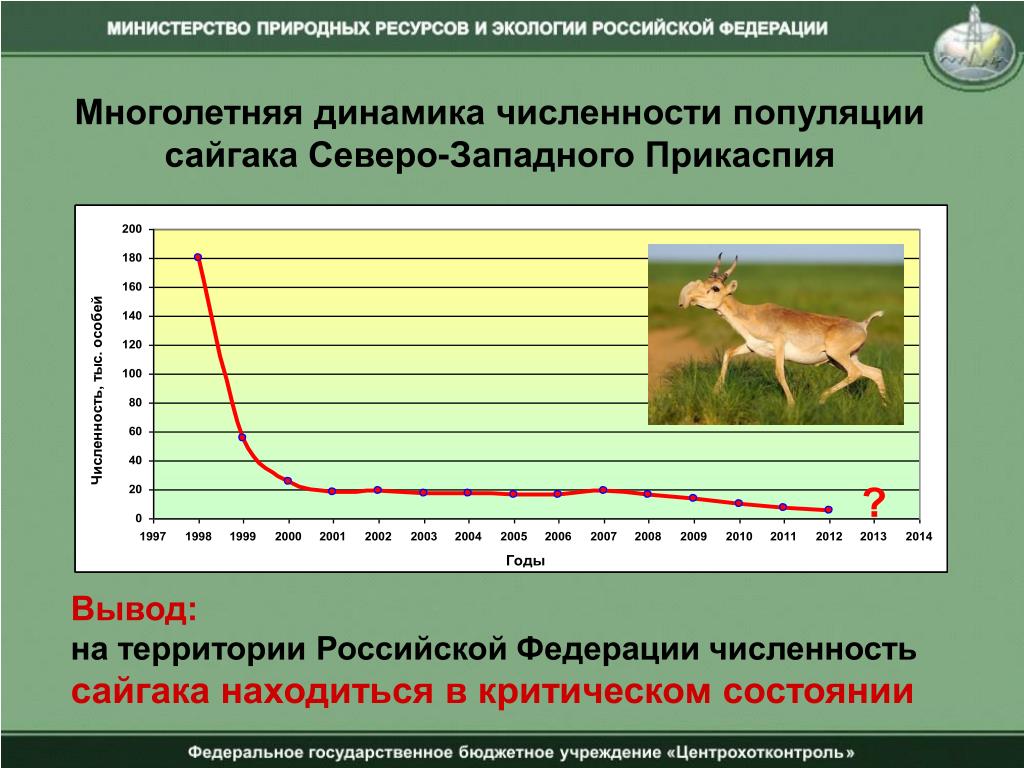 В принципе, Гептс и соавт. (6) использовали тот же метод и, что интересно, обнаружили неизменное общее количество островков у мышей ob/ob по сравнению с однопометниками без ожирения. Однако, не имея возможности объяснить эти явно расходящиеся результаты, следует упомянуть, что основанный на Викселле метод является гораздо более сильным инструментом для описания распределения объектов по размерам, а не для оценки их общего количества.
В принципе, Гептс и соавт. (6) использовали тот же метод и, что интересно, обнаружили неизменное общее количество островков у мышей ob/ob по сравнению с однопометниками без ожирения. Однако, не имея возможности объяснить эти явно расходящиеся результаты, следует упомянуть, что основанный на Викселле метод является гораздо более сильным инструментом для описания распределения объектов по размерам, а не для оценки их общего количества.
Ранее мы сообщали о линейной корреляции между взвешенным по объему средним объемом островков и общим объемом островков у крыс (7), наблюдение, которое предполагает, что увеличение общего объема островков во время физиологического роста у крыс старше 30 дней связано с к гипертрофии островков без участия гиперплазии островков, что мы и обнаружили в этом исследовании, используя прямое стереологическое измерение общего числа островков в ob/ob мышей. С другой стороны, ясно, что новые островки развиваются при определенных экспериментальных условиях, например, после частичной панкреатэктомии, где образование новых островков было четко продемонстрировано (15).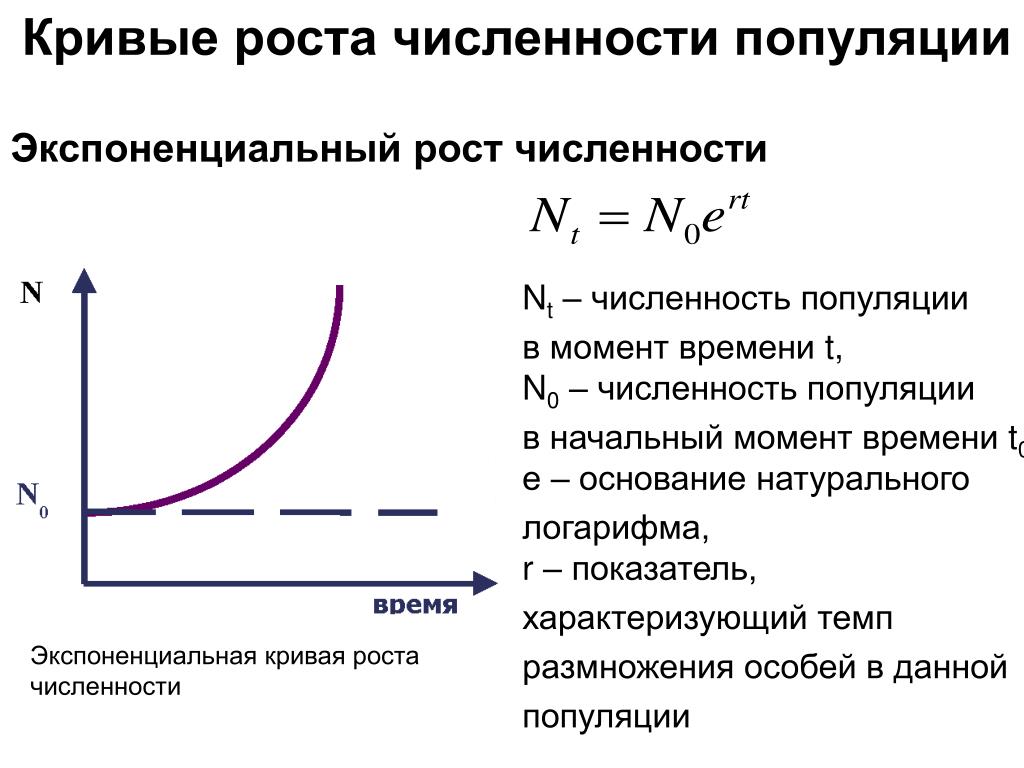 Однако увеличение массы островков в интактной поджелудочной железе из-за повышенных метаболических потребностей и регенерация поджелудочной железы после частичной панкреатэктомии не могут быть напрямую сопоставимы. Формирование новой ткани поджелудочной железы после резекции поджелудочной железы, по-видимому, повторяет эмбриональное развитие (15) и может включать экспрессию ряда факторов роста, отсутствующих в интактной поджелудочной железе.
Однако увеличение массы островков в интактной поджелудочной железе из-за повышенных метаболических потребностей и регенерация поджелудочной железы после частичной панкреатэктомии не могут быть напрямую сопоставимы. Формирование новой ткани поджелудочной железы после резекции поджелудочной железы, по-видимому, повторяет эмбриональное развитие (15) и может включать экспрессию ряда факторов роста, отсутствующих в интактной поджелудочной железе.
Очевидный вопрос, почему новые островки не образуются даже при предположительно максимальном росте общего объема островков, как это происходит у мышей ob/ob . Другие анатомические структуры, такие как почечные клубочки, также лишены способности к гиперплазии и вместо этого становятся гипертрофированными с повышенным спросом, вероятно, из-за очень специфической структуры нервно-сосудистой и канальцевой систем, необходимой для соответствующей функции. Возможно, архитектура (т. е. внутриостровковая сосудистая структура) островков настолько сложна, что позволяет формировать новые островки только во время формирования, роста или регенерации поджелудочной железы как таковой, как это происходит во время внутриутробного развития. или после частичной резекции поджелудочной железы. Однако мы не утверждаем, что новообразование островков как таковое не происходит у мышей, а скорее то, что количество новых островков, в конечном итоге образующихся, одинаково у 9 животных.мышей 0120 ob/ob и мышей ob /+, несмотря на выраженную разницу в общем объеме островков.
или после частичной резекции поджелудочной железы. Однако мы не утверждаем, что новообразование островков как таковое не происходит у мышей, а скорее то, что количество новых островков, в конечном итоге образующихся, одинаково у 9 животных.мышей 0120 ob/ob и мышей ob /+, несмотря на выраженную разницу в общем объеме островков.
Увеличение общего объема клеточной популяции может быть связано либо с увеличением числа клеток, либо с увеличением среднего клеточного объема, либо с их комбинацией. Однако, учитывая степень общего увеличения массы островков у мышей ob/ob как в предыдущих исследованиях, так и в настоящем исследовании, становится ясно, что подавляющее большинство увеличения массы островков является результатом гиперплазии островковых клеток. Если увеличение общего объема островков полностью вызвано ростом существующих островков, каковы первичные источники новых клеток (в первую очередь β-клеток)? Очевидный ответ — из клеток, уже находящихся внутри островков. Это может быть достигнуто за счет митоза внутри островковых β-клеток, событие, которое определенно происходит на основании наличия митотических фигур во внутриостровковых β-клетках (6,16) и обнаружения включения бромодезоксиуридина (BrdU) в β-клетки. также в нормальных условиях (17), или новые клетки могут быть получены из внутриостровковых стволовых клеток/клеток-предшественников, хотя существование таких клеток все еще обсуждается. Кроме того, важность митоза β-клеток подтверждается наблюдением, что 9Мыши 0120 ob/ob имеют повышенное соотношение BrdU-позитивных ядер β-клеток во время увеличения массы β-клеток (18). Клетки протоков также привлекли большое внимание, поскольку клетки способны дифференцироваться в β-клетки (19–21), и в протоках в условиях с увеличением массы β-клеток (22,23). Однако на основании результатов этого исследования можно утверждать, что эти клетки не имеют первостепенного значения для роста островковой массы в ob/ob мышей, и в отличие от скорости образования клеток протоков, положительных по PDX-1 и инсулину, скорость гибели этих клеток широко не изучалась.
Это может быть достигнуто за счет митоза внутри островковых β-клеток, событие, которое определенно происходит на основании наличия митотических фигур во внутриостровковых β-клетках (6,16) и обнаружения включения бромодезоксиуридина (BrdU) в β-клетки. также в нормальных условиях (17), или новые клетки могут быть получены из внутриостровковых стволовых клеток/клеток-предшественников, хотя существование таких клеток все еще обсуждается. Кроме того, важность митоза β-клеток подтверждается наблюдением, что 9Мыши 0120 ob/ob имеют повышенное соотношение BrdU-позитивных ядер β-клеток во время увеличения массы β-клеток (18). Клетки протоков также привлекли большое внимание, поскольку клетки способны дифференцироваться в β-клетки (19–21), и в протоках в условиях с увеличением массы β-клеток (22,23). Однако на основании результатов этого исследования можно утверждать, что эти клетки не имеют первостепенного значения для роста островковой массы в ob/ob мышей, и в отличие от скорости образования клеток протоков, положительных по PDX-1 и инсулину, скорость гибели этих клеток широко не изучалась. Тем не менее, возможность, которую не следует игнорировать, заключается в том, что β-клетки, образующиеся в протоках, могут мигрировать в существующие островки, поскольку большинство островков непосредственно прикрепляются к дереву протоков (24).
Тем не менее, возможность, которую не следует игнорировать, заключается в том, что β-клетки, образующиеся в протоках, могут мигрировать в существующие островки, поскольку большинство островков непосредственно прикрепляются к дереву протоков (24).
Таким образом, увеличение общей массы островков у мышей линии ob/ob полностью вызвано гипертрофией островков без образования дополнительных островков по сравнению с об /+ мыши. Это говорит о том, что делящиеся внутриостровковые β-клетки и, возможно, внутриостровковые прогениторные/стволовые клетки являются первичными источниками новых β-клеток во время адаптации к повышенным метаболическим потребностям. Это также предполагает, что островки Лангерганса с анатомической точки зрения представляют собой еще более уникальные структуры, чем считалось ранее, и что неогенез новых островков возможен только в таких условиях, как во время развития/роста поджелудочной железы или после частичной панкреатэктомии.
РИС. 1.
Посмотреть в большом размереСкачать слайд
На рисунке показан забор гистологических срезов. Поджелудочная железа была тщательно рассечена, и в стереологических исследованиях использовались как срезы, отмеченные как первичные, так и эталонные срезы.
РИС. 1.
Посмотреть в большом размереСкачать слайд
На рисунке показан забор гистологических срезов. Поджелудочная железа была тщательно рассечена, и в стереологических исследованиях использовались как срезы, отмеченные как первичные, так и эталонные срезы.
Режим закрытия
РИС. 2.
Просмотреть в большом размереЗагрузить слайд
Каждая отобранная первичная секция была систематически исследована, как показано в верхней части рисунка. Это было выполнено в два сеанса, во время которых либо рамка для подсчета (внизу слева на рисунке) была прикреплена к столу для подсчета островков, как описано в тексте, либо сетка для подсчета точек (внизу справа на рисунке) была прикреплена к столу. таблицу для подсчета общего объема островков, общего объема поджелудочной железы и средневзвешенного по объему объема островков, как описано в тексте.
таблицу для подсчета общего объема островков, общего объема поджелудочной железы и средневзвешенного по объему объема островков, как описано в тексте.
РИС. 2.
Просмотреть в большом размереЗагрузить слайд
Каждая отобранная первичная секция была систематически исследована, как показано в верхней части рисунка. Это было выполнено в два сеанса, во время которых либо рамка для подсчета (внизу слева на рисунке) была прикреплена к столу для подсчета островков, как описано в тексте, либо сетка для подсчета точек (внизу справа на рисунке) была прикреплена к столу. таблицу для подсчета общего объема островков, общего объема поджелудочной железы и средневзвешенного по объему объема островков, как описано в тексте.
Режим закрытия
РИС. 3.
Посмотреть в большом размереСкачать слайд
Пример подсчета дисекторов. В первичном разделе островки, обозначенные B, C и D, определяются как находящиеся внутри рамки счета, поскольку они не касаются (полных) линий исключения и либо полностью находятся в пределах рамки, либо касаются (пунктирных) линий включения. Островки, обозначенные A, E и F, определяются как находящиеся вне рамки, поскольку они либо полностью находятся вне рамки, либо касаются линий исключения. В справочном разделе, показанном внизу рисунка, островки B и D все еще присутствуют, и поэтому они не учитываются, тогда как островок C отсутствует, и, следовательно, он учитывается (см. текст для более подробной информации).
Островки, обозначенные A, E и F, определяются как находящиеся вне рамки, поскольку они либо полностью находятся вне рамки, либо касаются линий исключения. В справочном разделе, показанном внизу рисунка, островки B и D все еще присутствуют, и поэтому они не учитываются, тогда как островок C отсутствует, и, следовательно, он учитывается (см. текст для более подробной информации).
РИС. 3.
Посмотреть в большом размереСкачать слайд
Пример подсчета дисекторов. В первичном разделе островки, обозначенные B, C и D, определяются как находящиеся внутри рамки счета, поскольку они не касаются (полных) линий исключения и либо полностью находятся в пределах рамки, либо касаются (пунктирных) линий включения. Островки, обозначенные A, E и F, определяются как находящиеся вне рамки, поскольку они либо полностью находятся вне рамки, либо касаются линий исключения. В справочном разделе, показанном внизу рисунка, островки B и D все еще присутствуют, и поэтому они не учитываются, тогда как островок C отсутствует, и, следовательно, он учитывается (см. текст для более подробной информации).
текст для более подробной информации).
Режим закрытия
РИС. 4.
Посмотреть в большом размереСкачать слайд
Результаты стереологического исследования поджелудочной железы. Данные представлены в виде групповых средних с планками погрешностей, представляющими SE. A : Масса тела. B : Глюкоза крови натощак. C : Общий объем поджелудочной железы. D : Общий объем островков. E : Общее количество островков. F : Средний объем островков. G : Средний объем островков, взвешенный по объему. H : CV N (исл.). * Статистически значимое различие между группой ob/ob и группой ob /+. Фактические значения P приведены в тексте.
РИС. 4.
Посмотреть в большом размереСкачать слайд
Результаты стереологического исследования поджелудочной железы. Данные представлены в виде групповых средних с планками погрешностей, представляющими SE. A : Масса тела. B : Глюкоза крови натощак. С : Общий объем поджелудочной железы. D : Общий объем островков. E : Общее количество островков. F : Средний объем островков. G : Средний объем островков, взвешенный по объему. H : CV N (исл.). * Статистически значимое различие между группой ob/ob и группой ob /+. Фактические значения P приведены в тексте.
A : Масса тела. B : Глюкоза крови натощак. С : Общий объем поджелудочной железы. D : Общий объем островков. E : Общее количество островков. F : Средний объем островков. G : Средний объем островков, взвешенный по объему. H : CV N (исл.). * Статистически значимое различие между группой ob/ob и группой ob /+. Фактические значения P приведены в тексте.
Закрыть модально
РИС. 5.
Посмотреть в большом размереСкачать слайд
Данные о количестве островков на площадь поджелудочной железы и средней площади островков в срезах. Данные представлены в виде групповых средних с планками погрешностей, представляющими SE. A : Количество островков на область. B : Средняя площадь островка. * Статистически значимое различие между группой ob/ob и группой ob /+. Фактические значения P приведены в тексте.
Фактические значения P приведены в тексте.
РИС. 5.
Просмотреть в большом размереСкачать слайд
Данные о количестве островков на площадь поджелудочной железы и средней площади островков в срезах. Данные представлены в виде групповых средних с планками погрешностей, представляющими SE. A : Количество островков на область. B : Средняя площадь островка. * Статистически значимое различие между группой ob/ob и группой ob /+. Фактические значения P приведены в тексте.
Close modal
Эта работа была поддержана Датским исследовательским советом, Исследовательским комитетом H:S, Датской диабетической ассоциацией и Фондом Ново Нордиск.
1
Coleman DL: синдромы диабета и ожирения у мышей.
Diabetes
31 (Suppl. 1)
:
1
–6,
1982
2
Halaas JL, Gajiwala KS, Maffei M, Cohen Sl, Show Bti -Bti -Sl, Cowin Bti -Sl, Cowin Bti -Sl, Cowin Bti -Sl, Cowin Bti -Sl, Cowin Btist, S. Лаллоне Р.Л., Берли С.К., Фридман Дж.М. Эффекты снижения веса белков плазмы, кодируемых геном ожирения.
Лаллоне Р.Л., Берли С.К., Фридман Дж.М. Эффекты снижения веса белков плазмы, кодируемых геном ожирения.
Science
269
:
543
–546,
1995
3
Edvell A, LINDSTROM P: ПРОИЗВОДИТЕЛЬНОСТЬ В МОЛОДОЙ АБСИ -Гиперокемическом Гипер. Гиперогемическом стиле: Эффект.
AM J Physiol
274
:
E1034
-E1039,
1998
4
Edvell A, Lindstrom P: Разработка инсуаловальной функции in in Younge -in -incese. обь ).
Metabolism
44
:
906
–913,
1995
5
Hellman B, Brolin S, Hellerström C, Hellman K: The distribution pattern of the pancreatic islet volume in normal and мыши с гипергликемией.
Acta Endocrin
36
:
609
–616,
1961
6
Gepts W, Christophe J, Mayer J: PancReate Islets in Mice-HeLeg-HeLeGROME-HELEROME-HEGEROME. Эффект карбутамида.
Диабет
:
63
–69,
1960
7
Skau M, Pakkenberg B, Buschard K, Bock T: Linear Corpretation Mass Mass Mass-Mass-Mass-Mass-Arslet Mass-Arm-Islatation. средневзвешенный объем островков.
Диабет
50
:
1763
–1770,
2001
8
Gundersen HJ, Jensen EB: Эффективность систематической SAMPLING в стереологии.
J Microsc
147
:
229
–263,
1987
9
Sterio DC: невыразимая оценка числа и определения арбитральных. Использование DC.
J Microsc
134
:
127
–136,
1984
10
Gundersen HJ: Stereology of arbitrary particles: a review of unbiased number and size estimators and the presentation of some new те, в память об Уильяме Р. Томпсоне.
J Microsc
143
:
3
–45,
1986
11
Abercrombie M: Оценка популяции ядра из микротомических срезов.
ANAT REC
94
:
239
–247,
1946
12
Bleisch VR, Mayer J, Dickie Mmm: Familial MILTEN MICE IN MICE IN MICE IN MICE IN MICE IN MICE IN MICE, Issine IN MICE, Issin гиперплазия островков Лангерганса.
AM J PTATHOL
28
:
369
–385,
1952
13
Wicksell SD.
Biometrica
17
:
84
–99,
1925
14
Wicksell SD: The Corpuscle Проблема: Второй Memoir: Case of Ellipsidal.
Biometrica
18
:
151
–172,
1926
15
Bonner-Weir S, Baxter LA, Schuppin GT, Smith FE: A second pathway for regeneration of adult exocrine and эндокринная поджелудочная железа: возможное повторение эмбрионального развития.
Диабет
42
:
1715
–1720,
1993
16
Bonner-Weir S, Deery D, Leahy Jl, Weir GC: Cecompatory Grost of Panchary of Panchatory of Panchatory of Panchary of BeTATARY of BeTARTATION GSTATO крыс после кратковременной инфузии глюкозы.
Diabetes
38
:
49
–53,
1989
17
Scaglia L, Cahill CJ, Finegood DT, Bonner-Weir S: Apoptosis participates in the remodeling of the endocrine pancreas у новорожденных крыс.
Эндокринология
138
:
1736
–1741,
1997
18
Edvell A, Lindstrom P: Повышенная минимая.
Эндокринология
140
:
778
–783,
1999
19
Bonner-Weir S, Sharma A: Pancreatic Stem Cltle.
Дж. Патол
197
:
519
–526,
2002
20
Поджелудочная железа Петерс Дж., Юргенсен А., Клоппель Г.: дифференцировка эндогенного роста,
Virchows Arch
436
:
527
–538,
2000
21
Rosenberg L: в in vivo -трансформации: недеогензис из Beta Cltracal.
Пересадка клеток
4
:
371
–383,
1995
22
Stoffers DA, Kieffer TJ, Hussain MA, Drucker DJ, Bonner-Weir So, Habener Jf, Eanotrop, Eanotrop, Hussain Jmop, Habener Jf, Hussain Jmop, Hussain Jmop, Hussain Jmop, Hussain Jmop, Hussain Jmop, Hussain Jmop, Hussain Jmop, Hussain MA, Drucer DJ, Bonner-Weir. подобные агонисты пептида 1 стимулируют экспрессию гомеодоменового белка IDX-1 и увеличивают размер островков в поджелудочной железе мышей.
Диабет
49
:
741
–748,
2000
03
23Sharma A, Zangen DH, Reitz P, Taneja M, Lissauer ME, Miller CP, Weir GC, Habener JF, Bonner-Weir S: Гомеодоменовый белок IDX-1 увеличивается после раннего всплеска пролиферации во время регенерации поджелудочной железы.
