Кислота для очистка стекла. Как отмыть стекло кислотой
Содержание
- Традиционные способы очистки
- Синтетическая кислота для стекла EMS
- Рекомендуемые средства для очистки стекла
Необходимость отмыть стекло кислотой возникает как в производственных, так и в бытовых условиях. В первом случае это могут быть цеховые окна на улицу, в дверях, рабочие светильники, а также уличные фонари. В быту – это покрывшиеся известковым налетом окна, перегородки в душевых кабинах, стекла долго простоявшего в гараже автомобиля, теплицы.
Моющие средства для ванной комнаты
Особая проблема возникает при накоплении так называемого «водного камня». Это белесые отложения, которые образуются на оконном стекле при некачественной гидроизоляции фасада дома. Твердый налет накапливается в виде потеков и образуется из выпарившихся осадков грязных дождей, штукатурки, гипса и других смесей, которые использовались при строительстве дома.
Традиционные способы очистки
В старых чистящих средствах чаще всего использовалась кислота для стекла, а точнее, смесь нескольких жидкостей. Например, соляной, плавиковой, фосфорной с добавлением ПАВ, сульфита натрия и других агрессивных веществ. Они могли растворить карбонатный налет, но не справлялись с загрязнениями, включающими кремнистые соединения. Такие средства имеют много недостатков:
- соляная кислота активно разрушает металлическую арматуру, вызывая коррозию;
- плавиковая кислота токсична, вызывает ожоги, нужно применять меры защиты;
- разрушается поверхность стекла с образованием микротрещин.
Еще хуже получается результат, если пытаться не просто отмыть стекла кислотой, но и дополнительно использовать абразивные средства или скребки. На первый взгляд это ликвидирует проблему, но поцарапанное стекло еще быстрее накапливает отложения и стекло окажется безнадежно испорченным, его придется менять. Кроме того, с плавиковой кислотой нужно обращаться осторожно: если ее концентрация в растворе превысит 1%, стекло станет матовым.
Синтетическая кислота для стекла EMS
Производители химических средств очистки постоянно работают над улучшением состава очистителей для стекла и других материалов. Наиболее интересны разработки американского бренда EMS, чистящие средства которого сегодня можно приобрести и в российских магазинах.
Синтетическая кислота SynTech – запатентованная формула, действующая на загрязнения аналогично соляной и азотной кислоте, но в отличие от них безопасная для материалов и человека. Водород в ее составе находится в особом состоянии, с более сильной связью H+, чем в обычных технических кислотах, поэтому она действует более мягко, но также эффективно.
Свойства моющих средств EMS уникальны:
- растворяют известковый налет в два раза быстрее, чем соляная кислота;
- уничтожают патогенные микробы, благодаря использованию живых микроорганизмов;
- имеют универсальное действие – отмываю металл, стекло, бетон, пластик;
- абсолютно не вызывают коррозии металлов – D.
 O.T. равно 0, тогда как минимальный коррозионный порог составляет 6,25 мм/год;
O.T. равно 0, тогда как минимальный коррозионный порог составляет 6,25 мм/год;
Самое ценное качество синтетической кислоты для стекла SynTech: это безопасное для кожи и слизистых покровов средство, не токсичное (показатель 0), не создающее паров в воздухе. Продукция EMS одобрена Национальным фондом санитарной защиты США, имеет сертификаты категорий А1, А4, А5, А8, С1 и К1.
Рекомендуемые средства для очистки стекла
- Foro SapH Etch – средство изготовлено по технологии SynTech, аналогично по действию 32% раствору соляной кислоты, не парит. Синтетическая кислота позволяет отмыть стекло без повреждения его структуры.
- BlowOut – разрушает кальциевый налет, известь, молочный, пивной, водный камень, полностью заменяя традиционные средства на основе кислот и щелочей. Не теряет свойств при смешивании с моющими мыльными составами.
- Omni – универсальное средство для очистки любых поверхностей, включая стекло. Допускается его применение на пищевом производстве, в медицинских учреждениях, на транспорте.

- Aerosolutions Interior Cleaner – суперконцентрированное средство с дезинфицирующим эффектом. Идеально для применения в санузлах, так как содержит колонии микробных агентов, убивающих патогенную флору, и препятствует ее дальнейшему развитию.
Применение синтетической кислоты SynTech для стекла позволяет быстро очистить поверхности от трудноудаляемых налетов и не требует применения особых мер безопасности. Средства EMS экономичны в использовании, имеют практически неограниченный срок хранения.
Остались вопросы?
Характеристики плавиковой кислоты и применение в промышленности
Плавиковая кислота (фтороводородная, фтористоводородная) является неорганическим веществом, односоставной кислотой, которую получают путем растворения фтороводорода в воде. Название реактива напрямую связано с процессом получения плавиковой кислоты. Получение фтористоводородной кислоты происходит из фтороводорода, который синтезируют из плавикового шпата – минерала флюорита, способного светится под ультрафиолетом или действием высокой температуры.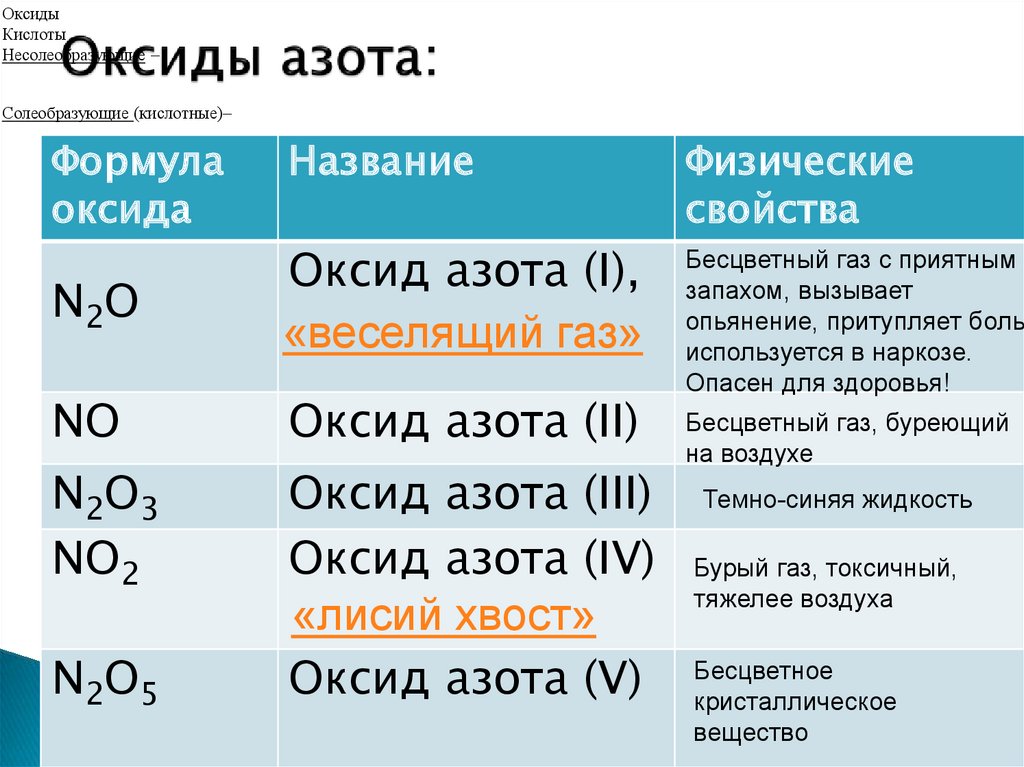
Свойства плавиковой кислоты
Фтороводородная кислота является жидкостью без цвета, но с резким запахом. Физические свойства плавиковой кислоты характеризуют вещество как не горючий, но очень токсичный реагент. Неорганическая кислота представляет опасность как для человека, так и для природы.
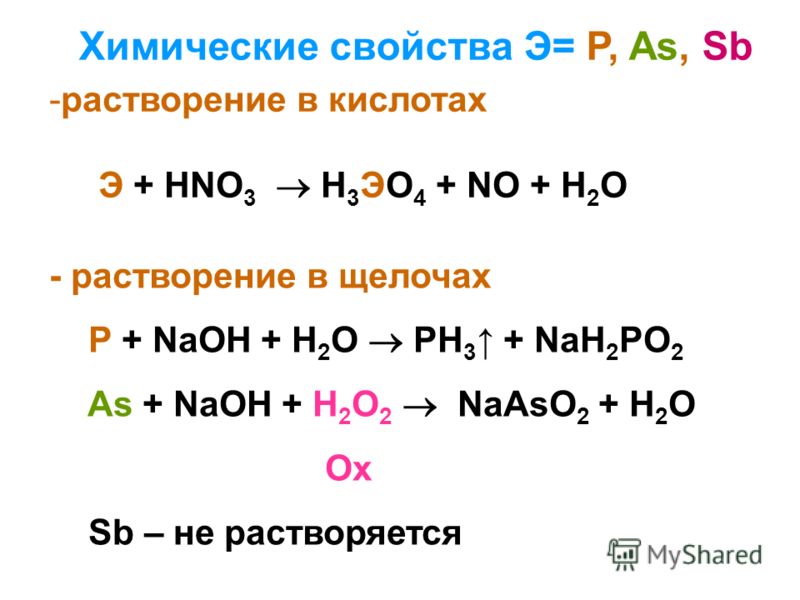
Химические свойства фтороводородной кислоты определяют реагент как кислоту средней силы, взаимодействующую с металлами и образующую фториды. Если реакция происходила с щелочным металлом, то полученная соль будет растворяться в воде, если с щелочно-земельными – растворение в воде будет происходить плохо, либо отсутствовать вообще.
Не вступает в реакции с пластмассой и каучуковыми материалами. Не растворяет некоторые металлы. Также среди особенностей плавиковой кислоты – хорошее взаимодействие с оксидом кремния, который является основой всех силикатов. Поэтом исключено хранение реагента в стеклянных емкостях.
Меры безопасности (класс опасности)
Опасность плавиковой кислоты для человека заключается и в самом растворе, и в его ядовитых парах. Разбавленная фтористоводородная кислота при попадании на кожу не вызывает никакого-раздражения или боли. Капли впитываются и проникают в кровоток, что приводит к появлению симптоматики токсического отравления, отека легких, нарушений ЖКТ и сердечно-сосудистой системы. Пары воздействуют на органы зрения и обоняния, приносят легкий наркотический эффект.
Разбавленная фтористоводородная кислота при попадании на кожу не вызывает никакого-раздражения или боли. Капли впитываются и проникают в кровоток, что приводит к появлению симптоматики токсического отравления, отека легких, нарушений ЖКТ и сердечно-сосудистой системы. Пары воздействуют на органы зрения и обоняния, приносят легкий наркотический эффект.
Поэтому присвоен 2 класс опасности фтороводородной кислоте, что обязует при работе с реагентом использовать респираторы, очки, защитные перчатки и одежду. Любые действия с веществом, включая получение фтороводородной кислоты, происходят в вытяжном шкафу.
Хранение и перевозка
Вне зависимости от того, для чего используется плавиковая кислота на конкретном производстве, ее хранение осуществляется только в пластиковых тарах при температуре не более +30 °С. Для больших емкостей используют усиление конструкции – металлическую обрешетку. Для транспортировки реагента, особенно высокой концентрации, используют ЖД и автомобили, в которые помещается ядовитое вещества в железных или стальных тарах.
Область применения плавиковой кислоты
Основные области применения фтористоводородной кислоты:
- Нефтехимия и горнодобывающая промышленность, в которых вещество используется для увеличения объемов нефтедобычи или разрушения горных пород, в составе которых имеется кремний.
- Применение плавиковой кислоты также распространяется на область выделения ряда металлов.
- Химическая индустрия, где вещество выступает в роли катализатора для получения фтористых соединений или синтетических смазок.
- Стекольная промышленность, в которой реактив используется для прозрачного травления стекла из кремния.
- Аналитическая химия, в которой вещество используется в реакциях, где необходимо растворить силикаты.
- Алюминиевая промышленность, где реактив применяют как на этапе получения легкого металла, так и при работе с ним.
- Плавиковую кислоту используют и при изготовлении полупроводников, где реагент применяется на стадии очистки и травления кремния.
- Также фтористоводородная кислота используется как одна из составляющих жидкостей, которые применяются для травления, полировки или электрохимического воздействия на сплавы и нержавеющую сталь.
Чтобы заказать фтороводородную кислоту, свяжитесь с нами по телефону или заполните соответствующую форму на сайте.
Как слабая кислота может растворить стекло? Учебное пособие
Инструменты для творчества скоро появятся, чтобы вдохновить!
Присоединяйтесь к списку рассылки, чтобы узнать, когда мы запустимся.
Химия
Общая химия
Кислоты и основания
Как слабая кислота может растворять стекло? Учебное пособие
Gayathri Mani
Стеклянный контейнер может агрессивно реагировать с плавиковой кислотой, но, как правило, он инертен или не реагирует с большинством кислот.
ВВЕДЕНИЕ:
Вы, должно быть, сталкивались с таким мастерством на куске стекла в своей повседневной жизни. Вы когда-нибудь задумывались, как были созданы эти конструкции? Пользователь делает эти рисунки на стекле с помощью процесса, называемого «травлением стекла». Способы создания произведений искусства на поверхности стекла с использованием кислотных, едких или абразивных химикатов называются травлением стекла. Шероховатая поверхность и прозрачный вид матового стекла вызваны потерей мельчайших кусочков стекла. Однако этого можно достичь только с помощью нескольких очень специфических химических веществ, поскольку стекло инертно по отношению к большинству химических веществ. Одним из таких химических веществ является плавиковая кислота, которая является слабой кислотой.
Источник
Хотите знать, что такое слабая кислота? Слабая кислота – это кислота, которая частично диссоциирует на составляющие ее ионы в водном растворе или воде. При этом давайте вернемся к нашей теме и обсудим инертность стекла по отношению к большинству химических веществ.
ИНЕРТНОСТЬ СТЕКЛА
Стекло может растворяться кислотой. Только некоторые кислоты, в основном содержащие фтор, обладают достаточной коррозионной активностью, чтобы адекватно растворять стекло. Соляная кислота не реагирует со стеклом.
ПОЧЕМУ БОЛЬШИНСТВО КИСЛОТ НЕ ВЛИЯЕТ НА СТЕКЛО?
Поскольку стекло очень устойчиво к большинству кислот, оно обычно используется для хранения кислот. Но почему большинство кислот не действуют на стекло?
Поскольку стекло имеет чрезвычайно прочную и стабильную атомную структуру, на него не действует кислота. Из-за сильных химических связей наиболее распространенный компонент стекла, диоксид кремния, является нереакционноспособным веществом, что делает стекло очень устойчивым к большинству кислот.
Растворение стекла (или любого другого материала в этом отношении) по существу представляет собой разрыв химических связей на атомном уровне. За исключением фторсодержащих кислот, большинство кислот недостаточно агрессивны для этого.
КАК КИСЛОТЫ НА ОСНОВЕ ФТОРА СПОСОБНЫ РАСТВОРЯТЬ СТЕКЛО?
Поскольку фтор имеет сильное свойство притягивать к себе электроны, кислоты, содержащие фтор, могут вызывать эрозию стекла (электроотрицательность).
Когда кислота на основе фтора, такая как плавиковая кислота, вступает в контакт со стеклом (диоксидом кремния), атом фтора притягивает к себе электроны, разрывая связь между кремнием и кислородом и растворяя стекло.
ПРОЧИЕ ПРИМЕНЕНИЯ ФТОРИСТОЙ КИСЛОТЫ
Плавиковая кислота имеет широкий спектр применения. Его можно использовать для удаления ржавчины с предметов белья. Очистка алюминия, гальваническое покрытие, подготовка поверхности для процессов производства кремния в электронике и даже в качестве реагента при синтезе широкого спектра органических соединений, содержащих фтор, — все это основные промышленные применения (например, тефлон).
Источник
На слое тефлона, который обычно используется для покрытия посуды с антипригарным покрытием, пролитое вино образует «пузыри», как видно на изображении выше.
ВЫВОД:
- Стекло может растворяться кислотой. Только некоторые кислоты, в основном содержащие фтор, обладают достаточной коррозионной активностью, чтобы адекватно растворять стекло.
- Процесс растворения стекла известен как травление стекла.
Часто задаваемые вопросы:
1. Существует ли кислота, растворяющая стекло?
Плавиковая кислота является предшественником практически всех соединений фтора и представляет собой раствор фтористого водорода (HF) в воде. Это бесцветный, чрезвычайно агрессивный раствор, способный растворять широкий спектр материалов и стекла.
2. Что растворяет стекло?
Мы дезинтегрируем стекло с помощью гидроксида натрия (очиститель канализации). Поскольку стекло почти непроницаемо для химикатов, оно является предпочтительным материалом для химических контейнеров и реакционных сосудов. С другой стороны, стекло растворяется при контакте с расплавленным гидроксидом натрия.
3. Что растворяет соляная кислота?
Соляная кислота используется для растворения различных металлов, оксидов металлов и карбонатов металлов, аналогично тому, как она используется для травления.
4. Может ли соляная кислота плавить пластик?
Пластмассы вообще плохо реагируют с кислотами, а кислотостойкие пластмассы чрезвычайно устойчивы. В результате соляная кислота не способна растворить пластик.
Мы надеемся, что вам понравился этот урок, и вы узнали что-то интересное о Может ли соляная кислота растворять стекло ! Присоединяйтесь к нашему сообществу Discord, чтобы получить ответы на любые вопросы и пообщаться с другими студентами, такими же, как и вы! Не забудьте загрузить наше приложение, чтобы испытать наши веселые классы виртуальной реальности — мы обещаем, это делает учебу намного веселее! 😎
ИСТОЧНИКИ:
- Использование плавиковой кислоты. https://www.ck12.
 org/c/chemistry/acid/rwa/How-Can-A-Weak-Acid-Dissolve-Glass/. По состоянию на 26 января 2022 г.
org/c/chemistry/acid/rwa/How-Can-A-Weak-Acid-Dissolve-Glass/. По состоянию на 26 января 2022 г. - Травление стекла. https://profoundphysics.com/can-acid-dissolve-glass/. По состоянию на 26 января 2022 г.
- Инертность стекла. https://www.britannica.com/science/водород-фторид. По состоянию на 26 января 2022 г.
Может ли кислота растворять стекло? Объяснение науки – Углубленная физика
Кислоты, особенно сильные, могут растворять множество различных веществ и материалов. Стекло, однако, не растворяется большинством веществ, но может ли кислота растворить его?
Короче говоря, кислота может растворять стекло. Однако лишь некоторые кислоты, в основном кислоты, содержащие элемент фтор, обладают достаточной коррозионной активностью, чтобы должным образом растворять стекло. Примером этого является фтористоводородная кислота, которая способна вступать в реакцию с диоксидом кремния, содержащимся в стекле, растворяя его.
Однако большинство других кислот практически не действуют на стекло. Лишь немногие кислоты действительно соответствуют химическим требованиям для растворения стекла.
Лишь немногие кислоты действительно соответствуют химическим требованиям для растворения стекла.
Содержание
Какие кислоты могут растворять стекло?
Только определенные виды кислот действительно способны растворять стекло, но какие именно?
Обычно растворяют стекло кислоты, содержащие фтор. Это связано с химической способностью фтора разрушать связи диоксида кремния, обнаруженные в стекле. Примерами кислот, которые могут растворять стекло, являются фтористоводородная кислота, фтористоводородная кислота и фторантимоновая кислота.
Below is a table of acids that can dissolve glass as well as their chemical formulas:
| Acid Capable Of Dissolving Glass | Chemical Formula |
|---|---|
| Hydrofluoric Acid | HF |
| Fluoroantimonic Acid (superacid) | H 2 FSbF 6 |
| Antimony Pentafluoride | SbF 5 |
| Fluorosulfuric Acid | HSO 3 F |
| Борнофтористая кислота | HBF 4 |

Далее в статье вы найдете дополнительную информацию о том, как эти конкретные кислоты реагируют со стеклом и способны растворять его.
Почему на стекло не действует большинство кислот?
Стекло является распространенным материалом, используемым для хранения кислот, поскольку оно обладает высокой устойчивостью к большинству кислот. Но почему именно на стекло не действует большинство кислот?
Кислота не действует на стекло, так как оно имеет очень прочную и стабильную атомную структуру. Это связано с тем, что наиболее распространенный материал в стекле, диоксид кремния, является особенно нереактивным веществом из-за его сильных химических связей, что делает стекло очень устойчивым к большинству кислот.
Итак, чтобы стекло чем-то растворялось, должна была произойти химическая реакция .
Растворение стекла (или любого другого твердого вещества в этом отношении) на самом деле просто означает разрыв химических связей на атомном уровне.
В настоящее время наиболее распространенным материалом, из которого изготавливается большинство стекол, является диоксид кремния или диоксид кремния , который имеет химическую формулу SiO 2 . Это молекула, состоящая из атома кремния и двух атомов кислорода.
Химическая связь между атомом кремния и атомами кислорода достаточно прочная, а это означает, что ее нелегко разорвать. Это, с другой стороны, означает, что стекло , как правило, достаточно устойчиво к большинству кислот .
Применительно к стеклу и кислоте, диоксид кремния, из которого изготовлено стекло должен вступить в реакцию с соединениями, содержащимися в кислоте , чтобы стекло растворилось.
Большинство кислот на самом деле недостаточно агрессивны для этого, за исключением тех, которые содержат фтор .
Типичным реальным примером этого является серная кислота, которая обычно хранится в стеклянных контейнерах.
Серная кислота, H 2 SO 4 , не способна растворять стекло, поэтому ее можно безопасно хранить в стеклянной таре. Это связано с тем, что серная кислота просто недостаточно агрессивна, чтобы разъедать чрезвычайно сильный диоксид кремния (SiO 2 ) соединения, которые являются основным компонентом стекла.
Почему кислоты на основе фтора способны растворять стекло?
Почти единственные кислоты, способные растворять стекло (реагировать с диоксидом кремния), это те, которые содержат элемент фтор .
Причина, по которой кислоты, содержащие фтор, могут растворять стекло, заключается в том, что фтор обладает очень сильной способностью притягивать к себе электроны (именно так создаются химические связи, «делясь» электронами между двумя атомами).
Эта способность называется электроотрицательностью и, по сути, является показателем того, насколько легко будут реагировать два атома.
Чем больше разница электроотрицательностей между двумя атомами, тем сильнее один из атомов будет притягивать к себе электроны и тем легче будет образоваться химическая связь между ними.
Ниже приведена таблица некоторых значений электроотрицательности различных элементов. Чтобы получить разницу электроотрицательностей между двумя элементами, просто возьмите большее значение минус меньшее значение .
| Element | Electronegativity |
|---|---|
| Silicon (Si) | 1.9 |
| Oxygen (O) | 3.4 |
| Hydrogen (H) | 2.2 |
| Chlorine (Cl ) | 3,2 |
| Фтор (F) | 4,0 |
Из этой таблицы видно, что фтор и кремний имеют большую разность электроотрицательностей (4,0 – 1,9 = 2,1) , чем кремний и кислород (3,4 – 1,9 = 1,5).
Теперь это означает, что когда кислота на основе фтора вступает в контакт со стеклом (диоксидом кремния), атом фтора сильнее притягивает к себе электроны, и, таким образом, связь между кремнием и кислородом разрывается, и стекло растворяется. .
Большая разница в электроотрицательности между фтором и кремнием является причиной того, что только кислоты на основе фтора могут растворять стекло, а что-то вроде соляной кислоты не может, хотя это очень сильная кислота.
По этой причине большинство чрезвычайно сильных кислот можно безопасно хранить в стеклянной бутылке или контейнере.
Суть в том, что для того, чтобы кислота могла растворять стекло, она должна быть кислотой на основе фтора .
Как различные кислоты растворяют стекло?
Здесь я объяснил, как различные кислоты на основе фтора реагируют со стеклом, растворяя его, а также некоторые происходящие химические реакции.
Плавиковая кислота
Возможно, наиболее распространенным является фтористоводородная кислота (HF), которая состоит из фтора и водорода, образующих кислоту при смешивании с водным раствором.
Плавиковая кислота действительно очень эффективно растворяет стекло, в результате чего от него ничего не остается.
То, как работает эта реакция, основано на том факте, что фтор имеет такую высокую электроотрицательность (способность притягивать электроны).
Он буквально похищает атомы кремния из диоксида кремния и образует с ним новые связи, образуя вещество под названием 9.0025 тетрафторид кремния . Происходит следующая химическая реакция:
Существует также другой вариант реакции, которая может произойти вместо гексафторкремниевой кислоты :
Обе эти реакции растворяют диоксид кремния (стекло) в процессе. Это связано с тем, что соединения, полученные в результате реакции (тетрафторид кремния и гексафторкремниевая кислота), будут растворяться в воде, которая также образуется в результате реакции.
Самое интересное, что здесь может быть тот факт, что фтористоводородная кислота даже не считается сильной кислотой, но все же обладает чрезвычайно сильной способностью растворять многие вещи, включая стекло.
Фторсурьмяная кислота
Другой растворяющей стекло кислотой (также на основе фтора) является фторсурьмяная кислота (H 2 FSbF 6 ).
Фторсурьмяная кислота — это суперкислота , которая легко в триллионы раз сильнее плавиковой кислоты (по определению, даже без преувеличения) и считается самой сильной кислотой в мире.
Так что, разумеется, эта кислота легко растворяет стекло. Практически единственный способ хранить фторантимоновую кислоту — в тефлоновый контейнер , так как тефлон состоит из очень прочных углерод-фтористых связей, поэтому даже суперкислота его не растворит.
Практически единственный способ хранить фторантимоновую кислоту — в тефлоновый контейнер , так как тефлон состоит из очень прочных углерод-фтористых связей, поэтому даже суперкислота его не растворит.
Пятифтористая сурьма
Еще одна кислота, растворяющая стекло при контакте с ней, – это пятифтористая сурьма
Это связано с тем, что пентафторид сурьмы будет реагировать с водой с образованием фтороводорода (= фтористоводородной кислоты) одним из следующих способов (второй способ обычно также требует некоторого количества тепла):
Образовавшаяся фтористоводородная кислота будет реагировать с диоксидом кремния в стекле, растворяя его. Вот почему, например, Национальная медицинская библиотека США не рекомендует хранить пентафторид сурьмы во влажной или сырой среде (поскольку влага содержит воду) или в стеклянных контейнерах.
